Foram encontradas 70 questões.
Em grandes cidades e em regiões muito industrializadas, o ar vai acumulando grandes quantidades de H2SO4 e HNO3. A chuva traz esses ácidos para o solo, dando origem ao fenômeno chamado de chuva ácida. Tecnicamente, a chuva ácida é qualquer chuva com pH<5,6; em regiões populosas e industriais são comuns chuvas com pH=4,5. Com base nessas informações denomine os ácidos acima na ordem que aparecem no texto.
Provas
As soluções aquosas de produtos químicos são vendidas, em geral, em concentrações elevadas, mas são quase sempre diluídas antes de serem empregadas. Isto porque evita o peso e o custo do transporte da água, além de permitir o ajuste da concentração em que o soluto será utilizado. Assim, num laboratório químico, é comum misturar duas ou mais soluções diluídas e de solventes iguais. Misturando-se 300 mL de HCl 0,4M e 200 mL de NaOH 0,8M, calcule a concentração molar da solução final em relação ao sal formado:
Provas
O sangue é vital para o funcionamento de nosso organismo. Para que as trocas gasosas ocorram normalmente, o sangue deve estar tamponado com pH em torno de 7,4.
Um dos sistemas que contribuem para o tamponamento do sangue é formado por:
Provas
Em uma titulação ácido-base, faz se reagir um ácido com uma base até atingir o ponto de equivalência, que pode ser determinado empregando-se um indicador ácido-base, ou por meio do ponto de inflexão da curva de titulação, que pode ser obtida empregando-se um medidor de pH (pHmetro). Suponha que 20,00 ml de uma solução de ácido oxálico, H2C2O4, seja titulada com 0,100 M de NaOH(aq) e que o ponto estequiométrico fosse atingido quando 40,00 ml da solução básica fosse adicionada.
Qual a molaridade da solução ácida do ácido oxálico?
Reação: H2C2O4(aq) + NaOH(aq) !$ \rightarrow !$ Na2C2O4(aq) + H2O(l)
Provas
A destilação é um processo físico que serve para desdobrar as misturas homogêneas, como as soluções de sólidos em líquidos (destilação simples) ou as soluções de dois ou mais líquidos (destilação fracionada). A destilação tende a ser mais perfeita quanto maior for a diferença entre as temperaturas dos dois líquidos, nesse caso sairá por último:
Provas
Em uma visita ao supermercado, percebe-se a oferta de vários produtos para a limpeza doméstica. No entanto, assim como um produto age sobre a sujeira, este também pode deteriorar a superfície metálica. Como prevenção, existem os revestimentos protetores que geralmente são aplicados sobre superfícies metálicas e impedem ou minimizam o processo de corrosão. Abaixo estão alguns valores de potenciais-padrão de eletrodos. Após a análise dos valores de potenciais-padrão apresentados na tabela abaixo, pode-se concluir que um procedimento para proteger o níquel da corrosão em ambientes onde esteja exposto à água e ao gás oxigênio, é revestir a superfície de cobre com:
Alguns valores de potencial padrão de eletrodo.
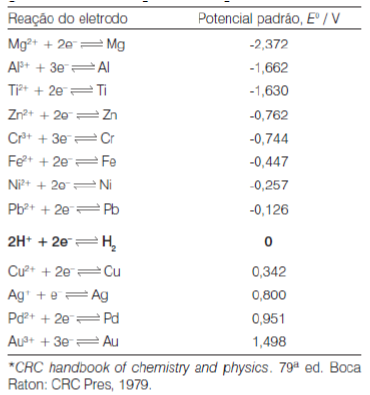
(Revista Química Nova na Escola, N19, maio, 2004.)
Provas
Na Química é comum o uso de reagentes impuros, principalmente em reações industriais, ou porque são baratos ou porque já são encontrados na natureza acompanhados de impurezas (o que ocorre, por exemplo, com os minérios). Dessa forma, se uma amostra de 120 g de magnésio com 70% de pureza reage com oxigênio, produzindo óxido de magnésio.
Determine a massa de óxido de magnésio produzida.
(Dadas massas molares: Mg= 24g/mol; MgO= 40g/mol).
Provas
Uma solução tampão de qualquer pH desejado pode ser preparada pela combinação de quantidades calculadas de um par ácido-base conjugado adequado. Na prática, porém, os valores de pH de tampões preparados em laboratório utilizando quantidades teóricas diferem dos valores previstos, por conta de incertezas nos valores numéricos de muitas constantes de dissociação e das simplificações utilizadas nos cálculos. Em virtude disso, é comum se prepararam tampões gerando uma solução cujo pH seja aproximadamente aquele desejado, e então o ajustam pela adição de um ácido forte ou base forte até que o pH requerido seja indicado por um pH-metro. Assim, para preparar 400 ml de uma solução tampão com pH= 5,00 a partir do ácido acético (HOAc) e acetato de sódio (NaOAc) 1,00 mol/L, a concentração e a massa de acetato de sódio respectivamente devem ser aproximadamente iguais a: (Dados: ka = !$ \dfrac {[H30^+][0Ac^-]} {[HOAc]} !$ = 1,75 x 10-5 e Massa molar de NaOAc = 82,034 g )
Provas
Para "fixação do nitrogênio", ou seja, para transformar o nitrogênio gasoso em algum composto sólido ou líquido, havia várias possibilidades, que podem ser percebidas na figura abaixo. O N2(g) pode ser oxidado aos óxidos, pode ser oxidado aos ânions ou pode ser reduzido a outros compostos, inclusive amônia. A conversão aos óxidos é termodinamicamente desfavorável, porém a altas temperaturas a formação dos mesmos passa a ser factível. As outras duas possibilidades já são favorecidas termodinamicamente, porém em todos os casos há a barreira cinética da inércia do N2(g). Entretanto, com o desenvolvimento da Termodinâmica e da Cinética, principalmente os estudos de catálise, a síntese da amônia foi viabilizada em condições específicas no processo Haber-Bosh.
Analisando a equação química que representa a síntese da amônia e considerando o Princípio de Le Chatelier, identifique uma das condições necessárias que favorece a produção de grandes quantidades de amônia.
N2(g) + 3 H2(g) !$ \leftrightarrows !$ 2NH3(g) !$ \Delta !$H= - 92,22 KJ
Provas
Nos grandes centros urbanos, onde há um número elevado de veículos automotores, se tem observado o fenômeno do smog fotoquímico. O smog é caracterizado pela presença de substâncias irritantes, coloração castanha (devido a presença de NO2) e constitui um material coloidal, formado por material particulado e gases diversos, denominado:
Provas
Caderno Container