Foram encontradas 50 questões.
Considere se necessário:

O ácido benzóico é um composto aromático, de fórmula química !$ C_7H_6O_2 !$, pertencente ao grupo dos ácidos carboxílicos, descoberto em meados do século XVI. Trata-se do mais simples dos ácidos carboxílicos (uma carboxila, COOH ligada a um anel benzênico), praticamente insolúvel em água, mas solúvel em solventes orgânicos menos polares, como éteres, alcoóis e benzeno. O nome oficial do ácido benzóico é ácido-benzenomonocarboxílico. Pela sua propriedade antimicrobiana, o ácido benzóico é muito utilizado pela indústria alimentícia para conservação de alimentos e pela indústria farmacêutica na produção de cosméticos e medicamentos, principalmente de antifúngicos. Há outros processos em que esse ácido é aplicado como a síntese de corantes, produção de resinas alquílicas, produtos plastificantes, componente de cremes dentais, etc.
Disponível em: <http://www.infoescola.com/quimica/acido-benzoico/>.
Uma amostra de ácido benzóico com massa de 1,250g foi colocada em uma bomba de combustão. A bomba foi preenchida com excesso de oxigênio em alta pressão, selada e imersa em um recipiente com água que atuou como calorímetro. A capacidade calorífica de todo o aparelho (bomba, recipiente, termômetro e água) era 10134J/K. A oxidação do ácido benzóico foi iniciada lançando uma fagulha elétrica na amostra. Após a combustão total, o termômetro imerso na água registrou uma temperatura 3,256K maior que a temperatura inicial. Através do processo realizado, pode-se afirmar que o valor da variação da energia, por mol, de ácido benzóico queimado foi de aproximadamente:
Provas
Considere se necessário:

Durante um experimento no laboratório químico, o éter metil terbutílico (MTBE), de fórmula!$ (CH_3)_3COCH_3 !$, que é usado como aditivo na gasolina vendida em várias áreas urbanas, é obtido através da reação do metanol com o isobuteno, de acordo com a seguinte equação:
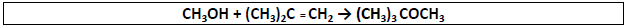
Se 45,0kg de metanol são colocados para reagir com 70,0kg de isobuteno, qual é o valor aproximado da massa máxima de MTBE que foi obtido durante a reação?
Provas
Considere se necessário:

As Leis de Faraday da eletrólise são:
1ª A massa de qualquer substância liberada ou depositada em um eletrodo é proporcional à carga elétrica;
2ª As massas de diferentes substâncias liberadas ou depositadas por uma mesma quantidade de eletricidade são proporcionais às massas equivalentes dessas substâncias.
Baseando-se nas Leis de Faraday, pode-se afirmar que, quando uma mesma quantidade de eletricidade que liberou 2,158 g de Ag passar por uma solução de sal de ouro, causando a deposição de 1,314g de Au, haverá a produção de uma massa equivalente de ouro de aproximadamente:
Provas


Provas
Considere se necessário:

Um cilindro de gás, cuja pressão máxima suportada é de 8,0atm, está em uso num laboratório de uma empresa. Ele foi calibrado com pressão interna equivalente a 3,0atm numa temperatura constante de 27°C. Após um acidente industrial, ocorreu o desligamento do sistema de resfriamento e a temperatura do cilindro alcançou o valor de 47°C. Considerando que o gás que ocupa o cilindro é ideal e que o mesmo sofreu uma transformação isocórica, qual a pressão máxima que o cilindro alcançou em função do aumento da temperatura?
Provas
Considere se necessário:

Os fertilizantes são compostos químicos utilizados na agricultura para aumentar a quantidade de nutrientes do solo e, consequentemente, conseguir um ganho de produtividade. Atualmente, são muito utilizados, ainda que paguemos um alto preço por isso. Entre os problemas estão: a degradação da qualidade do solo, a poluição das fontes de água e da atmosfera e aumento da resistência de pragas. Existem dois grandes grupos de fertilizantes: os inorgânicos e os orgânicos. O primeiro é formado por compostos químicos não naturais, feitos a partir de nutrientes específicos, necessários ao crescimento das plantas. Os mais comuns levam nitrogênio, fosfatos, potássio, magnésio ou enxofre e a maior vantagem desse tipo de fertilizante está no fato de conter grandes concentrações de nutrientes que podem ser absorvidos quase que instantaneamente pelas plantas.
Disponível em: <http://www.ecycle.com.br/component/content/article/35/1329-como-o-que-usofertilizantes- agricultura-emissoes-desequilibrio-efeito-estufa-problema-aquecimento-global-contaminacaomeio- ambiente.html>
Se um fertilizante é um composto de !$ KNO_3 !$ (nitrato de potássio) quase puro, qual é a porcentagem de nitrogênio que deve está informada na embalagem desse produto?
Provas
Provas

| Temperatura | Solubilidade em 100g de água |
| 25°C | 40g de sal |
| 60°C | 70g de sal |
Provas
Considere se necessário:

Considere as seguintes etapas de uma técnica de laboratório, chamada titulação, que requer o entendimento de estequiometria em solução: Uma reação na fase de solução é realizada sob condições controladas para que a quantidade de um reagente possa ser determinada com alta precisão. Uma quantidade medida cuidadosamente é colocada em um béquer, um corante chamado indicador pode ser adicionado à solução e um segundo reagente é inserido de maneira controlada, normalmente usando uma bureta. Quando a reação se completa, o indicador muda de cor. Em uma determinação experimental envolvendo essa técnica, 22ml de solução de NaOH a 0,50mol/L foi usado para titular uma amostra de 20mL de ácido sulfúrico. Qual dos valores abaixo melhor representa a concentração do ácido utilizado na titulação?
Provas
Considere se necessário:

A presença de !$ SO_2 !$ na atmosfera e o ácido sulfúrico que ele produz resultam no fenômeno da chuva ácida. Os ácidos da chuva ácida ou de outras fontes não são uma ameaça para os lagos onde a rocha é o calcário, que pode neutralizar o excesso de ácido. Entretanto, onde a rocha é o granito, nenhuma neutralização desse tipo ocorre. Sabendo disso, determine a massa mínima de cal, CaO, necessária para elevar o pH de 4,0 para 5,0 de um pequeno lago com volume 2,0 x !$ 10^9 !$litros.
Provas
Caderno Container