Foram encontradas 857 questões.
Observe as afirmações sobre os sólidos covalentes descritas abaixo:
I Um sólido covalente é muito duro.
II Um exemplo de sólido covalente é o K2CO3.
III A condutividade de um sólido covalente é baixa.
IV A força da ligação entre as unidades se dá pela força dipolo-dipolo.
Qual alternativa apresenta as afirmativas corretas?
Provas
Observe as afirmações sobre os sólidos iônicos descritas abaixo:
I Os sólidos iônicos são moles.
II A condutividade de um sólido iônico é baixa.
III O ponto de fusão dos sólidos iônicos é muito baixo.
IV As unidades nos pontos reticulares são formadas por íons negativos e positivos.
Qual alternativa apresenta as afirmativas corretas?
Provas
Relacione a geometria molecular com a sua respectiva representação gráfica:
I Trigonal Plana
II Tetraédica
III Linear
1 -
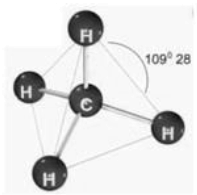
2 -
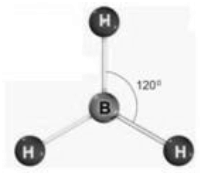
3 -

Qual alternativa apresenta a relação correta entre a geometria molecular e a sua representação gráfica?
Provas
Observe as estruturas gerais dos seguintes compostos:
Composto 1: R --- SH
Composto 2: R---- O ----- R’
Podemos classificar, respectivamente, os compostos 1 e 2 como sendo:
Provas
As simetrias são uma forma de classificação das moléculas. As moléculas de CH4 e CCl2 estão em um mesmo grupo, pois ambas possuem os elementos de simetria de um:
Provas
Correlacione os tipos de isomeria às suas respectivas características:
I Isomeria de ligação
II Isomeria de ionização
III Isomeria de hidratação
IV Isomeria de coordenação
a. Origina-se quando um dos ligantes é o H2O.
b. O mesmo ligante pode ligar-se através de diferentes átomos.
c. Ocorre quando um ligante e um contra-íon trocam de posição em um composto.
d. Origina-se quando há dois íons complexos diferentes que podem se formar a partir da mesma fórmula molecular.
Assinale a alternativa que apresenta a ordem CORRETA de correlação, de cima para baixo:
Provas
O que é a carga formal de um átomo?
Provas
É de competência da termoquímica, estudar a ocorrência de variações de energia durante os processos de transformação química. Essas transformações podem ser observadas pelo rearranjo dos átomos formando uma nova estrutura, acompanhada do desprendimento (processo exotérmico) ou absorção (processo endotérmico) de energia sob várias formas.
Observe as reações a seguir.
I H2(g) + ½ O2(g) → H2O(g) ΔH = A kcal
II H2(L) + ½ O2(g) → H2O(g) ΔH = B kcal
III H2(S) + ½ O2(g) → H2O(g) ΔH = C kcal
Assinale a alternativa que apresenta a relação entre os valores de A, B e C, em módulo, e o valor do ΔH CORRETOS:
Provas
Considerando as forças relativas dos ácidos e das bases, avalie as afirmativas abaixo sobre a reação entre o NH4CL e o NaCO3:
I O cloreto de amônio dissocia-se para formar os íons NH-4 e Cl- em água. O íon amônio é um ácido forte e o íon cloreto é uma base fraca.
II O carbonato de sódio dissocia-se em água para dar os íons Na+ e CO2-3. O íon sódio não reage apreciavelmente com a água; já o íon carbonato é uma base.
III A base conjugada do NH4Cl é o íon OH-, e o ácido conjugado do NaCO3 é o NaCl.
Está correto apenas o que se afirma em:
Provas
Nas fórmulas numeradas de 1 a 5 na tabela abaixo, quais são os elementos da família do metal?

Provas
Caderno Container