Foram encontradas 30 questões.
( ) Dalton afirmava que os átomos são permanentes e indivisíveis e que as transformações químicas consistem em uma separação, combinação ou rearranjo de átomos. Sua teoria contribuiu para explicação da conservação das massas em uma reação química.
( ) Após lançar o modelo de “pudim de ameixas" o físico inglês J. J. Thomson, anos mais tarde, postulou que os elétrons, carregados negativamente, estavam arranjados em anéis e circundavam completamente em órbitas a esfera positiva.
( ) Rutherford apresentou um modelo de átomo que possuía um pequeno núcleo rodeado por um grande volume no qual os elétrons estão distribuídos. O núcleo carrega toda a carga positiva e também toda massa do átomo.
( ) Bohr desenvolveu um modelo atômico no qual postulou a existência de níveis de energia eletrônica quantizada. O mesmo atentou para o fato de que os elementos exibem um espectro de linhas.
Assinale a seguir a alternativa CORRETA, na sequência de cima para baixo:
Provas
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
O ácido sulfúrico é muito importante na indústria, pois é utilizado no refino de petróleo, na fabricação de explosivos, na indústria de fertilizantes, bem como emprego para obtenção de outros ácidos. Este é considerado um _______________, pois apresenta _______________, possuindo fórmula molecular_______________.
Assinale a alternativa que completa, CORRETA e respectivamente, as lacunas do texto acima:
Provas
Com relação ao equilíbrio químico e aos fatores que o deslocam, assinale a alternativa CORRETA.
Provas
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química OrgânicaCadeias Carbônicas
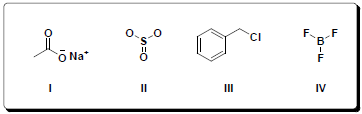
Considerando as estruturas dos compostos abaixo, assinale a alternativa CORRETA em relação às ligações químicas estabelecidas entre seus átomos constituintes.
Provas
- Química CinéticaTransformações Químicas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Em um laboratório de química analítica, um estudante encontrou um frasco com uma solução contendo, o seguinte rótulo: “cátion do grupo IV”. Para rotular corretamente, o aluno realizou alguns testes com alguns reagentes comuns para identificação de cátions do grupo IV e fez as seguintes observações:
1º) Ao fazer o teste utilizando solução de amônia, nenhum precipitado foi observado;
2º) Empregando uma solução de carbonato de amônio, um precipitado de cor branca foi formado, sendo este solúvel em ácidos minerais diluídos;
3º) Após utilizar ácido sulfúrico diluído, ocorreu a precipitação de um sólido branco, pesado e finamente dividido, que foi praticamente insolúvel em água.
Com base nos testes e observações do estudante, o cátion presente no frasco mal rotulado é?
Provas
Este relato é um histórico importante sobre o elemento ferro, que pode ser obtido através da hematita (óxido férrico). Para a formação da hematita ocorre uma reação entre ferro metálico e gás oxigênio. Considerando este processo químico, quantas gramas de hematita, podem ser obtidas quando 20 mols de ferro reagem com quantidade suficiente de oxigênio? Assinale a alternativa CORRETA.
Provas
Provas
I. Amostragem casual é o melhor método de amostragem a ser adotado, pois permite que todo o material seja analisado.
II. Uma amostra representativa permite estimar uma ou mais características para a totalidade de uma população.
III. Em líquidos, a homogeneidade do material a ser amostrado pode ser garantida pelo processo de agitação.
IV. Amostras sólidas sempre são homogêneas e não requerem procedimentos prévios à coleta.
Assinale a alternativa em que todas as afirmativas estão CORRETAS:
Provas
Caderno Container