Foram encontradas 30 questões.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
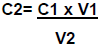
onde:
C2 = Concentração da solução em estudo.
C1 = Concentração da solução padrão.
V1 = volume gasto na bureta.
V2 = Volume da alíquota.
Considerando que cada uma das variáveis tenha incerteza padrão já identificada e quantificada ( uC1,uV1,uV2), e sabendo que no cálculo da incerteza final de um procedimento todas as contribuições de incertezas, expressas como padrão, podem ser combinadas, assinale a alternativa que apresenta a expressão que deve ser utilizada para o cálculo da incerteza combinada (uc).
Provas
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Provas
Uma solução tampão foi preparada a partir da mistura de uma solução 1,00 M de hidróxido de amônio (NH4OH) com uma solução 1,00 M de cloreto de amônio (NH4Cl), totalizando 1,0 litro. Em seguida foi adicionado 0,20 mol de OH- a solução tampão e o pH calculado. Sabendo que o valor de pKb é igual a 4,74, o pH da solução após a adição de 0,20 mol de OH- é igual a:
(Dado Kb:1,8 x 10-5; log de 0,66 = - 0,176)
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
1ª análise: foram gastos na titulação 21,3 mL da amostra de NaOH.
2ª análise: foram gastos na titulação 22,0 mL da amostra de NaOH.
3ª análise: foram gastos na titulação 21,5 mL da amostra de NaOH.
(Dado: equação da reação, NaOH(aq) + HOOCC6H4COOK(aq) → NaOOCC6H4COOK(aq) + H2O(liq); NaOH = 40,00 g mol-1 e KHC8H4O4 = 204, 22 g mol-1).
A concentração da solução de NaOH padronizada é:
Provas
Quando um sal se dissolve em água, a solução pode ser ácida, básica ou neutra, dependendo da natureza do sal. Sabendo disso, é correto afirmar que a hidrólise do acetato de amônio (NH4C2H3O2) em água resulta em uma solução:
(Dado: Ka do ácido acético = 1,8 x 10-5 e Kb da amônia = 1,8 x 10-5).
Provas
As pilhas e baterias são amplamente utilizadas em nossa sociedade como fonte de energia para diversos aparelhos eletroeletrônicos. Do ponto de vista químico, a energia elétrica fornecida por uma pilha é oriunda de uma reação de oxirredução espontânea. Uma pilha de mercúrio, que é utilizada em marca-passos, envolve as seguintes semi-reações e os respectivos potenciais padrão (Eº) a 25 ºC:
ZnO + H2O + 2e-
 Zn + 2OH- (Eº = -
1,26 V)
Zn + 2OH- (Eº = -
1,26 V) HgO + H2O + 2e-
 Hg + 2OH- (Eº =
0,098 V)
Hg + 2OH- (Eº =
0,098 V)Com relação à pilha, a alternativa INCORRETA é:
Provas
Caderno Container