Foram encontradas 40 questões.
- Química CinéticaReações e Soluções
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Avalie as afirmativas abaixo e assinale a alternativa em que (todas) a(s) afirmativa(s) está(ão) CORRETA(S):
I. O coeficiente de atividade é um fator utilizado para levar em conta a não-idealidade de uma solução.
II. Se a solução for ideal, o coeficiente de atividade será igual a 1.
III. Se a solução for real, deve-se considerar o coeficiente de atividade igual a zero.
Provas
Suponha que 1000 gramas de um líquido hipotético, quando é mantida constante sua temperatura de ebulição, seja submetido a uma pressão constante de 100 KPa e à adição de 2500 KJ de calor, convertendo o líquido em vapor. Nessa condição os volumes específicos do líquido e do vapor são 0,001 e 1,001 m3kg-1 respectivamente. Baseado nessas informações, o valor de ΔU é:
Provas
Suponha que 1000 gramas de um líquido hipotético, quando é mantida constante sua temperatura de ebulição, seja submetido a uma pressão constante de 100 KPa e à adição de 2500 KJ de calor, convertendo o líquido em vapor. Nessa condição os volumes específicos do líquido e do vapor são 0,001 e 1,001 m3kg-1 respectivamente. Baseado nessas informações, o valor de ΔH é:
Provas
As propriedades termodinâmicas podem ser divididas em duas classes gerais: as extensivas e intensivas. Das alternativas abaixo, qual delas NÃO se enquadra como uma propriedade intensiva?
Provas
Uma queda d’agua (cachoeira) representa um sistema onde ocorre a conversão de energia cinética em energia potencial, embora a quantidade de energia total do sistema, permaneça constante. Esse exemplo representa qual(is) lei(s) termodinâmica(s)?
Provas
Baseado no diagrama abaixo (H2O – NaCl), assinale a alternativa CORRETA.

Fonte: KORETSKY, M. D. Termodinâmica para Engenharia Química. Rio de Janeiro; LTC, 2007.p.388.
Provas
Para uma espécie que se aproxima do seu limite de diluição infinita, a sua fração molar se aproxima de:
Provas
Determine o grau de liberdade do seguinte sistema em equilíbrio: solução saturada de sal em água, com presença de corpo de fundo, a qual se apresenta no seu ponto de ebulição.
Provas
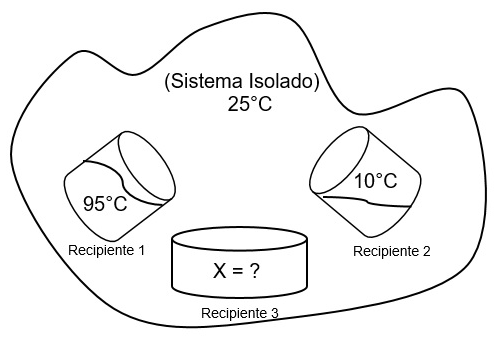
A figura esquemática abaixo representa um sistema isolado. No recipiente 3 são misturadas as duas substâncias contidas nos recipientes 1 e 2, as quais são totalmente miscíveis entre si. Pode-se concluir que a temperatura (X) do recipiente 3 após o equilíbrio:
Provas
Considere o quadro a seguir:
Sistema → | A | B | C |
Volume inicial →(L) | 200 | 200 | 400 |
Volume final →(L) | 400 | 400 | 400 |
Temperatura inicial →(K) | 100 | 100 | 100 |
Temperatura final →(K) | 100 | 200 | 200 |
Pressão inicial →(Pa) | 1 | 2 | 1 |
Pressão final →(Pa) | 2 | 2 | 2 |
Marque a alternativa que apresenta os sistemas na seguinte ordem: isotérmico, isobárico e isométrico.
Provas
Caderno Container