Foram encontradas 40 questões.
O sabão é utilizado há milhares de anos, e a reação de saponificação é uma das
reações mais antigas conhecidas pelo homem. Assinale a alternativa que apresenta um dos produtos
obtidos a partir da reação abaixo. 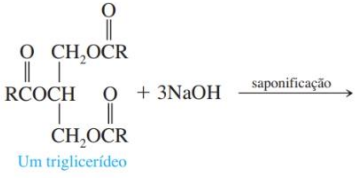

Provas
Questão presente nas seguintes provas
As aulas práticas no ensino de química têm uma importância indiscutível. Embora se
reconheça a existência de fatores limitantes para a proposição de aulas práticas, como ausência de
laboratório, falta de tempo para preparação, falta de equipamentos, entre outros, um pequeno número
de atividades práticas, desde que interessantes e desafiadoras, já será suficiente para proporcionar
um contato direto com os fenômenos, organizar e interpretar dados, entre outros. Relacione a
Coluna 1 à Coluna 2, associando as atividades práticas a seguir às suas características.
Coluna 1
1. Experimentos ilustrativos.
2. Demonstrações práticas.
3. Experimentos investigativos.
4. Experimentos descritivos.
Coluna 2
( ) Atividades realizadas pelo professor. Possibilitam ao aluno maior contato com os fenômenos já conhecidos e com equipamentos, instrumentos, fenômenos e até seres vivos.
( ) Atividades que os alunos podem realizar e que cumprem as mesmas finalidades das demonstrações práticas.
( ) Atividades que o aluno realiza e que não são obrigatoriamente dirigidas o tempo todo pelo professor. Nelas, o aluno tem contato direto com coisas ou fenômenos que precisa apurar, sejam comuns ou não ao seu dia a dia. Aproximam-se das atividades investigativas, porém não implicam a realização de testes de hipóteses.
( ) Atividades práticas que exigem participação ativa do aluno durante sua execução. Diferem das outras por envolverem obrigatoriamente discussão de ideias, elaboração de hipóteses investigativas e experimentos para testá-las.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Coluna 1
1. Experimentos ilustrativos.
2. Demonstrações práticas.
3. Experimentos investigativos.
4. Experimentos descritivos.
Coluna 2
( ) Atividades realizadas pelo professor. Possibilitam ao aluno maior contato com os fenômenos já conhecidos e com equipamentos, instrumentos, fenômenos e até seres vivos.
( ) Atividades que os alunos podem realizar e que cumprem as mesmas finalidades das demonstrações práticas.
( ) Atividades que o aluno realiza e que não são obrigatoriamente dirigidas o tempo todo pelo professor. Nelas, o aluno tem contato direto com coisas ou fenômenos que precisa apurar, sejam comuns ou não ao seu dia a dia. Aproximam-se das atividades investigativas, porém não implicam a realização de testes de hipóteses.
( ) Atividades práticas que exigem participação ativa do aluno durante sua execução. Diferem das outras por envolverem obrigatoriamente discussão de ideias, elaboração de hipóteses investigativas e experimentos para testá-las.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
O álcool amílico, C5H11OH, apresenta a reação de combustão a seguir:
C5H11OH + O2 → CO2 + H2O
Com base nessa equação, assinale a alternativa correta.
C5H11OH + O2 → CO2 + H2O
Com base nessa equação, assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
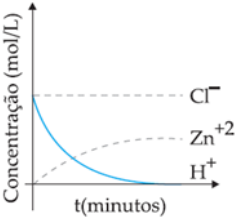
O gráfico a seguir representa a variação de concentração com o tempo durante a
reação de ácido clorídrico com zinco metálico. Analise-o e assinale a alternativa correta.

Provas
Questão presente nas seguintes provas
A Tabela Periódica pode ser usada na predição de inúmeras propriedades, muitas das
quais são cruciais para a compreensão da Química. Em relação à classificação periódica dos elementos
e propriedades periódicas, assinale a alternativa INCORRETA.
Provas
Questão presente nas seguintes provas
Sobre ligações químicas, analise as assertivas a seguir assinale V, se verdadeiras, ou
F, se falsas.
( ) A teoria dos orbitais moleculares é a que melhor descreve a ligação química, pois resolve as deficiências da Teoria de Lewis e é mais simples na utilização dos cálculos quando comparada à Teoria de Valência.
( ) Nas ligações múltiplas, um átomo forma uma ligação “sigma” usando um orbital híbrido (sp ou sp2 ) e uma ou mais ligações “pi” usando orbitais não hibridados. A superposição lateral que produz uma ligação “pi” não restringe a rotação das moléculas, resultando em ligações mais fracas do que as ligações “sigma”, não impedindo que átomos maiores formem ligações múltiplas.
( ) Os diagramas de níveis de energia de orbitais moleculares de moléculas diatômicas heteronucleares são fáceis de predizer qualitativamente. Entretanto, são dificilmente calculados usando softwares específicos disponíveis.
( ) Na Teoria dos Orbitais Moleculares, todos os elétrons de valência estão deslocalizados sobre toda a molécula, isto é, não pertencem a alguma ligação específica.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
( ) A teoria dos orbitais moleculares é a que melhor descreve a ligação química, pois resolve as deficiências da Teoria de Lewis e é mais simples na utilização dos cálculos quando comparada à Teoria de Valência.
( ) Nas ligações múltiplas, um átomo forma uma ligação “sigma” usando um orbital híbrido (sp ou sp2 ) e uma ou mais ligações “pi” usando orbitais não hibridados. A superposição lateral que produz uma ligação “pi” não restringe a rotação das moléculas, resultando em ligações mais fracas do que as ligações “sigma”, não impedindo que átomos maiores formem ligações múltiplas.
( ) Os diagramas de níveis de energia de orbitais moleculares de moléculas diatômicas heteronucleares são fáceis de predizer qualitativamente. Entretanto, são dificilmente calculados usando softwares específicos disponíveis.
( ) Na Teoria dos Orbitais Moleculares, todos os elétrons de valência estão deslocalizados sobre toda a molécula, isto é, não pertencem a alguma ligação específica.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
Existem milhares de processos eletroquímicos envolvidos em reações químicas e
biológicas, na fabricação de produtos e na pesquisa e no desenvolvimento de novas tecnologias.
Portanto, o estudo eletroquímico é fundamental, sendo importante ter um bom entendimento dos
principais conceitos para compreender todos os fenômenos envolvidos. Nesse sentido, analise a célula
galvânica a seguir e assinale a alternativa INCORRETA. 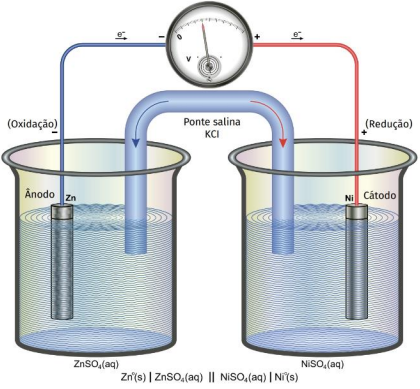

Provas
Questão presente nas seguintes provas
Em relação à termoquímica, analise as assertivas abaixo, assinalando V, se
verdadeiras, ou F, se falsas.
( ) A variação de entalpia (ΔH) de um sistema informa a quantidade de calor trocado por esse sistema à pressão constante. O sinal de ΔH informa se o processo é exotérmico ΔH>0 ou endotérmico ΔH<0.
( ) A representação de uma equação termoquímica deve incluir os coeficientes estequiométricos de todos os participantes e o ΔH do processo.
( ) A entalpia padrão de formação (ΔH0f) é positiva para as substâncias simples, desde que estejam no estado-padrão, no estado físico e na variedade alotrópica mais estável.
( ) Os valores ∆H são numericamente iguais, mas de sinais opostos, para reações químicas que sejam o inverso uma da outra.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
( ) A variação de entalpia (ΔH) de um sistema informa a quantidade de calor trocado por esse sistema à pressão constante. O sinal de ΔH informa se o processo é exotérmico ΔH>0 ou endotérmico ΔH<0.
( ) A representação de uma equação termoquímica deve incluir os coeficientes estequiométricos de todos os participantes e o ΔH do processo.
( ) A entalpia padrão de formação (ΔH0f) é positiva para as substâncias simples, desde que estejam no estado-padrão, no estado físico e na variedade alotrópica mais estável.
( ) Os valores ∆H são numericamente iguais, mas de sinais opostos, para reações químicas que sejam o inverso uma da outra.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
O etilenoglicol (HOCH2CH2OH) é um álcool muito utilizado como principal soluto nos
líquidos de arrefecimento de automóveis, sendo misturado com a água para elevar o ponto de ebulição
nos dias mais quentes ou dificultar seu congelamento nos dias mais frios. Determine os valores de
fração molar, molalidade e porcentagem em massa do etilenoglicol, respectivamente, ao adicionar
0,8 kg de etilenoglicol em 3,5 kg de água no radiador de um carro.
Provas
Questão presente nas seguintes provas
Os carboidratos são os compostos orgânicos mais abundantes no mundo vegetal,
apresentando inúmeras funções. Em relação aos carboidratos, analise as assertivas abaixo e assinale
V, se verdadeiras, ou F, se falsas.
( ) Os monossacarídeos que contêm um grupo aldeído são classificados como aldoses, enquanto aqueles que apresentam um grupo cetona são classificados como cetoses.
( ) Sacarose e lactose são exemplos de monossacarídeos.
( ) Três polissacarídeos importantes, todos constituídos de unidades de glicose, são o amido, o glicogênio e a maltose.
( ) A celulose é um dissacarídeo amplamente distribuído nas estruturas de sustentação das plantas.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
( ) Os monossacarídeos que contêm um grupo aldeído são classificados como aldoses, enquanto aqueles que apresentam um grupo cetona são classificados como cetoses.
( ) Sacarose e lactose são exemplos de monossacarídeos.
( ) Três polissacarídeos importantes, todos constituídos de unidades de glicose, são o amido, o glicogênio e a maltose.
( ) A celulose é um dissacarídeo amplamente distribuído nas estruturas de sustentação das plantas.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container