Foram encontradas 50 questões.
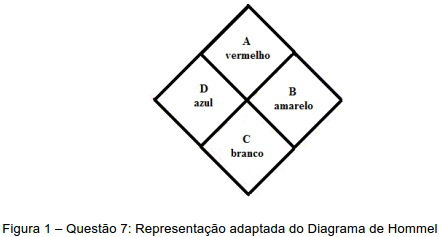
As letras A, B, C, e D presentes na representação do diagrama de Hommel (figura 1) estão associadas aos seguintes riscos, respectivamente:
Provas
Questão presente nas seguintes provas
Um programa de gerenciamento de resíduos deve contemplar dois tipos de resíduos: o ativo (gerado continuamente fruto das atividades rotineiras dentro da unidade geradora), e o passivo, que compreende todo aquele resíduo estocado. Em uma determinada Instituição de Ensino foram analisadas três diferentes amostras de resíduos sem identificação. A tabela abaixo apresenta os resultados encontrados em cada um dos testes:
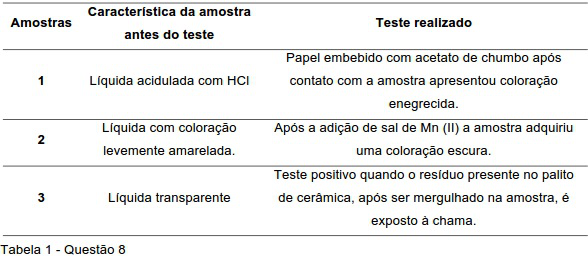
Com bases nos resultados dos testes, as amostras podem ser caracterizadas como:

Com bases nos resultados dos testes, as amostras podem ser caracterizadas como:
Provas
Questão presente nas seguintes provas
A análise coulométrica é uma aplicação da primeira lei de Faraday que pode ser expressa da seguinte forma: a extensão da reação química num eletrodo é diretamente proporcional à quantidade de eletricidade que passa através do eletrodo. Numa célula eletroquímica apropriada foi realizada a seguinte reação:
I3- + 2e- ⇌ 3 I -
Considerando as informações fornecidas acima, qual a quantidade de matéria de I3 - consumida após a passagem de 0,193 A durante 500 s ?
Dado: Constante de Faraday = 96500 C mol -1
I3- + 2e- ⇌ 3 I -
Considerando as informações fornecidas acima, qual a quantidade de matéria de I3 - consumida após a passagem de 0,193 A durante 500 s ?
Dado: Constante de Faraday = 96500 C mol -1
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A figura 1 apresenta a variação da pressão de vapor de quatro diferentes substâncias puras.
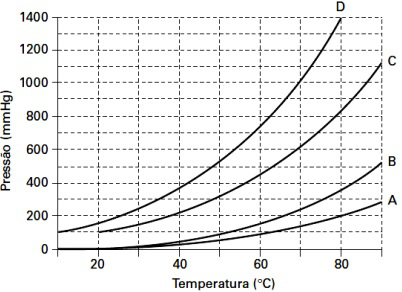
Figura 1 – Questão 11: Variação da pressão de vapor em função da temperatura para quatro diferentes substâncias puras.
Substância Massa Molar g mol-1 CHCl3 (Clorofórmio) 119,5
H2O (água) 18 CH3CH2OH (etanol) 46 CH2(OH)COOH (ácido glicólico) 76
As curvas apresentadas no gráfico foram obtidas em experimentos utilizando as substâncias listadas na Tabela 1. Identifique a alternativa que associa corretamente as curvas do gráfico às suas respectivas substâncias.
As curvas apresentadas no gráfico foram obtidas em experimentos utilizando as substâncias listadas na Tabela 1. Identifique a alternativa que associa corretamente as curvas do gráfico às suas respectivas substâncias.

Figura 1 – Questão 11: Variação da pressão de vapor em função da temperatura para quatro diferentes substâncias puras.
Substância Massa Molar g mol-1 CHCl3 (Clorofórmio) 119,5
H2O (água) 18 CH3CH2OH (etanol) 46 CH2(OH)COOH (ácido glicólico) 76
As curvas apresentadas no gráfico foram obtidas em experimentos utilizando as substâncias listadas na Tabela 1. Identifique a alternativa que associa corretamente as curvas do gráfico às suas respectivas substâncias.
As curvas apresentadas no gráfico foram obtidas em experimentos utilizando as substâncias listadas na Tabela 1. Identifique a alternativa que associa corretamente as curvas do gráfico às suas respectivas substâncias.
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosTransformações: Estados Físicos e Fenômenos
- Transformações Químicas e EnergiaTermoquímica
A figura 1 apresenta a curva de aquecimento da água pura. Nela são mostradas as quantidades de energia fornecida para a ocorrência das mudanças de fases.
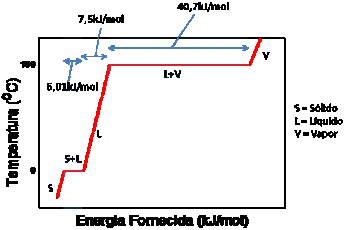
Figura 1 – Questão 12: Curva de aquecimento da água pura. (Adaptado). Fonte: Atkins, P. Jones, L. Chemistry, Molecules, Matter and Change. 4th ed. W. H. Freeman and Company. New York, 1999.
O mínimo de energia necessário para passar 1g de água do estado sólido para o estado vapor é: Dados: H= 1 g mol -1; O = 16 g mol -1

Figura 1 – Questão 12: Curva de aquecimento da água pura. (Adaptado). Fonte: Atkins, P. Jones, L. Chemistry, Molecules, Matter and Change. 4th ed. W. H. Freeman and Company. New York, 1999.
O mínimo de energia necessário para passar 1g de água do estado sólido para o estado vapor é: Dados: H= 1 g mol -1; O = 16 g mol -1
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um estudante necessita produzir gás hidrogênio a partir de raspas de zinco metálico. Há na bancada do laboratório dois reagentes líquidos concentrados:
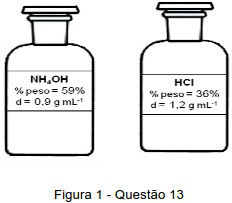
De acordo com as previsões do estudante, para produzir a quantidade de gás hidrogênio desejada ele deverá utilizar 500 mL de uma solução 6 mol L-1 preparada a partir de um dos reagentes acima. Indique a alternativa onde são apresentados, respectivamente, a identidade e o volume do reagente concentrado que o estudante deverá utilizar.
Dados: H = 1 g mol -1 ; N = 14 g mol -1 ; O = 16 g mol -1 ; Cl = 35,5 g mol -1 ; Zn = 65,4 g mol -1 .

De acordo com as previsões do estudante, para produzir a quantidade de gás hidrogênio desejada ele deverá utilizar 500 mL de uma solução 6 mol L-1 preparada a partir de um dos reagentes acima. Indique a alternativa onde são apresentados, respectivamente, a identidade e o volume do reagente concentrado que o estudante deverá utilizar.
Dados: H = 1 g mol -1 ; N = 14 g mol -1 ; O = 16 g mol -1 ; Cl = 35,5 g mol -1 ; Zn = 65,4 g mol -1 .
Provas
Questão presente nas seguintes provas
Num calorímetro misturam-se 50,0 g de uma solução HNO3 1mol.L-1 com 55,0 g de uma solução de KOH 1 mol .L-1 . A temperatura inicial de ambas as soluções era de 18º C. Após a reação de neutralização a temperatura medida foi 23o C. O calorímetro utilizado no experimento foi calibrado utilizando 60,0 g de água quente, a 57o C, adicionados a 60,0 g de água fria, a 12o C , que estavam presentes em um béquer dentro do calorímetro. Após a mistura mediu-se a temperatura e o valor encontrado foi de 32º C. Qual a entalpia da reação de neutralização em questão?
Dados:
Capacidade calorífica da água: 1 cal.g-1 . o C-1 .
Capacidade calorífica da solução neutralizada:1 cal.g-1 . o C-1 .
Densidade da água e de todas as soluções envolvidas: 1g.mL-1 .
Dados:
Capacidade calorífica da água: 1 cal.g-1 . o C-1 .
Capacidade calorífica da solução neutralizada:1 cal.g-1 . o C-1 .
Densidade da água e de todas as soluções envolvidas: 1g.mL-1 .
Provas
Questão presente nas seguintes provas
C
(grafite) + O2(g) → CO2(g) ∆H = -394 kJ mol-1 S
(rômbico) + O2(g) → SO2(g) ∆H = -297 kJ mol-1 CS
2(l) + 3 O2(g) → 2 SO2(g) + CO2(g) ∆H = - 1077kJ mol-1
A entalpia de formação do CS 2(l) a partir de seus elementos formadores tem ΔH = _____________ sendo, portanto uma reação _______________. Assinale a alternativa que contém os complementos corretos para a frase acima, respectivamente.
A entalpia de formação do CS 2(l) a partir de seus elementos formadores tem ΔH = _____________ sendo, portanto uma reação _______________. Assinale a alternativa que contém os complementos corretos para a frase acima, respectivamente.
Provas
Questão presente nas seguintes provas
A decomposição do N2O5 é uma reação de primeira ordem.
N2O5 (g) → 2 NO2(g) + 1/2 O2(g)
A constante de velocidade desta reação é igual a 1,38 x 10-5 s-1 a uma dada temperatura. Se a concentração inicial do N2O5 for 4,0 x 10-3 mol L-1,em quanto tempo aproximadamente a concentração cai até 1,0 x 10-3 mol L-1 ?
Dados: ln 2,5 = 0,916; ln 10-1 = -2,302
N2O5 (g) → 2 NO2(g) + 1/2 O2(g)
A constante de velocidade desta reação é igual a 1,38 x 10-5 s-1 a uma dada temperatura. Se a concentração inicial do N2O5 for 4,0 x 10-3 mol L-1,em quanto tempo aproximadamente a concentração cai até 1,0 x 10-3 mol L-1 ?
Dados: ln 2,5 = 0,916; ln 10-1 = -2,302
Provas
Questão presente nas seguintes provas
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O etilenoglicol CH2(OH)CH2(OH) é uma substância bastante utilizada como anticongelante. Pergunta-se: qual o volume mínimo de etilenoglicol que deve ser adicionado a 6,5L de água presentes no radiador de um carro, para prevenir o congelamento da água, num dia de inverno em que a temperatura atinge -20º C?
Dados: Densidade do etilenoglicol: 1,1 g cm-3 .
Densidade da água: 1,0 g cm-3
Kf = 1,9 K mol -1 Kg
H = 1 g mol -1 ; O = 16 g mol -1 ; C = 12 g mol -1
Dados: Densidade do etilenoglicol: 1,1 g cm-3 .
Densidade da água: 1,0 g cm-3
Kf = 1,9 K mol -1 Kg
H = 1 g mol -1 ; O = 16 g mol -1 ; C = 12 g mol -1
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container