Foram encontradas 50 questões.
Fósforo branco, que possui fórmula molecular P4, queima na presença do ar atmosférico para dar o composto A, no qual a porcentagem em massa de oxigênio é de 56,4%. O espectro de massa fornece a massa de A igual a 284 g mol -1 . Assinale a alternativa que contém a correta fórmula molecular de A. Dados: P = 31 g mol -1 ; O = 16 g mol -1 .
Provas
Questão presente nas seguintes provas
O tálio é um metal macio e maleável; quando imediatamente cortado por uma espátula, apresenta brilho metálico característico dos metais. O tálio, massa atômica 204,4 u, apresenta como isótopos mais estáveis o Tl-203 e o Tl-205. O isótopo Tl-205 apresenta abundância isotópica, em percentual inteiro, mais próximo de
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- FundamentosTransformações: Estados Físicos e Fenômenos
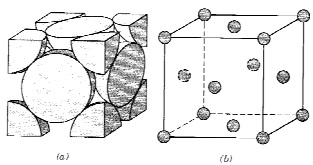
O níquel metálico cristaliza numa estrutura do tipo cúbica de faces centradas (cfc). Na figura são mostradas duas representações para célula unitária cfc: (a) utilizando esferas rígidas e (b) utilizando esferas reduzidas.
 Fonte: CALLISTER, W.D. Ciência de Engenharia de Materiais: uma Introdução, 5ª edição, Rio de Janeiro: LTC,
Fonte: CALLISTER, W.D. Ciência de Engenharia de Materiais: uma Introdução, 5ª edição, Rio de Janeiro: LTC,
O número de coordenação do níquel e o número de átomos de níquel por célula unitária são, respectivamente,
 Fonte: CALLISTER, W.D. Ciência de Engenharia de Materiais: uma Introdução, 5ª edição, Rio de Janeiro: LTC,
Fonte: CALLISTER, W.D. Ciência de Engenharia de Materiais: uma Introdução, 5ª edição, Rio de Janeiro: LTC, O número de coordenação do níquel e o número de átomos de níquel por célula unitária são, respectivamente,
Provas
Questão presente nas seguintes provas
O permanganato de potássio é bastante utilizado em titulações redox em análise química quantitativa, por se tratar de um forte reagente oxidante. Na equação, não balanceada, é representada a reação de uma das aplicações analíticas das titulações do permanganato.
MnO4 - + H2C2O4 + H+ → Mn2+ + CO2 + H2O
Após o correto balanceamento da reação redox descrita, a soma dos coeficientes estequiométricos na equação será igual a
MnO4 - + H2C2O4 + H+ → Mn2+ + CO2 + H2O
Após o correto balanceamento da reação redox descrita, a soma dos coeficientes estequiométricos na equação será igual a
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química InorgânicaSoluções e Substâncias Inorgânicas
Considere os íons indicados na tabela.
íons identificação nitrito I nitrato II sulfito III sulfato IV
O íon em que o átomo central apresenta conjunto de orbitais híbridos sp2 e o íon que apresenta geometria pirâmide trigonal são identificados na tabela, respectivamente, com os números
íons identificação nitrito I nitrato II sulfito III sulfato IV
O íon em que o átomo central apresenta conjunto de orbitais híbridos sp2 e o íon que apresenta geometria pirâmide trigonal são identificados na tabela, respectivamente, com os números
Provas
Questão presente nas seguintes provas
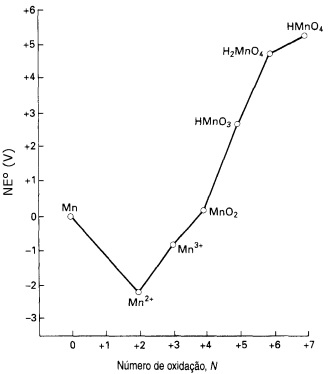
Considere o diagrama de Frost para o manganês em solução ácida com pH = 0.
Fonte: SHRIVER, D. F.; ATKINS, P.W, C.H. Química Inorgânica, 3ª edição, Porto Alegre:
A partir da análise do diagrama, pode-se afirmar que a espécie de manganês que se apresenta com o estado de oxidação mais estável em meio ácido, e uma das espécies de manganês que sofre desproporcionamento espontaneamente são, respectivamente,

Fonte: SHRIVER, D. F.; ATKINS, P.W, C.H. Química Inorgânica, 3ª edição, Porto Alegre:
A partir da análise do diagrama, pode-se afirmar que a espécie de manganês que se apresenta com o estado de oxidação mais estável em meio ácido, e uma das espécies de manganês que sofre desproporcionamento espontaneamente são, respectivamente,
Provas
Questão presente nas seguintes provas
No efeito fotoelétrico, quando um feixe de luz atinge uma superfície metálica provoca a emissão de elétrons. Para cada metal há uma frequência mínima da luz abaixo da qual não ocorre emissão de elétrons. Para explicar o efeito fotoelétrico _____________ admitiu que a energia radiante que atingia a superfície metálica era constituída por minúsculos pacotes de energia, chamados atualmente de fótons. No texto a lacuna pode ser corretamente substituída por:
Provas
Questão presente nas seguintes provas
Para abordar o tema equilíbrio químico, um professor nas aulas de química analítica apresentou dois sistemas em equilíbrio químico para discussão do princípio de Le Châtelier. O sistema A, em solução aquosa, refere-se ao equilíbrio dos íons dicromato (laranja) e cromato (amarelo). O sistema B, em fase gasosa, envolve os gases NO2 (castanho) e N2O4 (incolor).
sistema A: Cr2O7 2- (aq) + H2O (l) ⇄2 CrO42-(aq) + 2 H+ (aq)
sistema B: 2 NO2 (g) ⇄ N2O4 (g) ΔHº = -58 kJ
Cada sistema em equilíbrio foi submetido, separadamente, a duas perturbações, descritas a seguir:
I – Foram adicionadas gotas de solução de NaOH no sistema A.
II – Foram adicionadas gotas de solução de HCl no sistema A.
III – Foi aumentada a pressão do sistema B por meio de redução de volume.
IV – O sistema B foi aquecido.
Pode-se afirmar que as cores predominantes dos sistemas A e B após as perturbações I, II, III e V, foram, respectivamente,
sistema A: Cr2O7 2- (aq) + H2O (l) ⇄2 CrO42-(aq) + 2 H+ (aq)
sistema B: 2 NO2 (g) ⇄ N2O4 (g) ΔHº = -58 kJ
Cada sistema em equilíbrio foi submetido, separadamente, a duas perturbações, descritas a seguir:
I – Foram adicionadas gotas de solução de NaOH no sistema A.
II – Foram adicionadas gotas de solução de HCl no sistema A.
III – Foi aumentada a pressão do sistema B por meio de redução de volume.
IV – O sistema B foi aquecido.
Pode-se afirmar que as cores predominantes dos sistemas A e B após as perturbações I, II, III e V, foram, respectivamente,
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Na análise gravimétrica, diversas etapas sucessivas, ou operações unitárias, são empregadas durante a análise, tais como preparo da solução, precipitação, digestão, filtração, lavagem, calcinação e pesagem. Na etapa de preparo de soluções, para abertura de três diferentes amostras: calcário, paládio e materiais silicosos, recomenda-se o uso, respectivamente, de
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
A análise volumétrica é muito utilizada nos laboratórios químicos, especialmente na padronização de soluções. Na figura é representada uma curva de titulação.
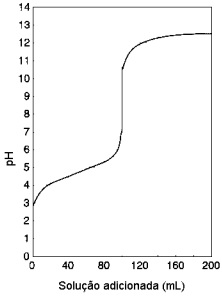
Considerando as soluções 0,1 mol/L de ácido acético, de ácido clorídrico, de hidróxido de sódio e de amônia, pode-se afirmar que a curva refere-se à adição da solução de

Considerando as soluções 0,1 mol/L de ácido acético, de ácido clorídrico, de hidróxido de sódio e de amônia, pode-se afirmar que a curva refere-se à adição da solução de
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container