Foram encontradas 80 questões.
Grandezas adimensionais são amplamente utilizadas em Engenharia Química, tais como as indicadas a seguir:
!$ X = { \large DG \over \mu} !$ !$ Y = { \large V^2 \over 2g} !$ !$ Z = { \large \tau \over ρV^2 / 2} !$
Considere:
D= diâmetro; G= vazão mássica; !$ \mu !$ = viscosidade dinâmica; V = velocidade;
g= aceleração da gravidade; !$ \tau !$ = tensão de cisalhamento e !$ \rho !$ = massa específica.
Exemplifica(m) este tipo de grandeza(s), a(s) expressão(ões):
Provas
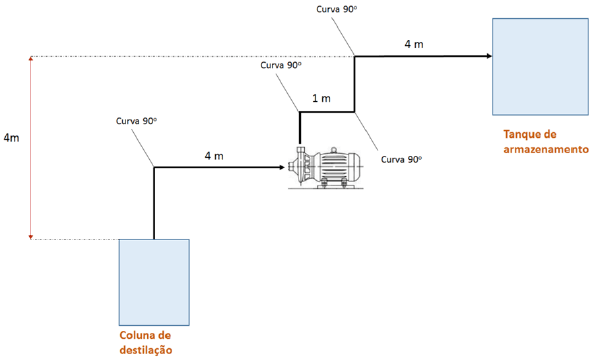
Etanol deve ser bombeado de uma coluna de destilação a um tanque de armazenamento a uma vazão constante, conforme figura abaixo. O setor de engenharia estipulou que o fluido deixa a coluna de destilação a uma pressão de 0,8 atm e alcança o tanque de armazenamento, cuja pressão interna é de 1,2 atm. Considerando que os diâmetros das tubulações de sucção e recalque sejam os mesmos, que o atrito propagado pela rugosidade da tubulação é de 0,03m/mtubulação, e que cada curva de 90º acrescenta propagação de atrito referente a 0,4m/curva, podemos dizer que a altura manométrica da bomba a ser projetada é aproximadamente:
DADOS: !$ ρ_{etanol} = 850 kg/m^3; !$ g = 10 m/s2; 1 atm = 10000 kg. m/s2
Provas
Deseja-se bombear água a 40°C, a uma vazão de 100 kg/min, de um tanque de armazenagem (1) para um segundo tanque (2), localizado 25 m acima do primeiro, a 25°C. Qual deve ser a potência da bomba utilizada nesse transporte de água, se transferência entre os tanques ocorre uma perda de calor de 200 kJ.s-1?
DADOS: !$ H (H_2O, \ell) = 104,89 \ kJ.kg^{-1} (25ºC); !$ !$ H (H_2O, \ell) = 167,50 \ kJ.kg^{-1} (40ºC) !$
Provas
No processo de fermentação para obtenção de etanol, o caldo utilizado como mosto deve estar à temperatura de 37ºC para que a produção ocorra de forma otimizada. No entanto, caldo provém da fábrica de açúcar a 32ºC. Para que haja este incremento de temperatura, um trocador de calor foi utilizado para aquecimento do fluido. No trocador, utilizou-se vazão de 5 L/s de água a 48ºC, que foi resfriada até 40ºC. Se o coeficiente global de transferência de energia para este caso é 300 W/m2K e se o sistema é perfeitamente isolado, ou seja, todo o calor perdido pela água é transferido ao caldo, podemos dizer que a área de transferência de energia do trocador de calor adaptado a esta situação é aproximadamente:
DADOS: Cp, água (20ºC a 100ºC) = 4,2 J/g.ºC; !$ ρ_{água} = 1000 kg/m^3 !$; ln (2) = 0,69; ln (1,37) = 0,31
Provas
Calcule a quantidade de calor necessária para aquecer de 300ºC até 1000ºC um volume de 3 m3 de um gás (nas CNTP) com a seguinte composição volumétrica: 20% CH4; 35% C2H6, 40% N2 e 5% H2O. Na tabela abaixo estão os valores das capacidades caloríficas molares médias em cal/molºC.
| 300ºC | 1000ºC | |
| CH4 | 10,20 | 14,27 |
| C2H6 | 13,73 | 19,24 |
| N2 | 7,04 | 7,50 |
| H2O | 8,23 | 9,20 |
Assinale a alternativa correta:
Provas
A queima metano em presença de oxigênio, forma dióxido de carbono e água. Em um reator a alimentação (150 mol.h-1) é formada por 20% de CH4, 60% de O2 e 20% de CO2 em base molar. Para uma conversão do reagente limitante de 90%, a composição, em base molar, do produto formado é:
Provas
A produção de butano, produto componente do GLP, pode ser realizada pela reação entre o propeno e o metano a 510 K e 175 atm.
Qual a quantidade de metano (kg.h-1) que deve ser alimentado ao reator para processar 5 ton.h-1 de propeno?
Considere a conversão da reação é completa e os reagentes são alimentados em sua composição estequiométrica.
DADOS: MMMETANO= 16 g/mol; MMPROPENO= 42 g/mol; MMBUTANO= 58 g/mol
Provas
Hidrociclones podem ser usados na classificação de sólidos a partir de uma suspensão. Para aperfeiçoar a eficiência dessas separações, são usados hidrociclones em série, conforme mostrado na figura abaixo.
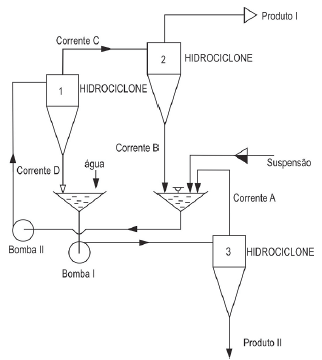
No processo apresentado, quanto ao diâmetro médio das partículas é correto afirmar:
Provas
Em um processo industrial, uma solução aquosa de ácido sulfúrico na concentração de 2,0 mol.L-1 entra em um reator com vazão de 1,00 m3.min-1. Sabendo-se que a densidade relativa do H2SO4 é igual a 1,03, a vazão mássica de H2SO4, em kg.s-1, é aproximadamente igual a:
Provas
O comportamento de um gás em condições de não idealidade pode ser descrito pela equação de van der Waals na qual ‘p’ é a pressão, ‘R’ é a constante universal dos gases ideais, ‘T’ é a temperatura, em graus Kelvin, ‘V’ é o volume molar e ‘a’ e ‘b’ definem os coeficientes de van der Waals.
!$ p = { \large R.T \over \overline V - b} - { \large a \over \overline V^2} !$
Assinale a alternativa correta com relação à equação de van der Waals:
Provas
Caderno Container