Foram encontradas 50 questões.
Uma solução de ácido HX de concentração 0,01mol/L foi colocada para a medição do seu potencial hidrogênio iônico. Sabendo que a constante de ionização do HX é 1,0 x 10-8 (0,00000001), o valor da medida será próximo de:
Provas
Os métodos instrumentais de análise são ferramentas importantes nas determinações qualitativas, quantitativas e estruturais da matéria. Verifique as análises descritas abaixo:
I. Uma amostra de um sólido orgânico de alta pureza a ser analisado para identificar as possíveis funções orgânicas presentes em sua molécula.
II. Uma amostra de um composto orgânico analisada para contribuir na elucidação da estrutura da molécula a partir dos seus fragmentos que geram respostas de razão massa-carga.
III. Determinação da concentração de uma espécie conhecida, a partir da simples relação linear entre absorção da radiação eletromagnética e concentração.
IV. Injeção de uma amostra em uma chama, provocando a excitação eletrônica dos átomos, gerando um sinal analítico através da radiação UV-Vis gerada.
As situações descritas acima estão relacionadas, respectivamente, com as técnicas de:
Provas
Por definição, uma solução tampão resiste a variações no pH decorrentes da diluição ou da adição de ácidos ou bases. Os químicos empregam as soluções tampão para manter o pH de soluções sob níveis predeterminados relativamente constantes.
Um estudante misturou 200mL de solução de ácido HX de concentração 0,1mol/L com 300mL de solução do sal de sódio desse ácido (NaX) que tinha concentração de 0,2mol/L. Sabendo que a constante de ionização do ácido HX é 0,000003. Qual o valor do pH da solução formada?
Provas
Uma solução de permanganato de potássio foi colocada em uma cubeta de 2cm de comprimento óptico. Feita a leitura em um equipamento espectrofotômetro UV-Vis, observou-se a absorbância medida de 0,200. Sabendo que o coeficiente de absortividade molar era de 20L.mol-1.cm-1, admite-se que a concentração da solução é de:
Provas
Uma indústria de sanitizantes faz o preparo de álcool líquido 70% INPM (concentração em massa) através da adição de: etanol hidratado 96% (porcentagem em volume) água desnaturante (quantidade desprezível).
Em uma das bateladas de 1000 litros de produto, o analista de controle de qualidade identificou que a concentração alcoólica estava em 70% em volume.
O que o operador deve fazer, desconsiderando as possíveis contrações ou dilatações de volume, para que a indústria entregue um produto com concentração próxima e não inferior a 70% INPM (equivalente à 74,5% em volume)?
Dados de densidade: água= 1,0g/mL; etanol= 0,8g/mL.
Provas
Quimicamente, a cloroquina (CQ) e a hidroxicloroquina (HCQ) pertencem à classe das 4-aminoquinodinas. Elas têm estrutura central aromática comum, com um cloro na posição 7, ligada às respectivas cadeias laterais básicas. A forma molecular da cloroquina é: C18H26CIN3, com massa molar de 319,9 g/mol. Já a hidroxicloroquina tem massa molar de 335,9 g/mol
.
A CQ e a HCQ são administradas como difosfato e sulfato, respectivamente, em suas formas racêmicas.
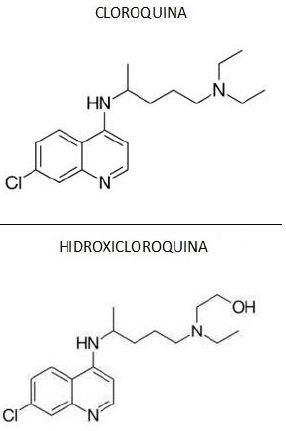
Sobre o medicamento citado acima, marque o que for correto.
Provas
Um mol de uma dada substância é aquecido de 80 °C para 110 °C, sem alterar o seu estado físico. Baseado nos seus conhecimentos de termodinâmica, analise as afirmativas abaixo:
I. A equação !$ \triangle H '= \int_{80}^{110} c_p dT !$ pode ser usada para calcular a variação da entalpia associado ao aquecimento de um mol da substância.
II. Se a substância for um líquido ou sólido, o processo de aquecimento terá praticamente o mesmo gasto energético a volume constante e a pressão constante.
III. Se a substância for um gás ideal, o processo de aquecimento a pressão constante gastará mais energia que o processo de aquecimento a volume constante.
Assinale a alternativa que contém a análise correta.
Provas
O dióxido de nitrogênio (NO2) é uma molécula intermediária na produção industrial de ácido nítrico (HNO3), que é muito aplicado na produção de fertilizantes.
O dióxido de nitrogênio existe em equilíbrio com o tetróxido de nitrogênio (N2O4), segundo a reação:
!$ 2 NO_2(g) \rightleftarrows N_2 O_4(g)\,\,\,\,\,\triangle = -57,23 KJ/mol !$
Para aumentar o rendimento do dióxido de nitrogênio na reação, segundo o princípio de Le Châtelier, deve-se:
Provas
“Na última semana, os consumidores sentiram pesar no bolso o preço do gás de cozinha. O valor médio do botijão de 13 kg subiu de R$ 85,27 para R$ 85,63 entre os dias 6 e 12 de junho. Considerando todo o país, o maior preço do produto foi registrado na região Centro-Oeste, onde consumidores chegaram a pagar R$ 125 por um botijão.”
(Disponível em: https://jovempan.com.br/noticias/
brasil/ gas-de-cozinha-atinge-maior-preco-em-2021-e-deve-ficar-ainda-mais-caro-entenda-o-reajuste-da-petrobras.html. Acessado em 28/09/2021)
Supondo que todo o GLP presente no botijão seja somente butano e está totalmente na forma líquida, e que o preço do botijão de gás seja de R$ 125,00, para uma família que teve um gasto mensal com a fatura de gás de R$ 55,77, qual a quantidade de energia que foi liberada, em quilojoules, na queima do gás butano?
A reação de combustão completa do butano (não balanceada):
C4H10(g)→CO2(g)+H2O !$ \triangle H_C^{ \circ} = 2.808 KJ/ mol !$
Provas
A amônia ou amoníaco é um composto químico que na temperatura ambiente é um gás incolor, tóxico e corrosivo quando há presença de umidade. Esse gás, além de altamente perigoso no caso de inalado, também é inflamável. Muito utilizado na refrigeração e em processos de absorção em combinação com a água, além de seu uso na agricultura e em produtos de limpeza.
A amônia, ao reagir com a água origina os íons amônio e hidroxila, segundo o seguinte equilíbrio químico:
!$ NH_3(g) + H_2O( \ell) \rightleftarrows NH_4^+ (aq) + OH^- (aq) !$
Com relação à amônia e a sua reação com água, analise os seguintes itens:
I. A geometria molecular da amônia é piramidal.
II. A amônia é dita como base de Bronsted-Lowry na reação com a água.
III. NH4+ é a base conjugada da amônia.
Assinale a alternativa que contém a análise correta.
Provas
Caderno Container