Foram encontradas 1.055 questões.
Os valores das constantes de ionização de muitos ácidos já foram determinados experimentalmente e encontram-se tabelados à mesma concentração e temperatura. Por meio dos valores tabelados, pode-se comparar a força desses ácidos. Analise a tabela a seguir e assinale a alternativa INCORRETA.
Acidez de alguns ácidos
ÁCIDOS | Constante de ionização (Ka) |
HCl | 10+7 |
H2SO4 | 10+3 |
H2SO3 | 1,5.10-2 |
H3PO4 | 7,6.10-3 |
HNO2 | 4,3.10-4 |
HF | 3,5.10-4 |
CH3COOH | 1,8.10-5 |
H2CO3 | 4,3.10-7 |
H2S | 1,3.10-7 |
HCN | 4,9.10-10 |
Fonte: Adaptado de ATKINS e JONES (2011).
Provas
Em relação a constante de equilíbrio, é correto afirmar:
Provas
Os ácidos são classificados de acordo com o número de hidrogênios ionizáveis. Sobre isso, assinale a alternativa INCORRETA.
Provas
Sobre ácidos e bases, analise as assertivas abaixo, assinalando V, se verdadeiras, ou F, se falsas.
( ) A dissolução do ácido sulfúrico concentrado em água libera uma grande quantidade de energia. Por esse motivo, em laboratório, para realizar a diluição do H2SO4, deve-se adicioná-lo à água e nunca adicionar água a ele.
( ) As bases são classificadas apenas pelo número de hidroxilas, ou seja, em função do número de grupos OH- liberados por fórmula, podendo ser denominadas ortobase e/ou metabase.
( ) O hidróxido de amônio é uma base, se dissolve facilmente em água e apresenta grau de ionização muito alto. Logo é uma base fraca.
( ) As bases Be(OH)2 e Mg(OH)2, por apresentarem solubilidade muito pequena, são consideradas praticamente insolúveis. Logo, apresentam baixo grau de dissociação, sendo consideradas bases fracas.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Provas
Um aluno tem uma solução X e fenolftaleína. Sendo assim, ele pinga algumas gotas de fenolftaleína em uma alíquota da solução X e percebe a mudança de cor, quase que imediatamente, para uma coloração rósea. Sobre isso, analise as assertivas abaixo:
I. A solução X deve ser um meio alcalino.
II. O soluto da solução X é um ácido forte.
III. A solução X tem características de um sal.
IV. A solução X pode ser preparada com H2SO4, conferindo um meio ácido à solução.
Quais estão corretas?
Provas
Analise os dados da tabela nutricional de uma determinada solução aquosa, conforme segue:
|
TABELA NUTRICIONAL |
|
|
Cada 100 mL contém: Calorias Carboidratos Proteínas Lipídeos Sódio Potássio Cloreto |
24 kcal 6,0 g 0,0 g 0,0 g 45,0 mg 12,0 mg 42,0 mg |
Fonte: Adaptado de Usberco e Salvador (2006).
Com base na informação acima, assinale a alternativa INCORRETA.
Provas
O , fórmula molecular , é um utilizado no tratamento de água. Ao ser adicionado à água em meio , forma flocos, que se juntam a impurezas sólidas presentes na água, constituindo estruturas maiores, que precipitam. O processo mencionado é denominado de .
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do trecho acima.
Provas
A reação de neutralização do hidróxido de sódio com ácido clorídrico é expressa pela equação:
HC !$ ℓ !$ + NaOH → NaC !$ ℓ !$ + H2O
Determine o volume de HC!$ ℓ !$, na concentração 0,05 mol∙L-1, necessário para neutralizar 10 mL de solução 0,1 mol∙L-1 de NaOH. Dados: C!$ ℓ !$ = 35,5 g∙mol-1; Na = 23 g∙mol-1; O = 16 g∙mol-1; H = 1 g∙mol-1.
Provas
O cloreto de bário, de fórmula química BaCl2, é uma substância muito utilizada no setor de metalurgia em sais de têmpera, com a finalidade de aumentar a dureza de ferro-ligas e/ou aços (tratamento térmico de metais). É utilizado também em indústrias de sais de bário e em indústrias para eliminação de sulfato. Determine a massa de cloreto de bário, em gramas, necessária para preparar 500 mL de solução de concentração 0,5 mol∙L-1. Dados: Massas moleculares: Ba = 137 g/mol e C!$ ℓ !$ = 35,5 g/mol.
Provas
O ácido acetilsalicílico ou AAS, conhecido popularmente como aspirina, nome de uma marca que se tornou de uso comum, é um fármaco da família dos salicilatos. Considerando a sua fórmula abaixo, assinale a alternativa correta.
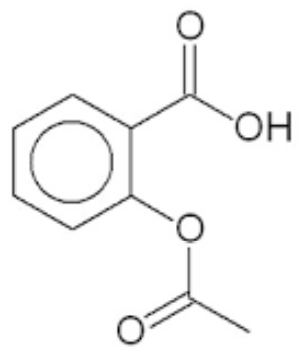
Ácido Acetilsalicílico
Provas
Caderno Container