Foram encontradas 80 questões.
Com respeito aos orbitais atômicos e à teoria da ligação de valência, assinale a alternativa INCORRETA.
Provas
Com relação às emissões radioativas observadas no planeta Terra, assinale a alternativa correta:
Provas
Os trabalhos de Joseph John Thomson e Ernest Rutherford resultaram em importantes contribuições na história da evolução dos modelos atômicos e no estudo de fenômenos relacionados à matéria. Das alternativas abaixo, aquela que apresenta corretamente o autor e uma de suas contribuições é:
Provas
O dispositivo a seguir utiliza a radiação solar para quantificar variações em propriedades termodinâmicas. Este dispositivo é composto por uma lente convergente e por um porta-amostras. A lente possui área útil de 80,0 cm2, absortividade (a) de 20% e transmissividade (t) de 80%. O porta-amostras possui absortividade de 100% e volume variável, operando à pressão constante de 1,0 atm.
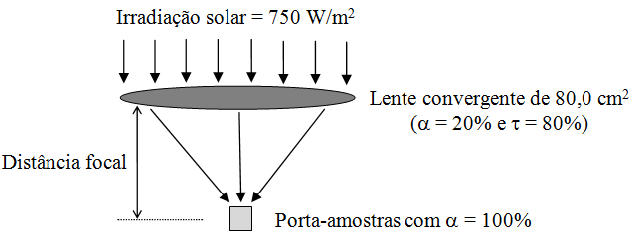
Em um procedimento experimental, injetou-se 0,100 mol de uma substância pura líquida no portaamostras do dispositivo. Em seguida, mediu-se um tempo de 15,0 min para a vaporização total da amostra, durante o qual a irradiação solar permaneceu constante e igual a 750 W/m2. Nesse processo, a temperatura do porta-amostras estabilizou-se em 351 K. No experimento, o calor sensível da amostra e a radiação emitida pelo porta-amostras são desprezíveis. Pode-se concluir que na vaporização total da substância, as variações de entalpia molar padrão e de entropia molar padrão são, respectivamente:
Provas
O gráfico abaixo ilustra as variações de energia devido a uma reação química conduzida nas mesmas condições iniciais de temperatura, pressão, volume de reator e quantidades de reagentes em dois sistemas diferentes. Estes sistemas diferem apenas pela presença de catalisador. Com base no gráfico, é possível afirmar que:
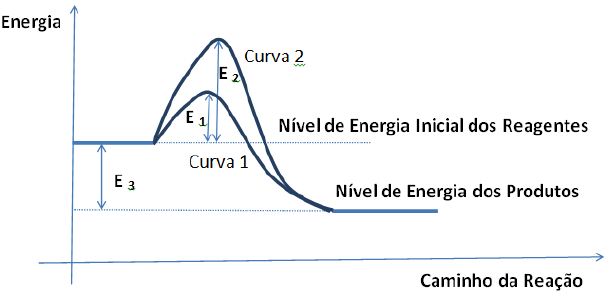
Provas
Um erlenmeyer contém 10,0 mL de uma solução de ácido clorídrico, juntamente com algumas gotas de uma solução de fenolftaleína. De uma bureta, foi-se gotejando uma solução 0,100 M de hidróxido de sódio até o aparecimento de leve coloração rósea. Nesse momento, observou-se um consumo de 20,0 mL da solução alcalina. Pode-se afirmar que a concentração de HCl na solução ácida original era de:
Dados:
Massas atômicas: H = 1,00 u, O = 16,0 u, Na = 23,0 u, Cl = 35,5 u
Provas
Um tambor selado contém ar seco e uma quantidade muito pequena de acetona líquida em equilíbrio dinâmico com a fase vapor. A pressão parcial da acetona é de 180,0 mm Hg e a pressão total no tambor é de 760,0 mm Hg.
Em uma queda durante seu transporte, o tambor foi danificado e seu volume interno diminuiu para 80% do volume inicial, sem que tenha havido vazamento. Considerando-se que a temperatura tenha se mantido estável a 20 oC, conclui-se que a pressão total após a queda é de:
Provas
Dentre as opções abaixo, escolha a que corresponde, respectivamente, às classes das moléculas: hemoglobina, amido, DNA, ácido palmítico.
Provas
Dados os íons: !$ _{16}S^{-2}; _{19}K^+; _{56}Ba^{2+} !$, indique qual das relações abaixo apresenta os íons isoeletrônicos em ordem correta de raio iônico.
Provas
Dadas as reações:
!$ PCl_3 + 3 H_2 O \rightarrow H_3 PO_3 + 3 HCl\\PCl_5 + 4 H_2 O \rightarrow H_3 PO_4 + 5HCl !$
Assinale a afirmativa correta:
Provas
Caderno Container