Foram encontradas 1.130 questões.
Provas
Questão presente nas seguintes provas

Provas
Questão presente nas seguintes provas

NH3 (g) + HCl (g) → NH4 Cl (s) ∆H0 = –176 kJ N2 (g) + 3H2 (g) → 2NH3 (g) ∆H0 = –92,2 kJ N2 (g) + 4H2 (g) + Cl2 (g) → 2NH4 Cl (s) ∆H0 = –628,9 kJ
Com base nas equações, é correto afirmar que a entalpia de reação de síntese do gás cloreto de hidrogênio é, em quilojoules, aproximadamente igual a:
Provas
Questão presente nas seguintes provas
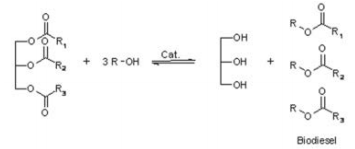 Sobre o processo químico de transesterificação, considere as afirmativas a seguir.
I. A reação de transesterificação do óleo é uma reação de um lipídeo com álcool para formar éster e um subproduto,
a glicerina.
II. Na produção do biodiesel, um dos processos mais usados é a catálise homogênea, em que o catalisador é um
ácido que melhora o rendimento da reação.
III. O álcool mais utilizado no processo de produção do biodiesel é um de cadeia longa que irá favorecer a solubilidade
da gordura na produção do biodiesel.
Estão corretas as afirmativas:
Sobre o processo químico de transesterificação, considere as afirmativas a seguir.
I. A reação de transesterificação do óleo é uma reação de um lipídeo com álcool para formar éster e um subproduto,
a glicerina.
II. Na produção do biodiesel, um dos processos mais usados é a catálise homogênea, em que o catalisador é um
ácido que melhora o rendimento da reação.
III. O álcool mais utilizado no processo de produção do biodiesel é um de cadeia longa que irá favorecer a solubilidade
da gordura na produção do biodiesel.
Estão corretas as afirmativas:Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
COLUNA I 1. Método de Volhard 2. Método de Mohr 3. Método de Fajans
COLUNA II ( )Método que detecta o ponto final por meio de um corante ácido fraco carregado negativamente. ( )Utilização de Fe3+ como indicador que formará um produto colorido.= ( )Forma-se um precipitado vermelho de Ag2 CrO4 . Assinale a sequência CORRETA.
Provas
Questão presente nas seguintes provas
Assinale a alternativa que apresenta o tipo de radiação
que completa a seguinte equação de desintegração
radioativa hipotética: 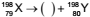 + energia
+ energia
Provas
Questão presente nas seguintes provas

Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais

Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
- Sistemas de EquilíbrioSistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores

Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais

Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container