Foram encontradas 50 questões.
Quando uma solução de hidróxido de sódio é adicionada a uma solução de sulfato férrico, forma-se um precipitado castanho de Fe(OH)3. À equação que melhor representa o processo citado é aquela que só representa os participantes essenciais da reação. Sendo assim, assinale a opção que apresenta essa equação.
Provas
Sabendo-se que as constantes de dissociação do gás sulfídrico, H2S, são K1=8,73 x 10-7 e K2=3,63 x 10-12, as concentrações molares de íons HS- e de S2- numa solução de 0,873M de gás sulfídrico são, respectivamente:
Provas
A dureza da água é um dado muito importante em diversas aplicações. As reações dos íons que geram a dureza na água com EDTA e o respectivo indicador são representados abaixo.

Em relação à dureza da água, assinale a opção INCORRETA.
Provas
Sobre a pilha de corrosão eletroquímica, que é constituída de elementos fundamentais, marque a opção correta.
Provas
Calcule a concentração resultante de [H+], em mol.L-1, ao se titular uma solução de 50mL de HCI 0,1 M com 25mL de NaOH 10-1 M e marque a opção correta.
Provas
Analise os complexos abaixo.
I- [Fe(CN)6]4-
II- [Fe(CN)6]3-
III- [Cu(NH3)4]2+
IV- [Cu(CN)4]3-
O número de coordenação em cada um dos complexos acima é, respectivamente:
Provas
Com relação aos instrumentos e técnicas usadas em laboratório, é correto afirmar que:
Provas
O éter etílico é um composto orgânico que foi muito usado no passado como anestésico. Um dos métodos usados para sua obtenção é a desidratação intermolecular do etanol, como mostrado na reação abaixo.
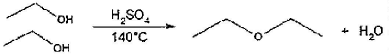
Um químico deseja utilizar o mesmo método descrito acima para sintetizar um éter assimétrico, o 2-etóxi-2- metilpropano. Nesse caso, os álcoois de partida devem ser
Provas
Um ácido fraco genérico HA, tem constante de acidez Ka = 5,6 x10-5. Sendo assim, calcule a porcentagem de moléculas desprotonadas em uma solução 0,00875 M desse ácido. Considere [HA]>>[A].
Provas
Um químico possui em seu laboratório uma substância de estrutura desconhecida, a qual ele chamou A. Essa substância reage com uma mistura de HNO3/H2SO4, gerando uma substância B. A substância B reage com uma mistura de Br2/Fe, resultando em uma substância C, a qual possui uma fórmula molecular determinada de C5H4O2NBr. Sabendo-se que o Índice de Deficiência de Hidrogênios (IDH) da substância C é igual a 5, o químico chegou à conclusão de que os compostos A, B e C são, respectivamente:
Provas
Caderno Container