Foram encontradas 800 questões.
Uma titulação redox se baseia em uma reação de oxirredução entre o analito e o titulante. Considere a titulação de 25,00 mL de uma solução de Fe2+ 0,2 mol/L com uma solução 0,2 mol/L de Ce4+ (titulante). Calcule o potencial do sistema para um volume de titulante de 25,00 mL e assinale a opção correta.
Dados: Equação de Nernst para redução da espécie genérica A (aA + ne-→ bB):
!$ E=E^º_{red}-{\large{0,059 \over n}} \log \left({\large{a^b_B \over a^a_A}}\right) !$
Onde: Eº red = potencial padrão de redução; n = número de elétrons da reação; e aI = atividade da espécie i (a atividade pode ser aproximada pela concentração da espécie caso ela esteja em solução ou pode ser considerada igual a 1 caso ela esteja no estado sólido).
Reação de titulação: Ce4+ + Fe2+ !$ \rightleftharpoons !$ Ce3+ + Fe3+
Semi-reações: Ce4+ + e- !$ \rightleftharpoons !$ Ce3+ E0=+1,44V
Fe3+ + e- !$ \rightleftharpoons !$ Fe2+ E0=+ 0,77V
Provas
Analise a estrutura da fexofenadina abaixo:
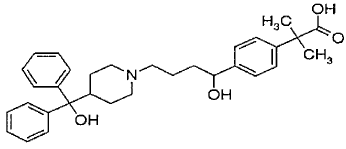
Com base na estrutura apresentada acima, analise as afirmativas a seguir e assinale a opção correta.
I- A molécula possui 32 carbonos em sua estrutura.
II- Há dois carbonos quirais.
III- O Nitrogênio da cadeia fechada funciona como uma base de Lewis.
IV- É possível identificar as funções orgânicas: cetona, álcool e amina.
Provas
Na análise gravimétrica, a massa de um determinado produto é usada para calcular a quantidade do analito presente na amostra original. Um dos métodos gravimétricos de análise consiste na precipitação química. Na análise gravimétrica do Mg2+, ele é precipitado como fosfato de amônio e magnésio Mg(NH4)PO4 • 6H2O, o qual em seguida é calcinado, transformando-se em Mg2P2O7. Sabendo-se que a massa de precipitado obtida após a calcinação é de 122,43g, calcule a massa, em gramas, de Mg2+ presente na amostra original e assinale a opção correta.
Dados: massas molares
MMg = 24,3 g/mol;
MP = 31 g/mol; e
Mo= 16 g/mol.
Provas
Assinale a opção que apresenta a molécula orgânica classificada como álcool.
Provas
Assinale a opção que apresenta a ordem crescente de ponto de ebulição à pressão atmosférica para os seguintes hidrocarbonetos:
I- propano
II- propeno
III- pentano
IV- 2,2-dimetilpropano
Provas
Observe a reação orgânica abaixo e assinale a opção que apresenta o mecanismo de reação envolvido.
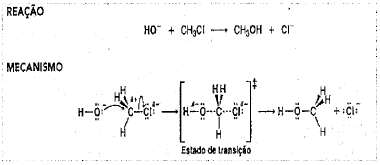
Provas
O petróleo é uma mistura complexa de compostos orgânicos, principalmente hidrocarbonetos. Uma das principais frações obtidas em seu refino é a gasolina, que pode ser obtida por outros processos além da destilação do petróleo, como a combinação de moléculas pequenas para formar moléculas maiores. Nesse contexto, a síntese de octano a partir de uma mistura de butano e buteno é uma reação característica do processo de:
Provas
Sobre os erros experimentais, assinale a opção correta.
Provas
Dadas as semirreações de redução abaixo e seus respectivos potenciais-padrão:
!$ ^1/_2 !$ Hg2CI2(g) + e- !$ \rightleftharpoons !$ Hg(I) +CI- Eº=+0,268 V
AgCI(s) + e- !$ \rightleftharpoons !$ Ag(s) + CI- Eº=+0,222 V
Com base nas informações acima, analise as afirmativas a seguir e assinale a opção correta.
I- A primeira reação é a redução do calomelano.
II- Uma célula galvânica com um eletrodo padrão de hidrogênio e um eletrodo de calomelano saturado terá uma diferença de potencial de +0,268 V.
III- O eletrodo de cloreto de prata não pode ser usado com um eletrodo padrão de hidrogênio.
IV- O eletrodo de cloreto de prata com KCI saturado possui potencial igual a +0,222 V.
Provas
Calcule a entalpia padrão de formação do etanol a 25ºC a partir de sua entalpia padrão de combustão e assinale a opção correta.
Dados:
C2H5OH(I) + 3O2(g) → 2CO2(g) + 3H2O(I) !$ \Delta !$Hº=-1.368 kJ.mol-1
Entalpia padrão de formação do CO2(g)=-393,5 kJ.mol-1
e
Entalpia padrão de formação da H2O(I)=-285,8 kJ.mol-1
Provas
Caderno Container