Foram encontradas 150 questões.
A figura a seguir apresenta o diagrama de fases de uma substância. Nesse diagrama, o ponto triplo e o ponto crítico correspondem, respectivamente, às coordenadas (216,8 K, 5,11 atm) e (340,2 K, 72,9 atm).
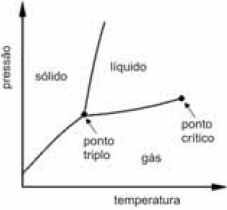
As curvas que representam os pontos de equilíbrio entre as fases podem ser descritas pela equação de Clapeyron, \({dp \over dT} = { \Delta H_{tr} \over T. \Delta V_{tr}},\) em que \(p\), \(T\), \(\Delta H_{tr}\) e \(\Delta V_{tr}\) representam a pressão, a temperatura e as variações de entalpia e de volume durante a transição de fase, respectivamente.
à temperatura de 280 K, a pressão de vapor dessa substância é maior que 72,9 atm.
Provas
A figura a seguir apresenta o diagrama de fases de uma substância. Nesse diagrama, o ponto triplo e o ponto crítico correspondem, respectivamente, às coordenadas (216,8 K, 5,11 atm) e (340,2 K, 72,9 atm).

As curvas que representam os pontos de equilíbrio entre as fases podem ser descritas pela equação de Clapeyron, \({dp \over dT} = { \Delta H_{tr} \over T. \Delta V_{tr}},\) em que \(p\), \(T\), \(\Delta H_{tr}\) e \(\Delta V_{tr}\) representam a pressão, a temperatura e as variações de entalpia e de volume durante a transição de fase, respectivamente.
A partir do diagrama apresentado e com base na equação de Clapeyron, é correto inferir que
à pressão de 1 atm, a referida substância pode sofrer sublimação.
Provas
A figura a seguir apresenta o diagrama de fases de uma substância. Nesse diagrama, o ponto triplo e o ponto crítico correspondem, respectivamente, às coordenadas (216,8 K, 5,11 atm) e (340,2 K, 72,9 atm).

As curvas que representam os pontos de equilíbrio entre as fases podem ser descritas pela equação de Clapeyron, \({dp \over dT} = { \Delta H_{tr} \over T. \Delta V_{tr}},\) em que \(p\), \(T\), \(\Delta H_{tr}\) e \(\Delta V_{tr}\) representam a pressão, a temperatura e as variações de entalpia e de volume durante a transição de fase, respectivamente.
A partir do diagrama apresentado e com base na equação de Clapeyron, é correto inferir que
na temperatura de fusão, a fase sólida da substância em apreço apresenta densidade maior que a do respectivo estado líquido.
Provas
\(2\,\quad\,BrC\,\ell_{\,(\mathrm\,{g})}\)![]() \(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
\(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
Com
base nessa informação e considerando que os logaritmos naturais de 5 e 2
sejam iguais a 1,609 e 0,693, respectivamente, julgue o item seguinte.
Na temperatura T, a energia livre padrão da reação apresentada é negativa, e o valor de seu módulo é superior a 5RT.
Provas
\(2\,\quad\,BrC\,\ell_{\,(\mathrm\,{g})}\)![]() \(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
\(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
Com
base nessa informação e considerando que os logaritmos naturais de 5 e 2
sejam iguais a 1,609 e 0,693, respectivamente, julgue o item seguinte.
Se 10,0 mol de \(BrC\,\ell_{\,\mathrm\,(g)}\) forem colocados em uma câmara inicialmente evacuada, quando o equilíbrio químico for atingido, à temperatura T, a quantidade de matéria de \(Br_2\) será inferior a 6,0 mol.
Provas
\(2\,\quad\,BrC\,\ell_{\,(\mathrm\,{g})}\)![]() \(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
\(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
Com
base nessa informação e considerando que os logaritmos naturais de 5 e 2
sejam iguais a 1,609 e 0,693, respectivamente, julgue o item seguinte.
Considerando que a reação seja endotérmica em toda a faixa compreendida entre as temperaturas T e T' e que T' seja maior que T, é correto concluir que a constante de equilíbrio da reação na temperatura T' é superior a 400.
Provas
\(2\,\quad\,BrC\,\ell_{\,(\mathrm\,{g})}\) ![]() \(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
\(Br_{2\,\mathrm\,{(g)}}\,+\,C\,\ell_{2\,\mathrm\,{(g)}}\)
Com base nessa informação e considerando que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue o item seguinte.
Para a reação em questão, o volume da câmara não influencia a velocidade com que o equilíbrio é atingido.
Provas
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.
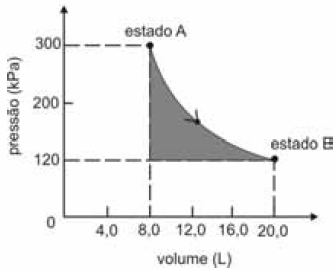
Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 J.mol-1.K-1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue o item a seguir.
A área sombreada do gráfico corresponde ao trabalho realizado pelo gás durante a referida expansão.
Provas
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.

Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 J.mol-1.K-1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue o item a seguir.
A temperatura do gás é maior que 300 K.
Provas
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.

Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 J.mol-1.K-1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue o item a seguir.
Considere que, após a referida transformação, o sistema tenha retornado ao estado A. Nessa situação, qualquer que seja o caminho de retorno, o calor trocado com as vizinhanças e o trabalho realizado pelo sistema durante o ciclo (estado A \(\rightarrow\) estado B \(\rightarrow\) estado A) são ambos iguais a zero, pois calor e trabalho são funções de estado termodinâmicas.
Provas
Caderno Container