Foram encontradas 503 questões.
Um exame químico analisando a tinta de determinado objeto levou à formação do íon diclorotetraminocobalto(III). Sobre esse íon complexo é correto afirmar que:
Provas
Uma substância gasosa, inflamável e tóxica foi identificada em um armazém de estocagem de feijão. Resultante da combinação dos elementos X (Z = 1) e Y (Z = 15), esse composto possui geometria:
Provas
Em uma sátira da indústria cinematografia, disfarçado de dentista, um personagem usa gás hilariante e arranca um dente (errado) de seu arquiinimigo. Agindo sobre o sistema nervoso central, o gás hilariante (N2O) tem características anestésicas e faz com que as pessoas riam, até de forma histérica. Esse óxido pode ser obtido, juntamente com vapor d'água, a partir da decomposição térmica do nitrato de amônio.
Qual a variação de entalpia, em Kcal, para a reação de decomposição do NH4NO3?
Dados: ∆Hf o N2O (g) = + 19,5 Kcal/mol, ∆Hf o H2O (g) = - 57,8 Kcal/mol e
∆Hf o NH4NO3 (s) = - 87,3 Kcal/mol.
Provas
Descobriu-se que uma solução de ácido acético 0,10 M foi utilizada para provocar transtornos em um local público fechado, causando alergias e tosses. De acordo com a tabela apresentada abaixo, qual o indicador mais adequado para indicar o pH no ponto de equivalência de uma titulação de 25 mL dessa solução ácido acético 0,10 M com uma solução de hidróxido de sódio 0,10 M?

Provas
Um artefato explosivo foi interceptado. Ele constava de um sistema formado por dois compartimentos. O primeiro continha um recipiente que gotejou uma solução de ácido clorídrico concentrado em um frasco contendo zinco metálico no seu interior. Uma conexão de vidro ligava a saída lateral do frasco ao segundo compartimento, que armazenava o 1,5 L do gás formado nesse processo. Considerando que não houve perda na coleta do gás, qual a massa de zinco que reagiu nesse processo, a 300 K e 0,82 atm de pressão? (Dados: PM do Zn = 65,4 g/mol; R = 0,082 atm.L.mol–1 .K–1)
Provas
Os dispositivos de segurança denominados airbags contêm uma mistura de compostos químicos (azida de sódio e óxidos) e são rapidamente acionados em uma colisão brusca. Um impulso elétrico inicia uma série de reações químicas envolvendo NaN3, KNO3 e SiO2, que ocorrem na seqüência indicada pelas equações (1, 2 e 3), não balanceadas, mostradas abaixo. Considerando que o N2 é gerado nas duas reações, quantos litros de nitrogênio serão produzidos, aproximadamente, a 27°C e 1 atm de pressão a partir de 10 mols de NaN3? (Dado: R = 0,082 atm·L/mol·K.)
1. NaN3 → Na + N2
2. Na + KNO3 → K2O + Na2O + N2
3. K2O + Na2O + SiO2 → silicato alcalino
Provas
Um haleto de alquila foi preparado segundo uma reação de substituição, representada pela seguinte equação química:
![]()
De acordo com as características desse tipo de reação, é correto afirmar que:
Provas
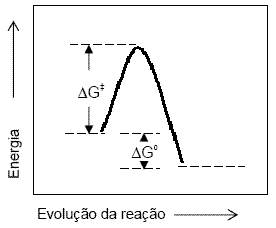
Dois compostos em análise reagem, segundo é ilustrado pelo diagrama de energia mostrado abaixo, que representa:
Provas
Um átomo de Hidrogênio sofre uma transição entre o primeiro estado excitado e o estado fundamental, cujas energias são E1 = -3,4 eV e E0 = -13,6 eV, respectivamente. Determine a freqüência do fóton emitido.
Provas
Um astronauta em uma espaçonave que viaja com velocidade v = 0,8 c em relação à terra, mede o intervalo de tempo ∆t = 3,0 min entre dois eventos que ocorrem no interior da nave. Para uma pessoa em repouso na terra, o intervalo de tempo medido entre os dois eventos é igual a:
Provas
Caderno Container