Foram encontradas 50 questões.
A remoção de H2S do GLP pode ser feita por meio de tratamento com solução aquosa a 20% em massa de dietanolamina (DEA), conforme a reação abaixo.

Sabendo-se que foram utilizados um excesso de 100% da base e um sistema sem reciclo, a massa da solução de DEA, em kg, posta para reagir com 10 mols de H2S, é
(Massas molares, em g/mol: H = 1; C = 12; N = 14; O = 16; S = 32)
Provas
As espécies CS2 e COS, presentes nos gases residuais de uma Unidade de Recuperação de Enxofre, precisam ser convertidas a H2S, para posterior absorção em solução de amina. Essa conversão é obtida por hidrólise, conforme as reações abaixo.
COS + H2O → H2S + CO2
CS2 + 2 H2O → 2 H2S + CO2
Foram hidrolizadas para conversão a H2S 728 gramas de uma mistura de COS e CS2. Sabendo-se que foram produzidos 612g de H2S, a proporção molar entre COS : CS2 na mistura inicial é
(Massas molares, em g/mol: H = 1 ; C = 12 ; O = 16 ; S = 32)
Provas
Qual o pH de uma solução 0,001 mol/L de ácido acético, sabendo-se que o grau de ionização do ácido nessas condições é de 10%?
Provas
Quanto à natureza das partículas do disperso, e quanto à afinidade entre o disperso e o dispergente, uma dispersão de cloreto de prata em água é composta por um disperso
Provas
Os sólidos cristalinos contêm seus elétrons ocupando estados eletrônicos organizados em estruturas de banda de energia. O grau de ocupação dessas bandas de energia determina a forma com que os elétrons respondem à aplicação de um campo elétrico, definindo sua condutividade. Das espécies abaixo, a que melhor conduz a corrente elétrica é
Provas
O acrílico é um polímero termoplástico, de aparência cristalina, com boa resistência à tensão e ao impacto. O monômero que lhe dá origem é o metacrilato de metila, cuja estrutura está representada abaixo.
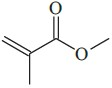
Com base no tipo de reação de polimerização, por meio da qual esse polímero é obtido, o acrílico é considerado um
Provas
O monitoramento ambiental realizado em amostras de efluentes de uma refinaria forneceu as seguintes concentrações de poluentes:
| Fração | Composição | Concentração | |
| I | BTEX | C6H6 a C8H10 | 1,2 ppm |
| II | Fenantrenos | C14H10 a C17H16 | 0,02 ppm |
| III | Alcanos lineares | C12H26 a C36H74 | 2,8 ppm |
| IV | Terpanos tricíclicos | C20H36 a C22H40 | 0,001 ppm |
| V | Fenol | C6H6O | 1,0 ppm |
A concentração de fenol detectada no efluente da refinaria corresponde a
(Massas molares, em g/mol: C = 12; H = 1; O =16)
Provas
O monitoramento ambiental realizado em amostras de efluentes de uma refinaria forneceu as seguintes concentrações de poluentes:
| Fração | Composição | Concentração | |
| I | BTEX | C6H6 a C8H10 | 1,2 ppm |
| II | Fenantrenos | C14H10 a C17H16 | 0,02 ppm |
| III | Alcanos lineares | C12H26 a C36H74 | 2,8 ppm |
| IV | Terpanos tricíclicos | C20H36 a C22H40 | 0,001 ppm |
| V | Fenol | C6H6O | 1,0 ppm |
Das frações analisadas, aquela que é composta por hidrocarbonetos com maior grau de insaturação é a
Provas
Considere a seguinte reação de oxirredução:
x H1+ + y MnO41– + z H2SO3 → t Mn2+ + w HSO41– + v H2O
De acordo com a equação balanceada, quantos mililitros de solução 0,1 mol/L de KMnO4 são necessários para oxidar 100 mL de solução 0,05 mol/L de H2SO3?
Provas
Com base nas propriedades ácido-base dos óxidos, foram feitas as seguintes afirmativas:
I - C!$ \ell !$2O6 reage com H2O gerando H2C!$ \ell !$O4;
II - A!$ \ell !$2O3 reage com NaOH gerando NaA!$ \ell !$O2;
III - FeO reage com HC!$ \ell !$ gerando FeC!$ \ell !$2.
Está(ão) correta(s) APENAS a(s) afirmativa(s)
Provas
Caderno Container