Foram encontradas 40 questões.
Nos ambientes naturais, os micro-organismos se encontram, quase sempre, sob forma de populações mistas. Assim sendo, para
que seja possível estudar as características das espécies que compõem tais misturas, é necessário fazer seu isolamento em
cultura pura. Para isso, necessita-se de um meio de cultura desejado. Após o seu crescimento, torna-se necessário, ainda, confirmar a sua pureza, de modo a garantir que a cultura obtida contenha apenas o micro-organismo de interesse. Sobre os meios
de cultura, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A adição de um carboidrato e um indicador de pH ao meio de cultura permite evidenciar as colônias de micro-organismos que produzem ácidos a partir da utilização daquele carboidrato, pois a cor do indicador irá se modificar em função da acidificação do meio ao redor da colônia.
( ) Turbidimetria é um método indireto no qual são contadas células totais, a partir da turvação observada no meio líquido onde ocorre o crescimento microbiano. Para essa contagem é preciso que seja obtida uma curva-padrão para cada micro- -organismo estudado, onde será relacionado o número de células conhecido com a turvação correspondente.
( ) Contagem direta em câmara de contagem é uma técnica estatística, na qual volumes da amostra original são inoculados em séries de tubos contendo um meio de cultura líquido apropriado. Comumente são empregadas três ou cinco séries, de cinco tubos cada, nas quais são inoculadas réplicas correspondentes de cada volume ou diluição da amostra original.
( ) Os meios sintéticos são utilizados para o isolamento de um grupo particular de micro-organismos, ou seja, são meios de cultura adicionados de substâncias químicas que irão propiciar o desenvolvimento dos micro-organismos de interesse e inibir o desenvolvimento dos micro-organismos acompanhantes.
A sequência está correta em
( ) A adição de um carboidrato e um indicador de pH ao meio de cultura permite evidenciar as colônias de micro-organismos que produzem ácidos a partir da utilização daquele carboidrato, pois a cor do indicador irá se modificar em função da acidificação do meio ao redor da colônia.
( ) Turbidimetria é um método indireto no qual são contadas células totais, a partir da turvação observada no meio líquido onde ocorre o crescimento microbiano. Para essa contagem é preciso que seja obtida uma curva-padrão para cada micro- -organismo estudado, onde será relacionado o número de células conhecido com a turvação correspondente.
( ) Contagem direta em câmara de contagem é uma técnica estatística, na qual volumes da amostra original são inoculados em séries de tubos contendo um meio de cultura líquido apropriado. Comumente são empregadas três ou cinco séries, de cinco tubos cada, nas quais são inoculadas réplicas correspondentes de cada volume ou diluição da amostra original.
( ) Os meios sintéticos são utilizados para o isolamento de um grupo particular de micro-organismos, ou seja, são meios de cultura adicionados de substâncias químicas que irão propiciar o desenvolvimento dos micro-organismos de interesse e inibir o desenvolvimento dos micro-organismos acompanhantes.
A sequência está correta em
Provas
Questão presente nas seguintes provas
3948381
Ano: 2025
Disciplina: Engenharia Ambiental e Sanitária
Banca: Consulplan
Orgão: Pref. João Ramalho-SP
Disciplina: Engenharia Ambiental e Sanitária
Banca: Consulplan
Orgão: Pref. João Ramalho-SP
Provas:
As caracterizações físico-químicas e biológicas da água e de soluções aquosas têm como objetivo identificar e quantificar os
elementos e espécies iônicas presentes nesses compostos e associar os efeitos de suas propriedades às questões ambientais,
permitindo a compreensão dos processos naturais ou alterações no meio ambiente. O conjunto de análises e métodos permitem
o entendimento do funcionamento dos ecossistemas, de seus problemas ambientais e a proposição de soluções viáveis para
resolução dos mesmos. Quanto aos métodos e princípios das análises físico-químicas e biológicas, é INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
3948380
Ano: 2025
Disciplina: Segurança e Saúde no Trabalho (SST)
Banca: Consulplan
Orgão: Pref. João Ramalho-SP
Disciplina: Segurança e Saúde no Trabalho (SST)
Banca: Consulplan
Orgão: Pref. João Ramalho-SP
Provas:
O uso dos Equipamentos de Proteção Individual (EPIs) e dos Equipamentos de Proteção Coletiva (EPCs) visa minimizar a possibilidade de contato das substâncias químicas com a pele, os olhos e o sistema respiratório, bem como a contenção em casos
de derramamento. Utilizando esses equipamentos de proteção adequadamente, minimiza-se o risco efetivo de acidentes ao
se manipular as diversas substâncias químicas em um laboratório. Sobre os EPIs, analise as seguintes afirmativas.
I. O avental para manuseio de substâncias químicas deve ser de algodão grosso, pois esse material queima mais devagar e reage com ácidos e bases, evitando, assim, que essas substâncias atinjam a pele.
II. Os óculos de segurança com vedação nas laterais são utilizadossomente para transferência de produtos químicos corrosivos.
III. Respiradores simples com filtros químicos possuem filtros adsorvedores capazes de reter gases e vapores de substâncias químicas.
Está correto o que a afirma em
I. O avental para manuseio de substâncias químicas deve ser de algodão grosso, pois esse material queima mais devagar e reage com ácidos e bases, evitando, assim, que essas substâncias atinjam a pele.
II. Os óculos de segurança com vedação nas laterais são utilizadossomente para transferência de produtos químicos corrosivos.
III. Respiradores simples com filtros químicos possuem filtros adsorvedores capazes de reter gases e vapores de substâncias químicas.
Está correto o que a afirma em
Provas
Questão presente nas seguintes provas
Uma das propriedades mais importantes da água é a sua capacidade de dissolver grande variedade de substâncias. Muitas
das reações químicas que acontecem no organismo do homem ou ao seu redor ocorrem devido às substâncias dissolvidas na
água. Considere que o técnico em química recebeu a tarefa de realizar alguns experimentos, ou seja, realizar algumas reações
químicas e anotar as observações diante de cada reação, observe:
1. Reação de uma solução de ácido clorídrico (HCl) com raspas de zinco.
2. Reação entre as soluções de carbonato de sódio (Na2CO3) e ácido bromídrico (HBr).
3. Reação entre as soluções de nitrato de prata (AgNO3) e cloreto de potássio (KCl). Sobre as observações anotadas, analise as afirmativas a seguir.
I. Na reação entre uma solução de ácido clorídrico com raspas de zinco ocorreu desprendimento de gás.
II. Na reação entre o carbonato de sódio e uma solução de ácido bromídrico ocorreu desprendimento de gás.
III. Na reação entre uma solução de nitrato de prata com uma solução de cloreto de potássio se formaram dois sais insolúveis.
Está correto o que se afirma em
1. Reação de uma solução de ácido clorídrico (HCl) com raspas de zinco.
2. Reação entre as soluções de carbonato de sódio (Na2CO3) e ácido bromídrico (HBr).
3. Reação entre as soluções de nitrato de prata (AgNO3) e cloreto de potássio (KCl). Sobre as observações anotadas, analise as afirmativas a seguir.
I. Na reação entre uma solução de ácido clorídrico com raspas de zinco ocorreu desprendimento de gás.
II. Na reação entre o carbonato de sódio e uma solução de ácido bromídrico ocorreu desprendimento de gás.
III. Na reação entre uma solução de nitrato de prata com uma solução de cloreto de potássio se formaram dois sais insolúveis.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A coleta de amostras de água se constitui em um dos elementos fundamentais no desenvolvimento de um programa de
controle da qualidade da água. Embora considerada uma atividade simples, alguns critérios técnicos, como a exigência de
pessoal treinado, devem ser rigorosamente observados no processo de amostragem, a fim de que as amostras sejam representativas do nível de qualidade que se pretende determinar. Sobre a coleta de amostras de água, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A coleta de água tratada deve ser realizada diretamente da torneira, fazendo-se a desinfecção com hipoclorito de sódio a 10%.
( ) As amostras destinadas às análises físico-químicas devem ser acondicionadas em frascos de vidro neutro, devidamente limpos e secos; e identificadas, a fim de se evitar erros.
( ) As amostras coletadas para análise bacteriológica devem ser transportadas em caixas térmicas, em temperatura em torno de 25°C e o período de transporte deve ser de oito horas, sendo que o tempo para a realização das análises não deve exceder vinte e quatro horas.
( ) A coleta de água bruta deve ser realizada em ponto estratégico do manancial de captação ou, quando não é possível, na chegada da água bruta na Estação de Tratamento de Água (ETA).
A sequência está correta em
( ) A coleta de água tratada deve ser realizada diretamente da torneira, fazendo-se a desinfecção com hipoclorito de sódio a 10%.
( ) As amostras destinadas às análises físico-químicas devem ser acondicionadas em frascos de vidro neutro, devidamente limpos e secos; e identificadas, a fim de se evitar erros.
( ) As amostras coletadas para análise bacteriológica devem ser transportadas em caixas térmicas, em temperatura em torno de 25°C e o período de transporte deve ser de oito horas, sendo que o tempo para a realização das análises não deve exceder vinte e quatro horas.
( ) A coleta de água bruta deve ser realizada em ponto estratégico do manancial de captação ou, quando não é possível, na chegada da água bruta na Estação de Tratamento de Água (ETA).
A sequência está correta em
Provas
Questão presente nas seguintes provas
Para um determinado experimento, o técnico em química deverá preparar 100 mL de solução de sacarose 0,02 mol/L seguindo
os seguintes procedimentos:
• Determinar a massa de sacarose a ser pesada;
• Pesar a quantidade calculada em um béquer de 50 mL;
• Adicionar, aproximadamente, 20 mL de água destilada ao béquer contendo a sacarose e dissolver o sólido com o auxílio de um bastão de vidro;
• Transferir essa solução para um balão volumétrico de 100 mL “quantitativamente”;
• Efetuar, pelo menos, 3 lavagens do béquer e do bastão de vidro com, no máximo, 20 mL de água destilada em cada lavagem, transferindo sempre para o balão volumétrico;
• Completar o volume do balão volumétrico com água destilada até o traço de aferição; e
• Agitar o balão volumétrico para homogeneizar a solução.
(Dados: MM sacarose: 342 g/mol.)
Qual a massa de sacarose a ser pesada para o preparo da solução?
• Determinar a massa de sacarose a ser pesada;
• Pesar a quantidade calculada em um béquer de 50 mL;
• Adicionar, aproximadamente, 20 mL de água destilada ao béquer contendo a sacarose e dissolver o sólido com o auxílio de um bastão de vidro;
• Transferir essa solução para um balão volumétrico de 100 mL “quantitativamente”;
• Efetuar, pelo menos, 3 lavagens do béquer e do bastão de vidro com, no máximo, 20 mL de água destilada em cada lavagem, transferindo sempre para o balão volumétrico;
• Completar o volume do balão volumétrico com água destilada até o traço de aferição; e
• Agitar o balão volumétrico para homogeneizar a solução.
(Dados: MM sacarose: 342 g/mol.)
Qual a massa de sacarose a ser pesada para o preparo da solução?
Provas
Questão presente nas seguintes provas
O técnico em química precisa determinar a concentração de cálcio em uma amostra de 200 mL de uma água natural. Para tal
análise, ele utilizou o método da gravimetria por precipitação seguindo os seguintes passos:
1. Adicionou a solução contendo amostra excesso de ácido oxálico;
2. Adicionou, também, amônia para neutralizar o ácido e provocar a precipitação completa do cálcio;
3. O precipitado formado foi filtrado, utilizando um cadinho de filtração que ele encontrou sobre a bancada do laboratório;
4.O precipitado filtrado foi seco e calcinado; e
5. Após o resfriamento, o precipitado juntamente ao cadinho de filtração foi pesado e a massa de óxido de cálcio encontrada.
Após seguir cada passo para determinar a concentração de cálcio em determinada amostra, o técnico em química cometeu quantos erros?
1. Adicionou a solução contendo amostra excesso de ácido oxálico;
2. Adicionou, também, amônia para neutralizar o ácido e provocar a precipitação completa do cálcio;
3. O precipitado formado foi filtrado, utilizando um cadinho de filtração que ele encontrou sobre a bancada do laboratório;
4.O precipitado filtrado foi seco e calcinado; e
5. Após o resfriamento, o precipitado juntamente ao cadinho de filtração foi pesado e a massa de óxido de cálcio encontrada.
Após seguir cada passo para determinar a concentração de cálcio em determinada amostra, o técnico em química cometeu quantos erros?
Provas
Questão presente nas seguintes provas
Para avaliar a qualidade da água para consumo humano, um dos parâmetros monitorados é o teor de cloreto. Em um laboratório
de análises, o químico precisava determinar esse teor de cloreto por titulação com uma solução padrão de AgNO3. Para isso, o
profissional prosseguiu com a análise através dos procedimentos descritos a seguir:
1. Com uma pipeta de 50 mL, pipete esse volume de NaCl;
2. Transfira esse volume de NaCl para um erlenmeyer de 50 mL;
3. Titule lentamente com a solução padronizada de AgNO3 0,05 mol/L até que mude a cor de forma permanente; e
4. Anote o volume consumido de AgNO3. (Observação: volume gasto de AgNO3 na titulação: 1 mL.)
A partir da realização de todas as etapas e das observações experimentais, analise as afirmativas a seguir.
I. O teor de cloreto é 0,001 mol/L.
II. A equação da reação envolvida é Cl(aq)- + AgNO3(aq) → AgCl(s) + NO3 - (aq)
III. A quantidade de matéria, em mol, de nitrato de prata presente no volume consumido no processo é 0,05 mol.
Está correto o que se afirma em
1. Com uma pipeta de 50 mL, pipete esse volume de NaCl;
2. Transfira esse volume de NaCl para um erlenmeyer de 50 mL;
3. Titule lentamente com a solução padronizada de AgNO3 0,05 mol/L até que mude a cor de forma permanente; e
4. Anote o volume consumido de AgNO3. (Observação: volume gasto de AgNO3 na titulação: 1 mL.)
A partir da realização de todas as etapas e das observações experimentais, analise as afirmativas a seguir.
I. O teor de cloreto é 0,001 mol/L.
II. A equação da reação envolvida é Cl(aq)- + AgNO3(aq) → AgCl(s) + NO3 - (aq)
III. A quantidade de matéria, em mol, de nitrato de prata presente no volume consumido no processo é 0,05 mol.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
3948374
Ano: 2025
Disciplina: Técnicas em Laboratório
Banca: Consulplan
Orgão: Pref. João Ramalho-SP
Disciplina: Técnicas em Laboratório
Banca: Consulplan
Orgão: Pref. João Ramalho-SP
Provas:
Historicamente, a literatura reporta que, em 1855, Theodor Escherich isolou uma bactéria em fezes de crianças, a qual recebeu a denominação original de Bacterium coli e mais tarde foi confirmada como habitante do trato intestinal de seres humanos e animais de sangue quente (Hofstra e Huisin’t Veld, 1988). Subsequentes tentativas de diferenciar a Bacterium coli de
outras bactérias da família Enterobacteriaceae (Jones, 1988), entre elas, aquelas mais nitidamente associadas à contaminação
de natureza fecal, deram origem à subclassificação do grupo coli – aerogenes, ou “coliformes”, e a definição de sua composição pelos gêneros Escherichia, Klebsiella e Citrobacter (1956), posteriormente complementado pela inclusão do gênero Enterobacter (Müller e Mossel, 1982; Hofstra e Huisin’t Veld, 1988). Sobre o método de análise, bem como as bactérias do grupo coliforme,
analise as afirmativas a seguir.
I. Coliformes totais são bacilos gram-negativos, aeróbios ou anaeróbios facultativos, capazes de se desenvolverem na presença de sais biliares ou agentes tensoativos que fermentam a lactose com produção de ácido, gás e aldeído a 35,0 ± 0,5°C em 24-48 horas; podem apresentar atividade da enzima ß galactosidase.
II. Escherichia coli é uma bactéria do grupo coliforme que fermenta lactose e manitol, com produção de ácido e gás a 44,5°C ± 0,2oC em 24 horas. Apresenta atividade das enzimas ß galactosidase e ß glucoronidase, sendo considerada o mais específico indicador de contaminação fecal recente e de eventual presença de organismos patogênicos.
III. O método do substrato cromogênico se baseia nas atividades enzimáticas específicas dos coliformes e E. coli. Os meios de cultura contêm nutrientes indicadores (substrato cromogênico) que, hidrolisados pelas enzimas específicas dos coliformes e/ou, E. coli, provocam uma mudança de cor no meio-amarelo, no caso de coliformes – ou produzem fluorescência quando a amostra é exposta à luz ultravioleta – no caso de E. coli.
Está correto o que se afirma em
I. Coliformes totais são bacilos gram-negativos, aeróbios ou anaeróbios facultativos, capazes de se desenvolverem na presença de sais biliares ou agentes tensoativos que fermentam a lactose com produção de ácido, gás e aldeído a 35,0 ± 0,5°C em 24-48 horas; podem apresentar atividade da enzima ß galactosidase.
II. Escherichia coli é uma bactéria do grupo coliforme que fermenta lactose e manitol, com produção de ácido e gás a 44,5°C ± 0,2oC em 24 horas. Apresenta atividade das enzimas ß galactosidase e ß glucoronidase, sendo considerada o mais específico indicador de contaminação fecal recente e de eventual presença de organismos patogênicos.
III. O método do substrato cromogênico se baseia nas atividades enzimáticas específicas dos coliformes e E. coli. Os meios de cultura contêm nutrientes indicadores (substrato cromogênico) que, hidrolisados pelas enzimas específicas dos coliformes e/ou, E. coli, provocam uma mudança de cor no meio-amarelo, no caso de coliformes – ou produzem fluorescência quando a amostra é exposta à luz ultravioleta – no caso de E. coli.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A identificação de determinado grupo funcional é feita com o reagente de Jones, que consiste em uma solução de ácido
crômico e ácido sulfúrico. O ácido ascórbico, que é um álcool, é oxidado pelo reagente de Jones, resultando em uma mudança
de sua estrutura química. O teste de Jones com o ácido ascórbico é representado pela equação a seguir; analise-a.
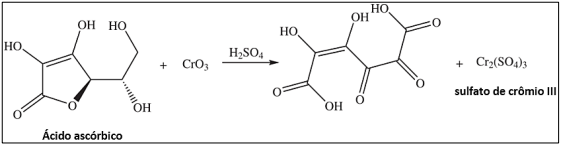
Considerando que uma massa de 200 g de ácido ascórbico (80% de pureza) sofre oxidação, qual a massa, em gramas, de sulfato de crômio III- Cr2(SO4)3 obtido?
(Considere a estequiometria da reação 1:1 / Dados: MM ácido ascórbico = 176 g/mol.)

Considerando que uma massa de 200 g de ácido ascórbico (80% de pureza) sofre oxidação, qual a massa, em gramas, de sulfato de crômio III- Cr2(SO4)3 obtido?
(Considere a estequiometria da reação 1:1 / Dados: MM ácido ascórbico = 176 g/mol.)
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container