Foram encontradas 50 questões.
A respeito do procedimento de gravimetria por precipitação, analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. A digestão é um processo no qual o precipitado formado é aquecido por um determinado tempo na solução em que foi formado (solução-mãe), possibilitando obter um precipitado mais puro e de melhor filtrabilidade.
II. Para favorecer o crescimento das partículas de um precipitado durante a sua formação, deve-se minimizar a supersaturação relativa da solução.
III. A peptização de um precipitado coloidal coagulado é um procedimento essencial que permite obter partículas de maior tamanho e mais puras.
Provas
Para se determinar a solubilidade do BaSO4, retirou-se uma alíquota de 200 ml da solução saturada de sulfato de bário e procedeu-se à secagem dessa solução em uma cápsula de porcelana sob exposição ao bico de Bunsen. Após a evaporação completa da solução, a massa de resíduo sólido (BaSO4) obtido foi de 0,00233 g. Considerando essas informações, assinale a alternativa que apresenta a solubilidade molar (mol/L) do sulfato de bário.
Provas
Durante um procedimento experimental, o técnico responsável pelo laboratório preparou uma mistura contendo solução aquosa de amônia e solução aquosa de cloreto de amônio, resultando em um volume total de 1,0 litro. Sabendo que na solução resultante, em equilíbrio, ambas as soluções apresentam a mesma concentração, de 0,10 mol/L (a 25 °C), analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. A solução resultante tem caráter ácido.
II. A solução resultante possui [H3O+ ] = 1,8×10−5 mol/L.
III. A solução resultante corresponde a uma solução tampão.
Dados: Kb (NH3) = 1,8×10−5 (25 °C); Kw (H2O) = 1,0×10−14 (25 °C).
Provas
A respeito dos instrumentos volumétricos de laboratório e de sua utilização, assinale a alternativa correta.
Provas
Assinale a alternativa que apresenta um reagente padrão primário para padronizar uma solução de hidróxido de sódio.
Provas
Um técnico de laboratório preparou uma solução de ácido clorídrico (HCl) a uma concentração estimada de 0,1 mol/L. Para a padronização dessa solução, retirou-se uma alíquota de 10,00 ml da solução de HCl e procedeu-se à titulação com uma solução-padrão de NaOH 0,1500 mol/L, consumindo o volume de 9,00 ml até o ponto final.
Considerando essa informação, assinale a alternativa que apresenta a concentração (mol/L) da solução de HCl padronizada.
Provas
No laboratório de análises físico-químicas de águas, foi necessário preparar 250 ml de uma solução de sulfato de sódio a 20 mg/ml a partir de uma solução-estoque a 100 mg/ml. Assinale a alternativa que apresenta o volume necessário (ml) da solução estoque a ser utilizado para preparar a referida solução.
Provas
No laboratório de análises físico-químicas de águas, foi necessário preparar 250 ml de uma solução de sulfato de sódio a 20 mg/ml a partir de uma solução-estoque a 100 mg/ml. Assinale a alternativa que apresenta o volume necessário (ml) da solução estoque a ser utilizado para preparar a referida solução.
Provas
Em uma análise titulométrica ácido-base, envolvendo o titulante padrão NaOH, obteve-se o seguinte resultado, representado pela curva de titulação (pH vs volume de titulante) a seguir:
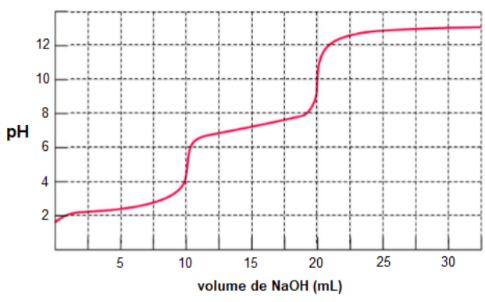
A partir desse perfil gráfico, assinale a alternativa que apresenta uma substância provável que foi titulada.
Provas
Em laboratórios, é comum proceder à secagem de diversos utensílios e vidrarias utilizando uma estufa de esterilização/secagem em temperaturas superiores a 70 °C. Assinale a alternativa que apresenta uma vidraria para a qual NÃO se deve proceder à secagem sob essas condições.
Provas
Caderno Container