Foram encontradas 50 questões.
Provas
Provas
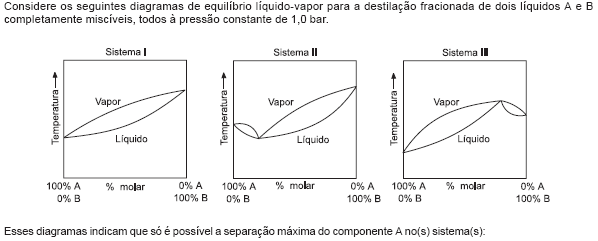
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
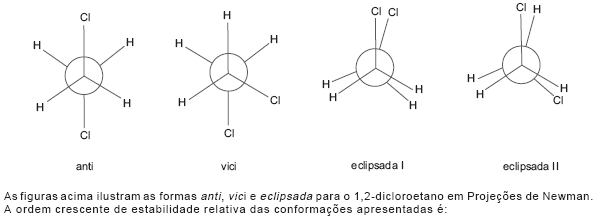
- Química OrgânicaIsomeria Plana e Espacial
Considere as espécies abaixo.
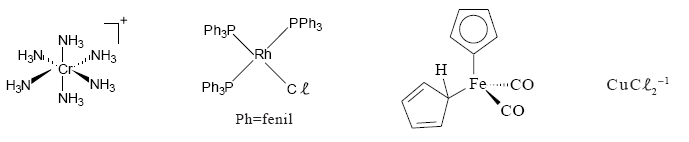 A geometria do composto organometálico é:
A geometria do composto organometálico é:
Provas
Para avaliar o nível de poluição de um curso d'água, foram analisadas amostras coletadas em seis pontos distintos desse rio.
Os resultados obtidos para oxigênio dissolvido (OD), demanda bioquímica de oxigênio (DBO) e demanda química de
oxigênio (DQO) estão apresentados nos gráficos abaixo.
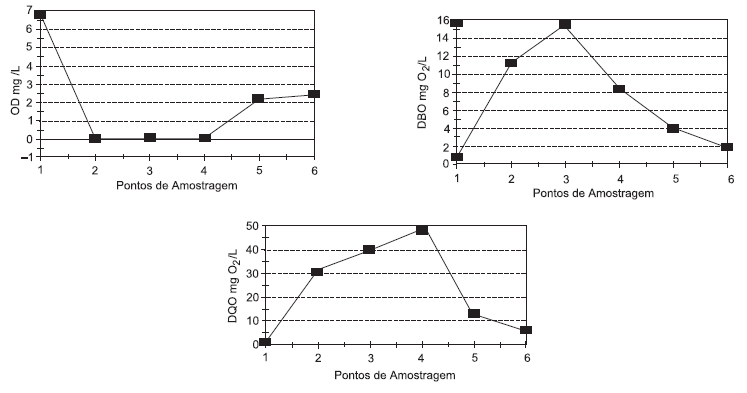 Os resultados dessas análises indicam que:
Os resultados dessas análises indicam que:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Transformações Químicas e EnergiaTermoquímica
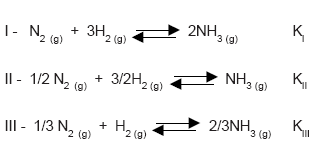 A alternativa que relaciona corretamente as constantes de
equilíbrio, a uma mesma temperatura, é:
A alternativa que relaciona corretamente as constantes de
equilíbrio, a uma mesma temperatura, é:Provas
Nos garimpos da Amazônia, o mercúrio metálico é empregado na extração de ouro e, por ser um metal de alta toxicidade com propriedades bioacumulativas, acarreta sérios danos ao meio ambiente e à saúde humana. Vários estudos têm sido realizados visando ao controle dos teores de mercúrio em águas, solos e alimentos. Em geral, a metodologia envolve um pré-tratamento da amostra, através da redução química do mercúrio para liberá-lo em sua forma metálica, de modo a proceder à determinação quantitativa do metal na matriz estudada. Dentre as técnicas analíticas abaixo, aquela adequada a determinações quantitativas de mercúrio é a:
Provas
Considere o diagrama de equilíbrio das fases sólida, líquida e vapor da água ilustrado esquematicamente abaixo e as afirmativas que se seguem.
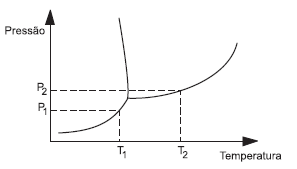
I - Um aumento da pressão externa provoca um abaixamento do ponto de fusão do sólido.
II - Uma diminuição de pressão externa provoca uma elevação no ponto de ebulição do líquido.
III - A pressão P1 corresponde à pressão de vapor do líquido na temperatura T1.
IV - A pressão P2 corresponde à pressão de vapor do líquido a temperatura T2.
Estão corretas apenas as afirmações
Provas
O teor de cobre em uma amostra de sal de cobre II foi determinado por titulação de oxirredução indireta utilizando-se o seguinte procedimento: uma amostra com 3,0 g do sal foi dissolvida em água deionizada e avolumada em balão volumétrico de 250 mL. Uma alíquota de 50,00 mL foi, então, tratada com 1g de KI, conforme a reação abaixo.
Cu+2 + 2I− → Cu+1 + I2
Em seguida, o iodo liberado foi convertido a I− através de titulação. O titulante adequado a esta análise é o:
Provas
Considere os mais simples orbitais atômicos s, p, d e f (1s, 2p, 3d e 4f). A soma total do número de planos nodais existentes nesses quatro orbitais é:
Provas

Provas
Caderno Container