Foram encontradas 897 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Química OrgânicaTipos de Reagentes e Mecanismos das Reações Orgânicas
A reação abaixo representa a formação do íon acílio, por meio da ação do catalisador A1C13, durante uma reação de acilação de Fiedel-Crafts (etapa 1 da rota de Boots apresentada no texto).
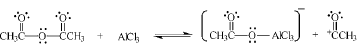
A respeito do mecanismo apresentado e das espécies envolvidas, julgue o item subsequente.
No mecanismo apresentado, o A1C13 atua como um ácido de Lewis.
Provas
A reação abaixo representa a formação do íon acílio, por meio da ação do catalisador A1C13, durante uma reação de acilação de Fiedel-Crafts (etapa 1 da rota de Boots apresentada no texto).
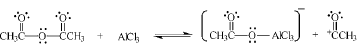
A respeito do mecanismo apresentado e das espécies envolvidas, julgue o item subsequente.
O mecanismo apresentado envolve a quebra homolítica de uma ligação química covalente.
Provas
A reação abaixo representa a formação do íon acílio, por meio da ação do catalisador A1C13, durante uma reação de acilação de Fiedel-Crafts (etapa 1 da rota de Boots apresentada no texto).
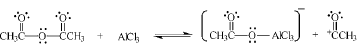
A respeito do mecanismo apresentado e das espécies envolvidas, julgue o item subsequente.
O íon acílio formado apresenta maior estabilidade que o carbocátion alquílico +CH2CH3.
Provas
O bombardeamento do urânio-235 com nêutrons induz a um a série de reações de fissão nuclear altamente energéticas. Em uma dessas reações, após a captura de um nêutron (1n), o urânio se desintegra para formar um átomo de césio-137, um isótopo X, e dois outros nêutrons capazes de gerar uma reação em cadeia:

O césio-137 assim formado é um isótopo radioativo que emite radiações gama e beta e pode ser em pregado em radioterapia com o intuito de destruir células cancerosas.
A partir do texto acima e considerando que o tempo de m eia-vida do césio-137 é de 30 anos, julgue o item que se segue.
O isótopo X da reação apresentada consiste em um átomo de 98Sr.
Provas
O bombardeamento do urânio-235 com nêutrons induz a um a série de reações de fissão nuclear altamente energéticas. Em uma dessas reações, após a captura de um nêutron (1n), o urânio se desintegra para formar um átomo de césio-137, um isótopo X, e dois outros nêutrons capazes de gerar uma reação em cadeia:

O césio-137 assim formado é um isótopo radioativo que emite radiações gama e beta e pode ser em pregado em radioterapia com o intuito de destruir células cancerosas.
A partir do texto acima e considerando que o tempo de m eia-vida do césio-137 é de 30 anos, julgue o item que se segue.
A radiação beta possui maior poder de penetração que a radiação gama.
Provas
O bombardeamento do urânio-235 com nêutrons induz a um a série de reações de fissão nuclear altamente energéticas. Em uma dessas reações, após a captura de um nêutron (1n), o urânio se desintegra para formar um átomo de césio-137, um isótopo X, e dois outros nêutrons capazes de gerar uma reação em cadeia:

O césio-137 assim formado é um isótopo radioativo que emite radiações gama e beta e pode ser em pregado em radioterapia com o intuito de destruir células cancerosas.
A partir do texto acima e considerando que o tempo de m eia-vida do césio-137 é de 30 anos, julgue o item que se segue.
Mesmo após um período de 300 anos, mais de 1% dos átomos de césio-137 deverão estar ativos.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um químico desejava preparar 500 mL de uma solução de hidróxido de amônio (NH4OH) 0,10 mol/L pela diluição de uma solução estoque de NH4OH que, segundo o rótulo do frasco, apresenta concentração 30% em m assa e densidade 0,895 g/mL. Com base nesses dados, o químico realizou o cálculo do volume da solução estoque a ser em pregado e preparou a solução. Como a amônia é um a substância altamente volátil, o químico julgou conveniente aferir a concentração da solução resultante realizando a titulação de 20,0 mL dessa solução com uma solução padrão de HC1 0,090 mol/L.
Considerando que, a 25 °C, a constante de basicidade do NH4OH é igual a 1,8 x 10 5 e a constante de autoprotólise da água, definida como o produto das atividades dos íons hidróxido e hidrônio, é igual a 1,0 x 10-14 , e atribuindo comportamento ideal para todas as soluções envolvidas, julgue o item seguinte, tendo o texto apresentado como referência.
De acordo com os dados fornecidos no rótulo do frasco, a concentração da solução estoque de NH4OH é superior a 7,0 mol/L.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um químico desejava preparar 500 mL de uma solução de hidróxido de amônio (NH4OH) 0,10 mol/L pela diluição de uma solução estoque de NH4OH que, segundo o rótulo do frasco, apresenta concentração 30% em m assa e densidade 0,895 g/mL. Com base nesses dados, o químico realizou o cálculo do volume da solução estoque a ser em pregado e preparou a solução. Como a amônia é um a substância altamente volátil, o químico julgou conveniente aferir a concentração da solução resultante realizando a titulação de 20,0 mL dessa solução com uma solução padrão de HC1 0,090 mol/L.
Considerando que, a 25 °C, a constante de basicidade do NH4OH é igual a 1,8 x 10 5 e a constante de autoprotólise da água, definida como o produto das atividades dos íons hidróxido e hidrônio, é igual a 1,0 x 10-14 , e atribuindo comportamento ideal para todas as soluções envolvidas, julgue o item seguinte, tendo o texto apresentado como referência.
O volume de solução estoque em pregada para a preparação da solução desejada foi superior a 8,0 mL.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Um químico desejava preparar 500 mL de uma solução de hidróxido de amônio (NH4OH) 0,10 mol/L pela diluição de uma solução estoque de NH4OH que, segundo o rótulo do frasco, apresenta concentração 30% em m assa e densidade 0,895 g/mL. Com base nesses dados, o químico realizou o cálculo do volume da solução estoque a ser em pregado e preparou a solução. Como a amônia é um a substância altamente volátil, o químico julgou conveniente aferir a concentração da solução resultante realizando a titulação de 20,0 mL dessa solução com uma solução padrão de HC1 0,090 mol/L.
Considerando que, a 25 °C, a constante de basicidade do NH4OH é igual a 1,8 x 10 5 e a constante de autoprotólise da água, definida como o produto das atividades dos íons hidróxido e hidrônio, é igual a 1,0 x 10-14 , e atribuindo comportamento ideal para todas as soluções envolvidas, julgue o item seguinte, tendo o texto apresentado como referência.
O indicador ácido-base mais apropriado para a detecção do ponto final da titulação deve apresentar a faixa de viragem em pH ácido.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um químico desejava preparar 500 mL de uma solução de hidróxido de amônio (NH4OH) 0,10 mol/L pela diluição de uma solução estoque de NH4OH que, segundo o rótulo do frasco, apresenta concentração 30% em m assa e densidade 0,895 g/mL. Com base nesses dados, o químico realizou o cálculo do volume da solução estoque a ser em pregado e preparou a solução. Como a amônia é um a substância altamente volátil, o químico julgou conveniente aferir a concentração da solução resultante realizando a titulação de 20,0 mL dessa solução com uma solução padrão de HC1 0,090 mol/L.
Considerando que, a 25 °C, a constante de basicidade do NH4OH é igual a 1,8 x 10 -5 e a constante de autoprotólise da água, definida como o produto das atividades dos íons hidróxido e hidrônio, é igual a 1,0 x 10-14 , e atribuindo comportamento ideal para todas as soluções envolvidas, julgue o item seguinte, tendo o texto apresentado como referência.
A 25 °C, a porcentagem de dissociação do NH4OH em uma solução 0,10 mol/L é superior a 1 %.
Provas
Caderno Container