Foram encontradas 897 questões.
Considerando a constante de Faraday igual a 96.500 C/mol e as informações apresentadas acima, julgue o próximos item.
O potencial elétrico mínimo (E) que deve ser aplicado à célula eletrolítica para que ocorra a eletrólise do NaCl pode ser calculado pela equação E = E (Na+/Na) + 2E (Cl2/ Cl- ) , em que E ( Na+ /Na ) e E(C12 /Cl- ) são, respectivamente, os potenciais elétricos de redução dos pares Na+/Na e Cl2/Cl- na temperatura do experimento.
Provas
Considerando a constante de Faraday igual a 96.500 C/mol e as informações apresentadas acima, julgue o próximo item.
No processo, sabendo que M(Na) = 23 g/mol, a circulação de uma corrente elétrica igual a 2,0 A em um intervalo de 4.825 s deve produzir uma massa superior a 2,0 g de sódio metálico.
Provas
Considerando a constante de Faraday igual a 96.500 C/mol e as informações apresentadas acima, julgue o próximo item.
A formação de 2,0 g de sódio metálico deve ser acompanhada pela formação de uma massa superior a 4,0 g de Cl2.
Provas
Considerando a constante de Faraday igual a 96.500 C/mol e as informações apresentadas acima, julgue o próximo item.
A partir da localização do N a e do K na tabela periódica, é correto concluir que a eletrólise do KC1 requer a aplicação de um potencial elétrico maior que aquele requerido para a eletrólise do NaCl.
Provas
Considerando a constante de Faraday igual a 96.500 C/mol e as informações apresentadas acima, julgue o próximo item.
Na produção do sódio metálico, é possível realizar a eletrólise do NaCl na forma sólida.
Provas
Considerando a constante de Faraday igual a 96.500 C/mol e as informações apresentadas acima, julgue o próximo item.
Os mesmos produtos produzidos na eletrólise do NaCl puro são obtidos na eletrólise de uma solução aquosa de NaCl.
Provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A reação abaixo representa a formação do íon acílio, por meio da ação do catalisador A1C13, durante uma reação de acilação de Fiedel-Crafts (etapa 1 da rota de Boots apresentada no texto).
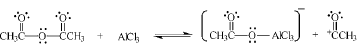
A respeito do mecanismo apresentado e das espécies envolvidas, julgue o item subsequente.
O A1C13 apresenta três ligações covalentes polares e a molécula, como um todo, é apoiar.
Provas
Nas ciências humanas, a fase de estabelecimento e clarifícação da problemática e do próprio problema constitui o momento crucial da pesquisa. A partir dessa afirmação, julgue o item seguinte.
A pesquisa fundamental destina-se a ampliar os saberes disponíveis, que podem, em algum momento, ser utilizados para solucionar problemas oriundos do meio social.
Provas
Nas ciências humanas, a fase de estabelecimento e clarifícação da problemática e do próprio problema constitui o momento crucial da pesquisa. A partir dessa afirmação, julgue o item seguinte.
O seguinte enunciado constitui um problema de pesquisa sociológica corretamente formulado: a causa principal do divórcio é o casamento e a solução do problema é a sua interdição.
Provas
Nas ciências humanas, a fase de estabelecimento e clarifícação da problemática e do próprio problema constitui o momento crucial da pesquisa. A partir dessa afirmação, julgue o item seguinte.
Um problema de pesquisa deve ser resolvido pela intuição, tradição, senso comum ou especulação.
Provas
Caderno Container