Foram encontradas 924 questões.
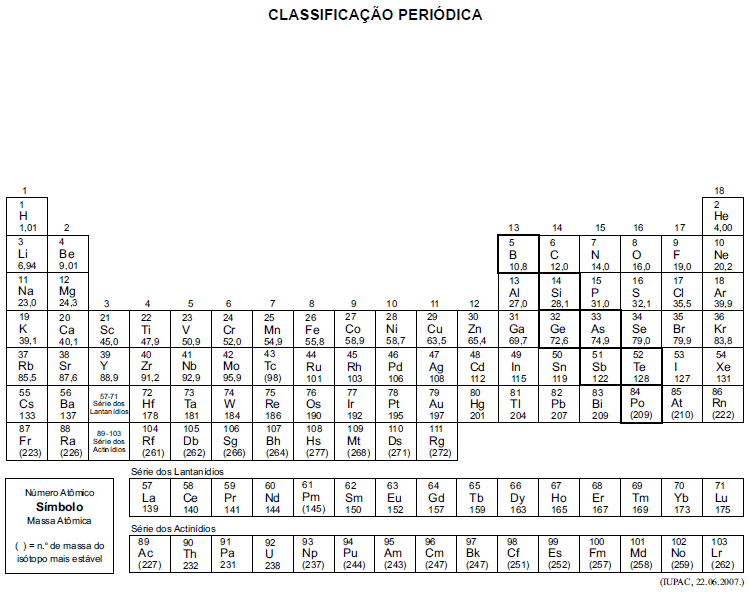
A tabela periódica encontra-se no final deste caderno.
Os minérios de cobre são as fontes naturais do cobre metálico utilizado em fios condutores de eletricidade e de vários compostos de cobre produzidos industrialmente, entre eles, o sulfato de cobre (II), amplamente utilizado como fungicida e algicida no tratamento de águas de reservatórios e na agricultura. Embora a origem seja a mesma, a produção do cobre metálico empregado como condutor elétrico tem custo muito maior do que a do sulfato de cobre (II). Uma das principais razões para essa diferença de custo é o fato de
Provas
A tabela periódica encontra-se no final deste caderno.

A massa máxima de hidrogênio gasoso, H2 (g), que pode ser obtida pela adição de 1,15 g de sódio metálico a 1 000 g de água líquida é, em gramas, igual a
Provas
A tabela periódica encontra-se no final deste caderno.


Provas
A tabela periódica encontra-se no final deste caderno.

Provas
A tabela periódica encontra-se no final deste caderno.

Considere as seguintes informações sobre o cloreto de hidrogênio, HCl:
– apresenta ponto de fusão igual a – 114 ºC e ponto de ebulição igual a – 85 ºC, a 1 atm;
– quando puro, no estado líquido, conduz muito mal a corrente elétrica;
– ao interagir com água líquida, origina solução aquosa que conduz muito bem a corrente elétrica.
Sendo assim, o HCl é um __________ nas condições ambiente. Conduz mal a corrente elétrica no estado líquido, pois a ligação entre os átomos em sua molécula é __________ . Em contato com a água líquida, essas ligações são rompidas, originando __________ hidratados.
As lacunas desse texto são preenchidas, correta e respectivamente, por:
Provas
A tabela periódica encontra-se no final deste caderno.

Comparando-se os modelos atômicos de Thomson, Rutherford e Bohr, é possível afirmar que os três permitem justificar
I. a ionização de gases verificada em tubos de descarga sob baixa pressão e alta tensão elétrica.
II. os espectros de emissão luminosa emitidos por diferentes elementos químicos.
III. a presença de nêutrons no núcleo dos átomos.
Está correto o que se afirma apenas em
Provas
A tabela periódica encontra-se no final deste caderno.


Provas
A tabela periódica encontra-se no final deste caderno.

Considerando 1 mol de cada um dos compostos indicados nas alternativas apresentadas, indique o que requer maior massa de oxigênio, O2 , para sua combustão completa.
Provas
A tabela periódica encontra-se no final deste caderno.


Provas
A tabela periódica encontra-se no final deste caderno.

Pode-se obter cal hidratada a partir de cal viva e água pela transformação representada por:
cal viva + água – energia → cal hidratada
Por outro lado, pode-se obter cal viva e água a partir da cal hidratada, pela transformação representada por:
cal hidratada + energia → cal viva + água
Examinando-se essas representações, conclui-se que a
I. obtenção de cal hidratada é um processo exoergônico;
II. cal hidratada é uma mistura de substâncias constituída por cal viva e água;
III. obtenção de cal viva e água a partir de cal hidratada é um processo revertível.
Está correto o que se afirma apenas em
Provas
Caderno Container