Foram encontradas 120 questões.
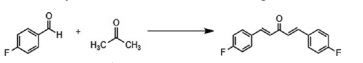
Com base nessas informações, julgue o item a seguir.
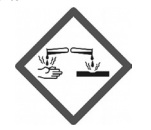
Considerando as características químicas da acetona, o pictograma a seguir representa corretamente um dos elementos de risco presentes no rótulo desse solvente.
Provas
Acerca da mudança de estado, das características e das propriedades e das ligações químicas nos sólidos, julgue o item seguinte.
Nas mudanças de estado físico, a temperatura da substância pura permanece constante enquanto ocorre a transição.
Provas
Acerca da mudança de estado, das características e das propriedades e das ligações químicas nos sólidos, julgue o item seguinte.
Nos sólidos metálicos, os átomos compartilham uma nuvem de elétrons deslocalizados, sendo estes responsáveis pela elevada condutividade elétrica, pela maleabilidade e pela ductilidade desses materiais.
Provas
Acerca da mudança de estado, das características e das propriedades e das ligações químicas nos sólidos, julgue o item seguinte.
Sólidos moleculares são formados por moléculas unidas por forças intermoleculares, como interações de London, dipolo-dipolo ou ligações de hidrogênio, o que explica os seus altos pontos de fusão em comparação aos sólidos iônicos.
Provas
Acerca da mudança de estado, das características e das propriedades e das ligações químicas nos sólidos, julgue o item seguinte.
Uma mistura eutética comporta-se como uma substância pura durante a ebulição.
Provas
A respeito das leis ponderais, julgue o item a seguir.
Conforme o entendimento da lei de Dalton, dois elementos podem combinar-se formando mais de um composto, mantendo fixa a massa de um dos elementos, ao passo que a massa do outro se combine em proporções múltiplas e inteiras.
Provas
A respeito das leis ponderais, julgue o item a seguir.
Uma consequência importante do princípio estabelecido pela lei de Proust é a inalterabilidade da composição centesimal de um composto químico puro.
Provas
A respeito das leis ponderais, julgue o item a seguir.
Segundo a Lei de Lavoisier, em toda reação química conduzida em sistema fechado, pode ocorrer perda ou ganho de massa, uma vez que a energia liberada ou absorvida é sempre transformada em matéria.
Provas
Sabendo-se que, em soluções aquosas diluídas, 1 ppm equivale a 1 mg de soluto por litro de solução, que cálcio (Ca), estrôncio (Sr) e bário (Ba) são elementos que pertencem ao grupo 2A da tabela periódica, que o número atômico (Z) do carbono seja 6, que ZCa = 20, ZSr = 38 e ZBa = 56 e considerando que M CaCO3 = 100,1 g·mol-1 seja a massa molar do carbonato de cálcio, julgue o item a seguir.
O Ca(HCO₃)₂ corresponde a um sal ácido, ao passo que o CaCO₃ corresponde a um sal neutro.
Provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Sabendo-se que, em soluções aquosas diluídas, 1 ppm equivale a 1 mg de soluto por litro de solução, que cálcio (Ca), estrôncio (Sr) e bário (Ba) são elementos que pertencem ao grupo 2A da tabela periódica, que o número atômico (Z) do carbono seja 6, que ZCa = 20, ZSr = 38 e ZBa = 56 e considerando que M CaCO3 = 100,1 g·mol-1 seja a massa molar do carbonato de cálcio, julgue o item a seguir.
De acordo com a teoria da ligação de valência, o dióxido de carbono apresenta geometria linear, sendo que o átomo de carbono central se encontra em hibridização sp, formando as duas ligações duplas C=O.
Provas
Caderno Container