Foram encontradas 120 questões.
A rota sintética do composto alanina, preparada a partir do ácido 2-bromopropanoico, é representada pelo esquema a seguir.
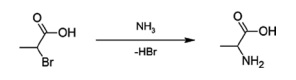
A partir dessas informações e supondo-se que uma solução foi preparada a partir de 0,89 g de alanina e 100 mL de água, e considerando-se que
No que se refere à síntese da alanina, é correto afirmar que se trata de uma reação de eliminação.
Provas
A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Um composto da classe peróxido de metal alcalino reage com água produzindo uma base e H2O2. Caso reaja com um ácido diluído, os produtos obtidos serão sal e H2O2.
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
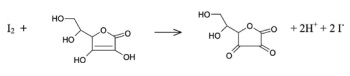
A vitamina C apresenta, em sua fórmula estrutural, os grupos funcionais correspondentes às funções álcool e éster cíclico.
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Assumindo-se que 1 mol de vitamina C é consumido para cada mol de H₂O₂, em uma solução contendo 0,0010 mol·L⁻¹ de C₆H₈O₆, se o tempo de reação for 20 segundos, então a velocidade média da reação, em relação à vitamina C, será inferior a 4,0 × 10⁻⁵ mol·L⁻¹·s⁻¹
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Se, a partir de uma solução de peróxido de hidrogênio a 30% (massa/massa), com densidade de 1,13 g/mL, for preparada uma solução a 3% (massa/massa), a concentração molar desta última será superior a 1,5 mol·L⁻¹.
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir
Compostos iônicos, como o KI, são sólidos nas condições ambiente e apresentam elevada temperatura de fusão e ebulição.
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
O raio atômico do átomo de iodo elementar é menor do que o raio do íon iodeto (I⁻).
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
A utilização de um catalisador provoca o aumento da entalpia de reação (ΔH), elevando a quantidade total de energia liberada ou absorvida.
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Na ausência do íon iodeto, que atua como catalisador, é esperado que a redução de H2O2 apresente uma energia de ativação menor do que a reação catalisada.
Provas

A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Suponha-se que, em um dos experimentos, tenham sido usados 10 mL de iodeto de potássio 0,28 mol/L. Nesse caso, é correto afirmar que, considerando-se dissociação completa, o número de íons iodeto é superior a 2,0 × 1021.
Provas
Caderno Container