Foram encontradas 796 questões.
Considerando as fórmulas químicas de ácidos, bases, óxidos e
sais, assinale a opção que apresenta apenas fórmulas de
compostos que podem ser obtidos em uma reação de
neutralização total.
Provas
Questão presente nas seguintes provas
Texto 10A2-II
O álcool estearílico é usado na indústria de cosméticos para a produção de cremes, loções, máscaras capilares, entre outros, por ser compatível com vários tipos de emulsionantes e apresentar baixa irritabilidade na pele.
Devido a um problema técnico em uma das indústrias de
produção desse insumo, esse produto passou a ficar escasso no
mercado, o que levou uma indústria de cosméticos a considerar o
estearato de metila como possível alternativa para a produção do
álcool estearílico, a partir da hidrogenação do estearato de metila,
em solução de heptano, por meio da seguinte reação.
C19H38O2 (sol) + 2 H2 (g) → C18H37OH (sol) + CH3OH (sol)
A planta piloto dessa indústria de cosméticos é equipada
com um reator do tipo autoclave, que opera em temperatura
máxima de 200 °C e pressão máxima de 1.000 psi e que pode ser
utilizado para desenvolver o projeto. Para que a síntese do álcool
estearílico seja bem-sucedida, o químico resolveu testar várias
condições reacionais, a fim de descobrir qual delas proporcionará
a obtenção de maior quantidade de álcool estearílico
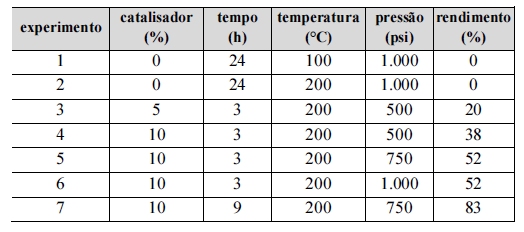
(rendimento) no menor tempo possível. Ele testou diversas
condições experimentais, tais como tempo de reação,
temperatura e pressão do reator, além de um catalisador
comercial à base de cobre. Os resultados dos testes são
mostrados na tabela a seguir. Sabe-se que o hidrogênio molecular
(H2) é instável a temperaturas acima de 200 °C.
Provas
Questão presente nas seguintes provas
Texto 10A2-I
A exposição à radiação ultravioleta pode causar queimadura na pele, lesão em células epiteliais, alteração do DNA, inflamação, dilatação dos vasos sanguíneos, câncer, entre outros fatores adversos. O ozônio (O3) existente na estratosfera atua como um filtro dos raios ultravioletas provenientes do Sol.
Antigamente, muitos sprays utilizavam
clorofluorcarbonos (CFCs) em sua composição. Esses CFCs
ficavam na atmosfera e reagiam com o ozônio, decompondo-o.
Em 1989, foi assinado um acordo internacional
denominado Protocolo de Montreal, por meio do qual mais de
130 países, incluído o Brasil, comprometeram-se a eliminar
progressivamente o uso dessas substâncias em sprays e outras
aplicações.
Um dos CFCs mais comuns possui fórmula CF2Cl2. Na
estratosfera, sob luz ultravioleta, ele sofre a seguinte reação.
CF2Cl2 → •CF2Cl + Cl•
O átomo livre de cloro (Cl•), por sua vez, pode
desencadear uma cascata de reações, como, por exemplo, as
apresentadas a seguir.
O3 (g) + Cl• (g) → O2 (g) + ClO• (g)
O3 (g) + ClO• (g) → 2 O2 (g) + Cl• (g)
Provas
Questão presente nas seguintes provas
A adrenalina, também conhecida como epinefrina, é um
hormônio liberado na corrente sanguínea que tem a função de
atuar sobre o sistema cardiovascular e manter o corpo em alerta
para situações de fortes emoções ou estresse, como luta, fuga,
excitação ou medo.
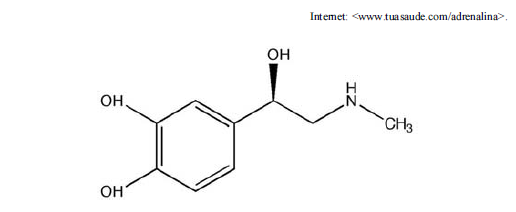
Considerando-se a fórmula estrutural da adrenalina, representada na figura precedente, é correto afirmar que o número de ligações sigma e pi presentes em uma molécula de adrenalina corresponde, respectivamente, a

Considerando-se a fórmula estrutural da adrenalina, representada na figura precedente, é correto afirmar que o número de ligações sigma e pi presentes em uma molécula de adrenalina corresponde, respectivamente, a
Provas
Questão presente nas seguintes provas
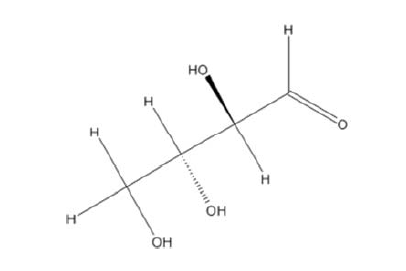
Considerando a estrutura química da D-eritrose, apresentada na figura anterior, assinale a opção que contém o número total de estereoisômeros para essa molécula orgânica.
Provas
Questão presente nas seguintes provas
A água do mar é um eletrólito, devido à alta concentração de sal,
e eletrólitos causam corrosão em metais. Cascos de navios
podem sofrer toda sorte de processos corrosivos eletroquímicos,
tais como aeração diferencial, corrosão atmosférica e corrosão
eletrolítica. A fim de evitar essa deterioração do casco, as
companhias navais utilizam revestimentos protetores, tais como
tintas, lacas, esmaltes, vernizes, resinas, dispersões, emulsões,
óleos protetores e recoberturas. Esses revestimentos protegem o
casco do navio porque
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
A figura a seguir mostra a estrutura química do
remdesivir, um profármaco de ação antiviral de amplo espectro,
com atividade in vitro observada contra diversos vírus de RNA,
tais como o ebola, o MERS-CoV e o SARS-CoV. Ele atua como
um inibidor de RNA polimerase dependente de RNA,
comprometendo o processo de replicação do genoma viral.
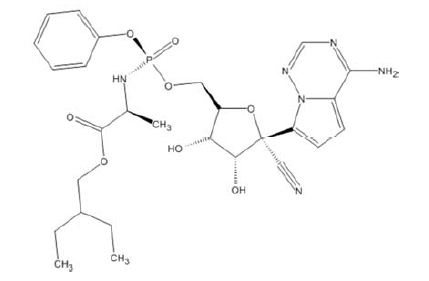
De acordo com a estrutura química apresentada, é correto afirmar que os grupos funcionais do remdesivir incluem

De acordo com a estrutura química apresentada, é correto afirmar que os grupos funcionais do remdesivir incluem
Provas
Questão presente nas seguintes provas
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
- Química OrgânicaReações OrgânicasReações Orgânicas: Substituição, Adição e Eliminação
Os primeiros sabões eram feitos com misturas de gorduras
de animais (sebo), como o material graxo, com as cinzas de
madeira, que possuem substâncias alcalinas, como o carbonato
de sódio e de potássio. A seguir, é apresentado um exemplo de
reação de saponificação.
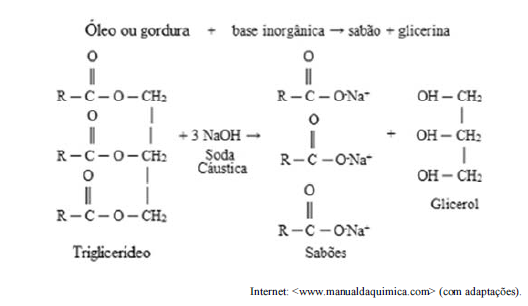
Com relação à reação de saponificação mostrada no texto anterior, assinale a opção correta.

Com relação à reação de saponificação mostrada no texto anterior, assinale a opção correta.
Provas
Questão presente nas seguintes provas
Texto 10A2-I
A exposição à radiação ultravioleta pode causar queimadura na pele, lesão em células epiteliais, alteração do DNA, inflamação, dilatação dos vasos sanguíneos, câncer, entre outros fatores adversos. O ozônio (O3) existente na estratosfera atua como um filtro dos raios ultravioletas provenientes do Sol.
Antigamente, muitos sprays utilizavam
clorofluorcarbonos (CFCs) em sua composição. Esses CFCs
ficavam na atmosfera e reagiam com o ozônio, decompondo-o.
Em 1989, foi assinado um acordo internacional
denominado Protocolo de Montreal, por meio do qual mais de
130 países, incluído o Brasil, comprometeram-se a eliminar
progressivamente o uso dessas substâncias em sprays e outras
aplicações.
Um dos CFCs mais comuns possui fórmula CF2Cl2. Na
estratosfera, sob luz ultravioleta, ele sofre a seguinte reação.
CF2Cl2 → •CF2Cl + Cl•
O átomo livre de cloro (Cl•), por sua vez, pode
desencadear uma cascata de reações, como, por exemplo, as
apresentadas a seguir.
O3 (g) + Cl• (g) → O2 (g) + ClO• (g)
O3 (g) + ClO• (g) → 2 O2 (g) + Cl• (g)
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A água e o ácido sulfídrico são moléculas semelhantes,
porque o oxigênio e o enxofre pertencem à mesma família da
Tabela Periódica; ambas as moléculas apresentam duas ligações
e geometria angular. Porém, as temperaturas de ebulição dessas
duas substâncias são muito diferentes, conforme demonstrado a
seguir.
TE (H2O) = +100 °C TE (H2S) = −60 °C
Essas diferenças entre as temperaturas de ebulição das substâncias podem ser explicadas pela(o)
TE (H2O) = +100 °C TE (H2S) = −60 °C
Essas diferenças entre as temperaturas de ebulição das substâncias podem ser explicadas pela(o)
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container