Foram encontradas 796 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A glicose (C6H12O6) é o principal carboidrato encontrado
no sangue. A taxa considerada normal é de 0,70 mg/mL a
1,10 mg/mL no sangue. Valores abaixo de 0,70 mg/mL
caracterizam uma pessoa com hipoglicemia e, quando esse
parâmetro é superior a 1,10 mg/mL, a pessoa está com
hiperglicemia.
A partir dessa informação, considere que uma pessoa com massa corporal de 70 kg tenha doado sangue em um hemocentro. Sabendo-se que M (C6H12O6) = 180 g/mol, que o volume retirado de sangue correspondeu a 9 mL/kg e que o nível de glicose nesse sangue é de 0,80 mg/mL, é correto afirmar que foram doados por este paciente
A partir dessa informação, considere que uma pessoa com massa corporal de 70 kg tenha doado sangue em um hemocentro. Sabendo-se que M (C6H12O6) = 180 g/mol, que o volume retirado de sangue correspondeu a 9 mL/kg e que o nível de glicose nesse sangue é de 0,80 mg/mL, é correto afirmar que foram doados por este paciente
Provas
Questão presente nas seguintes provas
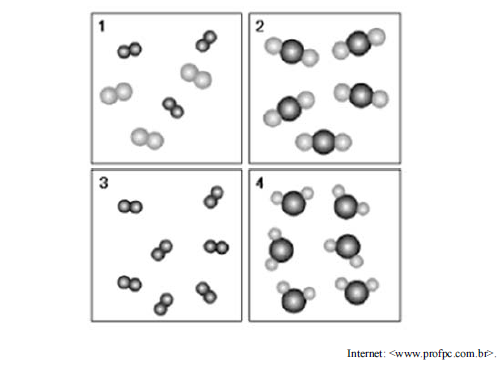
A figura precedente representa 4 sistemas formados por moléculas, em que bolinhas de cores diferentes representam átomos de elementos diferentes, e bolinhas juntas, que os átomos estão ligados entre si. Assinale a opção correta, de acordo com essa figura.
Provas
Questão presente nas seguintes provas
O gás NO reage com o gás O3 conforme a seguinte
equação.
NO (g) + O3 (g) ⇌ NO2 (g) + O2 (g)
Estudos mostraram que, quando esses dois gases são colocados em um mesmo recipiente a 25 °C e 1 atm, cada molécula colide, em média, cerca de um bilhão de vezes por segundo com outras moléculas. Se todas essas colisões resultassem em formação de produto, a reação aconteceria em uma fração de segundo. Porém, não é isso que se observa empiricamente, sendo a reação muitíssimo mais lenta.
Nesse caso, para que a reação aconteça, a simples colisão entre as moléculas não é suficiente; é necessário, também, que
NO (g) + O3 (g) ⇌ NO2 (g) + O2 (g)
Estudos mostraram que, quando esses dois gases são colocados em um mesmo recipiente a 25 °C e 1 atm, cada molécula colide, em média, cerca de um bilhão de vezes por segundo com outras moléculas. Se todas essas colisões resultassem em formação de produto, a reação aconteceria em uma fração de segundo. Porém, não é isso que se observa empiricamente, sendo a reação muitíssimo mais lenta.
Nesse caso, para que a reação aconteça, a simples colisão entre as moléculas não é suficiente; é necessário, também, que
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Os equilíbrios representados pelas reações a seguir
ocorrem quando o ácido fórmico (HCO2H) e a metilamina
(CH3NH2) se dissolvem em água.
reação 1: HCO2H (l) + H2O (l) ⇌ H3O+ (aq) + HCO2 – (aq) reação 2: CH3NH2 (l) + H2O (l) ⇌ CH3NH3 + (aq) + OH– (aq)
A partir dessas informações, assinale a opção que apresenta os pares conjugados ácido/base para as reações 1 e 2, respectivamente, considerando a reação direta, ou seja, o reagente ácido e sua respectiva base conjugada.
reação 1: HCO2H (l) + H2O (l) ⇌ H3O+ (aq) + HCO2 – (aq) reação 2: CH3NH2 (l) + H2O (l) ⇌ CH3NH3 + (aq) + OH– (aq)
A partir dessas informações, assinale a opção que apresenta os pares conjugados ácido/base para as reações 1 e 2, respectivamente, considerando a reação direta, ou seja, o reagente ácido e sua respectiva base conjugada.
Provas
Questão presente nas seguintes provas
A festa da virada de ano (réveillon) é marcada pela queima de
fogos de artifício. No Brasil, o maior espetáculo acontece na
praia de Copacabana, no Rio de Janeiro, mas este ano o evento
foi cancelado por causa da pandemia. A explosão de cores no céu
causada pela queima dos fogos é decorrente de um fenômeno que
acontece com os elétrons dentro dos átomos, que, por sua vez,
pode ser explicado pelo modelo atômico de Bohr que
Provas
Questão presente nas seguintes provas
Texto 10A2-II
O álcool estearílico é usado na indústria de cosméticos para a produção de cremes, loções, máscaras capilares, entre outros, por ser compatível com vários tipos de emulsionantes e apresentar baixa irritabilidade na pele.
Devido a um problema técnico em uma das indústrias de
produção desse insumo, esse produto passou a ficar escasso no
mercado, o que levou uma indústria de cosméticos a considerar o
estearato de metila como possível alternativa para a produção do
álcool estearílico, a partir da hidrogenação do estearato de metila,
em solução de heptano, por meio da seguinte reação.
C19H38O2 (sol) + 2 H2 (g) → C18H37OH (sol) + CH3OH (sol)
A planta piloto dessa indústria de cosméticos é equipada
com um reator do tipo autoclave, que opera em temperatura
máxima de 200 °C e pressão máxima de 1.000 psi e que pode ser
utilizado para desenvolver o projeto. Para que a síntese do álcool
estearílico seja bem-sucedida, o químico resolveu testar várias
condições reacionais, a fim de descobrir qual delas proporcionará
a obtenção de maior quantidade de álcool estearílico
(rendimento) no menor tempo possível. Ele testou diversas
condições experimentais, tais como tempo de reação,
temperatura e pressão do reator, além de um catalisador
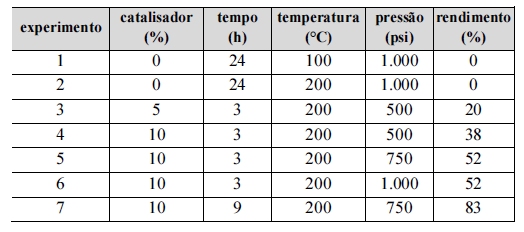
comercial à base de cobre. Os resultados dos testes são
mostrados na tabela a seguir. Sabe-se que o hidrogênio molecular
(H2) é instável a temperaturas acima de 200 °C.
Provas
Questão presente nas seguintes provas
Em uma solução ácida,
Provas
Questão presente nas seguintes provas
As substâncias A, B e C reagem entre si, produzindo as
substâncias D e E. A velocidade inicial dessa reação foi medida
para várias concentrações iniciais de A, B e C, à temperatura
constante, e os resultados obtidos são os mostrados na seguinte
tabela.
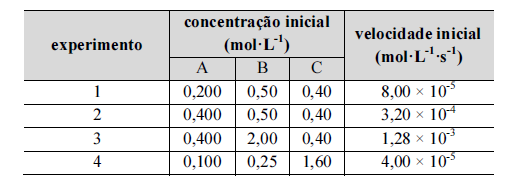
Com relação à situação hipotética precedente, assumindo-se v como a velocidade da reação e k como a constante de velocidade, é correto afirmar que a lei de velocidade dessa reação é dada por

Com relação à situação hipotética precedente, assumindo-se v como a velocidade da reação e k como a constante de velocidade, é correto afirmar que a lei de velocidade dessa reação é dada por
Provas
Questão presente nas seguintes provas
A Tabela Periódica aumenta sua família de elementos
com quatro nomes adicionais. Em sua sétima fila, foram
incluídos oficialmente quatro novos inquilinos: os elementos
113, 115, 117 e 118 foram batizados como nihônio, moscóvio,
tennessino e oganessono, respectivamente. O primeiro deles foi
descoberto por cientistas do Instituto Riken no Japão; os outros,
por equipes de cientistas da Rússia e dos Estados Unidos, todos
eles integrados à Tabela Periódica desde janeiro.
Internet: <brasil.elpais.com> (com adaptações).
A esse respeito, assinale a opção correta.
Internet: <brasil.elpais.com> (com adaptações).
A esse respeito, assinale a opção correta.
Provas
Questão presente nas seguintes provas
Os modelos atômicos tentam explicar como é a estrutura de um
átomo, já que este é uma partícula muito pequena que não pode
ser vista a olho nu. Até hoje, os cientistas não conseguiram ver
um átomo isolado, muito menos a sua estrutura interna, mas os
modelos tentam recriar este átomo. Nesse contexto, o modelo
atômico de
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container