Foram encontradas 40 questões.
Para preparar 250 mL de uma solução 0,1 mol . L-1 de HCl a partir do estoque de ácido concentrado (37% massa/massa, densidade de 1,19 g . mL-1), o volume necessário de HCl será de: (Expresse o resultado em mililitro, com uma casa após a vírgula e com arredondamento.)
Provas
A imagem mostra as variações de entalpia que acompanham o processo de formação de uma solução; observe.
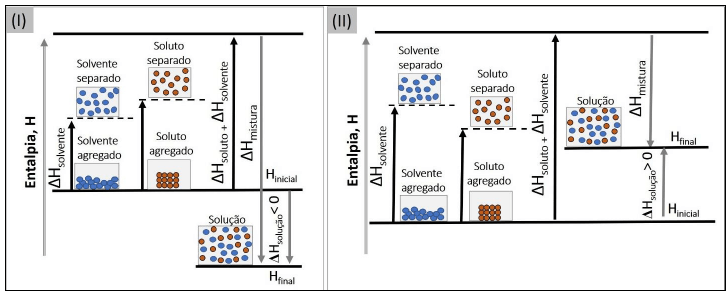
Dados: NaCl ΔHsolução= 3,9 kJ . mol-1; MgSO4 ΔHsolução= –91,2 kJ . mol-1; NH4NO3 ΔHsolução= 26,4 kJ . mol-1.
Considerando a imagem, os dados fornecidos e os conceitos relacionados ao tema, assinale a afirmativa correta.
Provas
Sobre os conceitos de solubilidade envolvidos na equação química representada, assinale a afirmativa correta.

Provas
Considere a reação 2A(aq)→ B2(aq) + C(aq) e os dados empíricos das velocidades iniciais para diferentes concentrações do reagente A mostrados na Tabela:
| [A] mol . L-1 | Velocidade mol . L-1 . s-1 |
| 0,1 | 0,2 |
| 0,2 | 0,2 |
| 0,4 | 0,2 |
A partir das informações, a Lei de Velocidade para esta reação será de:
Provas
Os conceitos de solubilidade molar e solubilidade são amplamente utilizados em laboratórios de química, biologia e farmácia. A solubilidade do sulfato de cálcio (massa molar 136,2 g . mol-1) é 0,67 g . L-1 e sua solubilidade molar é de 4,9 x 10-3 mol . L-1 (dados a 25° C). O produto de solubilidade do sal será de:
Provas
Considere que 2 g de determinado açúcar tenha sido queimado em uma bomba calorimétrica previamente calibrada. Em consequência, a temperatura da água aumentou de 21,0 °C para 26,2 °C. A capacidade calorífica do calorímetro é de 551 J . °C-1 e a reação aconteceu em excesso de oxigênio. Considerando a calorimetria a volume constante, o valor da energia interna por grama de açúcar (resultado expresso em Joule e em número inteiro) será de:
Provas
Certa reação química, ocorrida em pressão atmosférica, apresentou as seguintes variações termodinâmicas: 55 kJ . mol-1 de energia deixou o sistema na forma de calor (Q) e 15 kJ . mol-1 deixou o sistema na forma de trabalho (W) de expansão. Considerando os dados fornecidos sobre o sistema, assinale a afirmativa correta.
Provas
Os elementos radioativos, muito utilizados na medicina como ferramenta de diagnóstico e como meio de tratamento, especialmente para o câncer, são usados, também, para ajudar a determinar os mecanismos de reações químicas, investigar o movimento de átomos em sistemas biológicos e achar a idade de importantes artefatos históricos. As reações nucleares são empregadas tanto para gerar eletricidade quanto para criar armas de destruição em massa. Sobre radioatividade, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A radiação gama consiste em fótons de alta energia e não muda o número atômico nem a massa atômica de um núcleo.
( ) Quanto menor a energia de coesão, mais estável é o núcleo no sentido da decomposição.
( ) Os núcleos 2He4, 20Ca40 e 43Tc98 exibem estabilidade.
( ) O produto formado quando o rádio-226 sofre decaimento alfa é 86 Rn222.
A sequência está correta em
Provas
O mol é uma unidade de medida utilizada para expressar a quantidade microscópica, como átomos e moléculas. No século XX, após estudos do químico Francis Perrin é que os cientistas conseguiram determinar qual a quantidade de matéria presente em um mol. Um laboratório com menores amostras trabalha com quantidade de mol. Os profissionais que trabalham com aviação também utilizam cálculos que incluem conceito de mol para determinar a quantidade de combustível necessária para transportar passageiros em segurança. Sobre o mol, analise as afirmativas a seguir.
I. Existem 2,53 x 1024 átomos de H em 0,350 mol de C6H12O6.
II. Em uma molécula de tetracloreto de carbono existem 1,02 x 10-22 g.
III. São produzidas 0,3 g de água na oxidação de 1 g de glicose – C6H12O6.
Está correto o que se afirma apenas em
Provas
A estequiometria, nome derivado das palavras gregas stoicheion e metron, é uma ferramenta essencial na química. É imprescindível, principalmente na indústria, para o cálculo do rendimento dos processos industriais e da quantidade de reagentes necessária para atingir as expectativas de produção. Para isso, é necessário conhecer as equações que representam as reações químicas envolvidas. Sobre os cálculos estequiométricos, analise as afirmativas a seguir.
I. Quando o sulfeto de chumbo e o óxido de chumbo são aquecidos juntos, os produtos são chumbo metálico e dióxido de enxofre. Se 14 g de óxido de chumbo reagem, forma-se 9,42 x 10-2 mol de átomos de chumbo.
II. O mais importante processo comercial para converter N2 do ar em compostos contendo nitrogênio é baseado na reação de N2 e H2 para formar NH3. São formadas 4 mols de NH3 a partir de 3 mols de N2 e 6 mols de H2.
III. Xileno é uma substância composta somente de carbono e hidrogênio. Uma amostra de xileno foi queimada em excesso de oxigênio e este produziu somente como produtos 33,4 g de CO2 e 8,55 g de água. A fórmula empírica do xileno é C4H5.
Está correto o que se afirma em
Provas
Caderno Container