Foram encontradas 792 questões.
O diagrama mostra os caminhos e suas respectivas entalpias-padrão (a 298 K) para a conversão do carbono e do oxigênio em dióxido de carbono; observe.
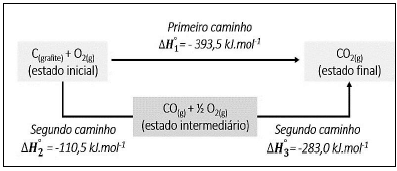
Considerando o diagrama e os conceitos termodinâmicos de uma forma geral, assinale a afirmativa correta.
Provas
Considere a reação de formação da amônia, estudada pelo químico alemão Fritz Haber.
N2(g) + H2(g) ⇌ NH3(g)
Considerando, ainda, as propriedades do equilíbrio químico citado, assinale a afirmativa correta.
Provas
Para preparar 250 mL de uma solução 0,1 mol . L-1 de HCl a partir do estoque de ácido concentrado (37% massa/massa, densidade de 1,19 g . mL-1), o volume necessário de HCl será de: (Expresse o resultado em mililitro, com uma casa após a vírgula e com arredondamento.)
Provas
A imagem mostra as variações de entalpia que acompanham o processo de formação de uma solução; observe.
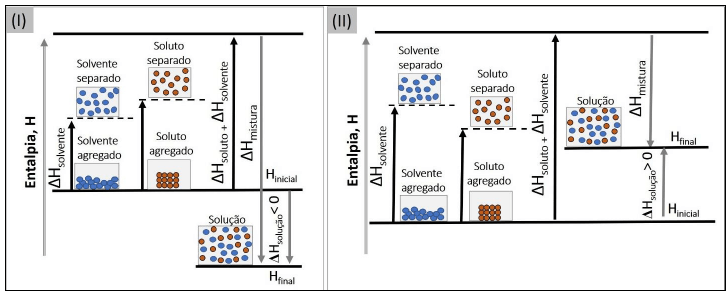
Dados: NaCl ΔHsolução= 3,9 kJ . mol-1; MgSO4 ΔHsolução= –91,2 kJ . mol-1; NH4NO3 ΔHsolução= 26,4 kJ . mol-1.
Considerando a imagem, os dados fornecidos e os conceitos relacionados ao tema, assinale a afirmativa correta.
Provas
Sobre os conceitos de solubilidade envolvidos na equação química representada, assinale a afirmativa correta.

Provas
Considere a reação 2A(aq)→ B2(aq) + C(aq) e os dados empíricos das velocidades iniciais para diferentes concentrações do reagente A mostrados na Tabela:
| [A] mol . L-1 | Velocidade mol . L-1 . s-1 |
| 0,1 | 0,2 |
| 0,2 | 0,2 |
| 0,4 | 0,2 |
A partir das informações, a Lei de Velocidade para esta reação será de:
Provas
Os conceitos de solubilidade molar e solubilidade são amplamente utilizados em laboratórios de química, biologia e farmácia. A solubilidade do sulfato de cálcio (massa molar 136,2 g . mol-1) é 0,67 g . L-1 e sua solubilidade molar é de 4,9 x 10-3 mol . L-1 (dados a 25° C). O produto de solubilidade do sal será de:
Provas
Considere que 2 g de determinado açúcar tenha sido queimado em uma bomba calorimétrica previamente calibrada. Em consequência, a temperatura da água aumentou de 21,0 °C para 26,2 °C. A capacidade calorífica do calorímetro é de 551 J . °C-1 e a reação aconteceu em excesso de oxigênio. Considerando a calorimetria a volume constante, o valor da energia interna por grama de açúcar (resultado expresso em Joule e em número inteiro) será de:
Provas
Certa reação química, ocorrida em pressão atmosférica, apresentou as seguintes variações termodinâmicas: 55 kJ . mol-1 de energia deixou o sistema na forma de calor (Q) e 15 kJ . mol-1 deixou o sistema na forma de trabalho (W) de expansão. Considerando os dados fornecidos sobre o sistema, assinale a afirmativa correta.
Provas
Os elementos radioativos, muito utilizados na medicina como ferramenta de diagnóstico e como meio de tratamento, especialmente para o câncer, são usados, também, para ajudar a determinar os mecanismos de reações químicas, investigar o movimento de átomos em sistemas biológicos e achar a idade de importantes artefatos históricos. As reações nucleares são empregadas tanto para gerar eletricidade quanto para criar armas de destruição em massa. Sobre radioatividade, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A radiação gama consiste em fótons de alta energia e não muda o número atômico nem a massa atômica de um núcleo.
( ) Quanto menor a energia de coesão, mais estável é o núcleo no sentido da decomposição.
( ) Os núcleos 2He4, 20Ca40 e 43Tc98 exibem estabilidade.
( ) O produto formado quando o rádio-226 sofre decaimento alfa é 86 Rn222.
A sequência está correta em
Provas
Caderno Container