Foram encontradas 70 questões.
Na análise da absorção de um soluto (diluído), absorvido
da fase gasosa para a fase líquida (solvente), estima-se a
altura da torre l (em m) como:
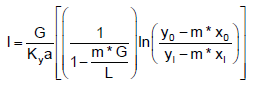
tal que G e L são, respectivamente, as vazões molares de gás e líquido por unidade de área (em kgmol/sm2); m* é a constante de equilíbrio; Ky a é o coeficiente global de transferência de massa vezes a área por volume (em kgmol/sm); y0 e yl são as frações molares do soluto no gás na entrada e na saída da torre, respectivamente, e x0 e xl são as frações molares do soluto no solvente na saída e na entrada da torre, respectivamente.
Para um dado problema, os valores numéricos (no sistema SI) são conhecidos, e os termos da equação acima foram calculados, aproximadamente, como:
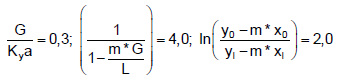
tal que as unidades (quando há) foram omitidas aqui propositadamente.
Usando-se o conceito da literatura de “número de unidades de transferência” (NTU) e “altura de uma unidade de transferência” (HTU), tem-se, nesse caso:
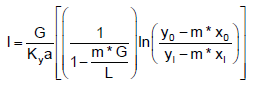
tal que G e L são, respectivamente, as vazões molares de gás e líquido por unidade de área (em kgmol/sm2); m* é a constante de equilíbrio; Ky a é o coeficiente global de transferência de massa vezes a área por volume (em kgmol/sm); y0 e yl são as frações molares do soluto no gás na entrada e na saída da torre, respectivamente, e x0 e xl são as frações molares do soluto no solvente na saída e na entrada da torre, respectivamente.
Para um dado problema, os valores numéricos (no sistema SI) são conhecidos, e os termos da equação acima foram calculados, aproximadamente, como:
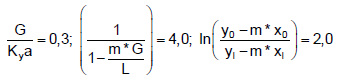
tal que as unidades (quando há) foram omitidas aqui propositadamente.
Usando-se o conceito da literatura de “número de unidades de transferência” (NTU) e “altura de uma unidade de transferência” (HTU), tem-se, nesse caso:
Provas
Questão presente nas seguintes provas
Uma mistura gasosa de hidrocarbonetos é formada por
0,4 mol de CH4, 0,7 mol de C2H6
e 0,9 mol de C3H8
. Essa
mistura se encontra em um reservatório sob pressão total
de 200 kPa.
A pressão parcial de CH4 nessa mistura é igual a
A pressão parcial de CH4 nessa mistura é igual a
Provas
Questão presente nas seguintes provas
Uma indústria de produtos alimentícios possui um reator
do tipo CSTR em um processo de mistura intensa. A
função desse reator é processar a reação de hidrólise do
anidrido acético (1a
ordem em anidrido) com excesso de
água a 25 °C e 1 atm. Essa reação está expressa abaixo:
C4H6O3 + H2 O → 2 CH3COOH
A reação deverá produzir 20 kg/h de ácido acético, a constante de velocidade é aproximadamente 0,05 min-1 , a concentração inicial de anidrido acético é de 100 g/L, e a conversão, de 80%.
O volume aproximado, em litros, desse reator é
Dados Massa Molar do Ácido Acético (CH3COOH) = 60 g/mol Massa Molar do Anidrido Acético (C4H6O3 ) = 102 g/mol
C4H6O3 + H2 O → 2 CH3COOH
A reação deverá produzir 20 kg/h de ácido acético, a constante de velocidade é aproximadamente 0,05 min-1 , a concentração inicial de anidrido acético é de 100 g/L, e a conversão, de 80%.
O volume aproximado, em litros, desse reator é
Dados Massa Molar do Ácido Acético (CH3COOH) = 60 g/mol Massa Molar do Anidrido Acético (C4H6O3 ) = 102 g/mol
Provas
Questão presente nas seguintes provas
Considere que foi desenvolvido um modelo empírico, relacionando-se dados experimentais de vazão volumétrica, q, de um
líquido através de uma válvula e a diferença entre as pressões a montante, P1, e a jusante da mesma, P2, tal que:
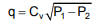
em que a constante Cv foi estimada por regressão não linear.
Considerando-se as três dimensões fundamentais MLt, a dimensão de Cv para consistência dimensional é
em que a constante Cv foi estimada por regressão não linear.
Considerando-se as três dimensões fundamentais MLt, a dimensão de Cv para consistência dimensional é
Provas
Questão presente nas seguintes provas
A formação do trióxido de enxofre (SO3(g)) ocorre a partir
da oxidação do dióxido de enxofre (SO2(g)), reagindo com
oxigênio (O2(g)) a temperatura de 960K e a constante de
equilíbrio nesta temperatura de Kp=10.
A energia de Gibbs nessas condições, em KJmol-1, é
Dado Pressões parciais, em bar, do SO2(g), O2(g), SO3(g), respectivamente, 10-3, 0,20, 10-4. Constante dos gases, R = 8,314 J.-1 .mol-1; Logaritmo Neperiano, ln(5)=1,609; ln(10)=2,303.
A energia de Gibbs nessas condições, em KJmol-1, é
Dado Pressões parciais, em bar, do SO2(g), O2(g), SO3(g), respectivamente, 10-3, 0,20, 10-4. Constante dos gases, R = 8,314 J.-1 .mol-1; Logaritmo Neperiano, ln(5)=1,609; ln(10)=2,303.
Provas
Questão presente nas seguintes provas
Um sistema formado por CO2
saturado com vapor d’água
apresenta pressão total de 100 kPa a 363 K. Nessa temperatura, a pressão de vapor da água é 70 kPa.
A fração molar do CO2 na mistura é igual a
A fração molar do CO2 na mistura é igual a
Provas
Questão presente nas seguintes provas
A reação elementar A → B ocorre em um reator tubular
(PFR – reator com escoamento uniforme), representado pela Figura abaixo, com uma vazão volumétrica de
entrada de 6 L/min. A velocidade específica de reação
é 0,25 min-1.

O volume do reator necessário para reduzir a concentração de saída a 20% da concentração de entrada é, aproximadamente,
Dado In 0,2 = -1,609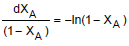

O volume do reator necessário para reduzir a concentração de saída a 20% da concentração de entrada é, aproximadamente,
Dado In 0,2 = -1,609
Provas
Questão presente nas seguintes provas
A Equação de Arrhenius, k = k0
exp(-E/RT), pode ser escrita na forma logarítmica gerando a expressão ln k = ln k0
– E/RT. Os
dados apresentados na Tabela a seguir referem-se à reação 2A → 2B + C.
T (°C) T (K) K (L mol-1 s-1) ln k 161,63 434,78 148,42 5,00 104,20 377,35 1 0 60,18 333,33 0,0067 -5,0
A partir desses dados plotados na Figura abaixo, calcula-se a Energia de Ativação desta reação.
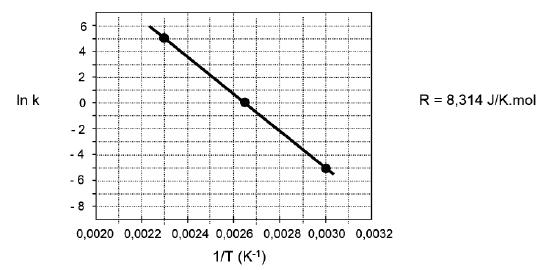
O valor da Energia de Ativação expresso em Joules/mol é
T (°C) T (K) K (L mol-1 s-1) ln k 161,63 434,78 148,42 5,00 104,20 377,35 1 0 60,18 333,33 0,0067 -5,0
A partir desses dados plotados na Figura abaixo, calcula-se a Energia de Ativação desta reação.

O valor da Energia de Ativação expresso em Joules/mol é
Provas
Questão presente nas seguintes provas
Um sistema de segunda ordem, cuja função de transferência é representada abaixo, possui frequência amortecida e tempo de pico iguais a 6 rad/s e 0,5236 s, respectivamente.
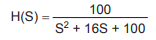
Qual o valor do tempo de acomodação do sistema para o critério de 2%?
Qual o valor do tempo de acomodação do sistema para o critério de 2%?
Provas
Questão presente nas seguintes provas
Um engenheiro precisa selecionar um trocador de calor
de escoamento em passe único capaz de resfriar óleo de
máquina de 70 ºC para 50 ºC e com carga térmica de projeto igual a 150 kW. Outra exigência do projeto é que a
temperatura do fluido de resfriamento (água) deve variar
de 20 ºC até 40 ºC.
Considerando-se as possibilidades de adoção de um trocador de contracorrente, qual a área de superfície de transferência de calor desse trocador?
Dado Coeficiente de transferência de calor global médio igual a 100 W/(m2.ºC).
Considerando-se as possibilidades de adoção de um trocador de contracorrente, qual a área de superfície de transferência de calor desse trocador?
Dado Coeficiente de transferência de calor global médio igual a 100 W/(m2.ºC).
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container