Foram encontradas 60 questões.
Uma forma de avaliar a estabilidade de um alceno é através da determinação de sua entalpia-padrão de hidrogenação. Quanto menor a energia liberada nessa reação,
maior a estabilidade do alceno.
Na Tabela a seguir, são apresentados três alcenos isômeros.
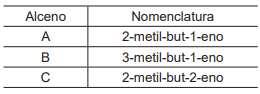
A representação em ordem crescente de energia liberada na combustão de 1 mol do alceno é a seguinte
Na Tabela a seguir, são apresentados três alcenos isômeros.

A representação em ordem crescente de energia liberada na combustão de 1 mol do alceno é a seguinte
Provas
Questão presente nas seguintes provas
Um processo industrial para a obtenção de etanol consiste na reação de adição entre eteno e água. Os valores de
energia de ligação referentes a esses compostos estão
representados a seguir.

A variação de entalpia, em kJ mol-1 , da reação correspondente a esse processo industrial é

A variação de entalpia, em kJ mol-1 , da reação correspondente a esse processo industrial é
Provas
Questão presente nas seguintes provas
Considere as duas semirreações e seus respectivos potenciais-padrão de redução que envolvem íons de halogênios, na
formação de uma pilha.
BrO3 - (aq) + 6 H+ (aq) + 6 e- → Br- (aq) + 3 H2 O (l) Eo red = +1,44 V
I2 (s) + 2 e- → 2 I- (aq) Eº red = +0,54 V
Em relação à pilha formada, observa-se que
BrO3 - (aq) + 6 H+ (aq) + 6 e- → Br- (aq) + 3 H2 O (l) Eo red = +1,44 V
I2 (s) + 2 e- → 2 I- (aq) Eº red = +0,54 V
Em relação à pilha formada, observa-se que
Provas
Questão presente nas seguintes provas
Algumas reações químicas envolvidas no processo de formação de gás de síntese são representadas pelas equações
termoquímicas a seguir.
I - C (s) + H2 O (v) → CO (g) + H2 (g) ∆H° = -28.000 cal mol-1 II - CO (g) + H2 O (v) → CO2 (g) + H2 (g) ∆H° = +9.400 cal mol-1 III - C (s) + 2 H2 O (v) → CO2 (g) + 2 H2 (g)
Considerando-se essas informações, a variação de entalpia, em cal mol-1 , da equação termoquímica III é
I - C (s) + H2 O (v) → CO (g) + H2 (g) ∆H° = -28.000 cal mol-1 II - CO (g) + H2 O (v) → CO2 (g) + H2 (g) ∆H° = +9.400 cal mol-1 III - C (s) + 2 H2 O (v) → CO2 (g) + 2 H2 (g)
Considerando-se essas informações, a variação de entalpia, em cal mol-1 , da equação termoquímica III é
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A análise gravimétrica de magnésio presente em uma
amostra, correspondente a 200,0 mL de solução aquosa
desse metal, seguiu as seguintes etapas:
A amostra reagiu com uma solução de íons oxalato em excesso, acarretando a precipitação de MgC2 O4 , conforme apresentado na reação I. Considere que o magnésio foi o único componente da amostra a precipitar.
Em seguida, o precipitado foi filtrado, lavado e calcinado (reação II), gerando uma amostra sólida de 3,05 g.
Reação I: Mg2+ (aq) + C2 O4 2- (aq) → MgC2 O4 (s)
Reação II: MgC2 O4 (s) → MgO (s) + CO (g) + CO2 (g)
A concentração, em g L-1, de magnésio na amostra é
Dado massas molares: Mg = 24 g mol-1 , O = 16 g mol-1 , C = 12 g mol-1
A amostra reagiu com uma solução de íons oxalato em excesso, acarretando a precipitação de MgC2 O4 , conforme apresentado na reação I. Considere que o magnésio foi o único componente da amostra a precipitar.
Em seguida, o precipitado foi filtrado, lavado e calcinado (reação II), gerando uma amostra sólida de 3,05 g.
Reação I: Mg2+ (aq) + C2 O4 2- (aq) → MgC2 O4 (s)
Reação II: MgC2 O4 (s) → MgO (s) + CO (g) + CO2 (g)
A concentração, em g L-1, de magnésio na amostra é
Dado massas molares: Mg = 24 g mol-1 , O = 16 g mol-1 , C = 12 g mol-1
Provas
Questão presente nas seguintes provas
A reação química entre clorometano e a solução aquosa
de NaOH a 60°C corresponde a uma reação de substituição.
A ordem global dessa reação e o principal produto orgânico formado são
A ordem global dessa reação e o principal produto orgânico formado são
Provas
Questão presente nas seguintes provas
Em uma célula eletrolítica, é realizada a eletrólise de uma
solução aquosa de iodeto de potássio.
Nessa eletrólise, a substância simples formada no catodo é
Nessa eletrólise, a substância simples formada no catodo é
Provas
Questão presente nas seguintes provas
Um determinado processo acarreta a liberação de dióxido
de enxofre para a atmosfera. Na atmosfera, esse composto reage com o gás oxigênio e com o vapor d’água
formando um ácido inorgânico forte.
A fórmula molecular desse ácido é
A fórmula molecular desse ácido é
Provas
Questão presente nas seguintes provas
A análise dos componentes presentes em um depósito
salino indicou a presença de nitrato de bário.
A fórmula química desse sal é
A fórmula química desse sal é
Provas
Questão presente nas seguintes provas
O 2-metil-pent-1-eno foi submetido a duas reações distintas. A primeira consistiu na reação desse composto com
KMnO4
em meio básico sob aquecimento, com posterior
acidificação. Na segunda reação, o 2-metil-pent-1-eno
foi submetido à reação com ozônio e posterior adição de
zinco e ácido acético.
Quando se compararam os produtos obtidos em ambas as reações, constatou-se a formação de
Quando se compararam os produtos obtidos em ambas as reações, constatou-se a formação de
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container