Foram encontradas 540 questões.
Todo processo de transformação do estado de uma determinada substância em uma cadeia de processamento,
para a composição de um produto final, envolve operações que necessitam de controle, a fim de manter algumas grandezas dentro de valores pré-estabelecidos. A vazão é uma das principais variáveis desse tipo de processo
e pode ser medida utilizando-se um medidor de vazão
por área variável, no qual um flutuador varia sua posição
dentro de um tubo cônico, proporcionalmente à vazão do
fluido.
Esse tipo de medidor é denominado
Esse tipo de medidor é denominado
Provas
Questão presente nas seguintes provas
Em refinarias de petróleo, alcenos podem ser preparados
por meio da quebra de moléculas de alcanos com cadeias
longas, através do processo de craqueamento. A equação
a seguir representa uma possibilidade de obtenção de um
alceno a partir do craqueamento de um alcano de cadeia
longa com fórmula molecular de C22H46 .
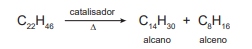
Ao se partir do alcano C30H62 , com formação de um alcano C12H26, a fórmula molecular do alceno produzido será
Ao se partir do alcano C30H62 , com formação de um alcano C12H26, a fórmula molecular do alceno produzido será
Provas
Questão presente nas seguintes provas
- Química OrgânicaIsomeria Plana e Espacial
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
- Química OrgânicaReações OrgânicasReações Orgânicas: Substituição, Adição e Eliminação
O reagente de Tollens é frequentemente usado em testes para identificar a presença de um grupo funcional em
compostos orgânicos.
O grupo funcional detectado pelo teste com o reagente de Tollens e o resultado esperado dessa reação são os(as)
O grupo funcional detectado pelo teste com o reagente de Tollens e o resultado esperado dessa reação são os(as)
Provas
Questão presente nas seguintes provas
Uma forma de avaliar a estabilidade de um alceno é através da determinação de sua entalpia-padrão de hidrogenação. Quanto menor a energia liberada nessa reação,
maior a estabilidade do alceno.
Na Tabela a seguir, são apresentados três alcenos isômeros.
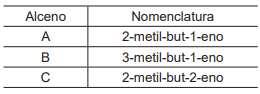
A representação em ordem crescente de energia liberada na combustão de 1 mol do alceno é a seguinte
Na Tabela a seguir, são apresentados três alcenos isômeros.

A representação em ordem crescente de energia liberada na combustão de 1 mol do alceno é a seguinte
Provas
Questão presente nas seguintes provas
Um processo industrial para a obtenção de etanol consiste na reação de adição entre eteno e água. Os valores de
energia de ligação referentes a esses compostos estão
representados a seguir.

A variação de entalpia, em kJ mol-1 , da reação correspondente a esse processo industrial é

A variação de entalpia, em kJ mol-1 , da reação correspondente a esse processo industrial é
Provas
Questão presente nas seguintes provas
Considere as duas semirreações e seus respectivos potenciais-padrão de redução que envolvem íons de halogênios, na
formação de uma pilha.
BrO3 - (aq) + 6 H+ (aq) + 6 e- → Br- (aq) + 3 H2 O (l) Eo red = +1,44 V
I2 (s) + 2 e- → 2 I- (aq) Eº red = +0,54 V
Em relação à pilha formada, observa-se que
BrO3 - (aq) + 6 H+ (aq) + 6 e- → Br- (aq) + 3 H2 O (l) Eo red = +1,44 V
I2 (s) + 2 e- → 2 I- (aq) Eº red = +0,54 V
Em relação à pilha formada, observa-se que
Provas
Questão presente nas seguintes provas
Algumas reações químicas envolvidas no processo de formação de gás de síntese são representadas pelas equações
termoquímicas a seguir.
I - C (s) + H2 O (v) → CO (g) + H2 (g) ∆H° = -28.000 cal mol-1 II - CO (g) + H2 O (v) → CO2 (g) + H2 (g) ∆H° = +9.400 cal mol-1 III - C (s) + 2 H2 O (v) → CO2 (g) + 2 H2 (g)
Considerando-se essas informações, a variação de entalpia, em cal mol-1 , da equação termoquímica III é
I - C (s) + H2 O (v) → CO (g) + H2 (g) ∆H° = -28.000 cal mol-1 II - CO (g) + H2 O (v) → CO2 (g) + H2 (g) ∆H° = +9.400 cal mol-1 III - C (s) + 2 H2 O (v) → CO2 (g) + 2 H2 (g)
Considerando-se essas informações, a variação de entalpia, em cal mol-1 , da equação termoquímica III é
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A análise gravimétrica de magnésio presente em uma
amostra, correspondente a 200,0 mL de solução aquosa
desse metal, seguiu as seguintes etapas:
A amostra reagiu com uma solução de íons oxalato em excesso, acarretando a precipitação de MgC2 O4 , conforme apresentado na reação I. Considere que o magnésio foi o único componente da amostra a precipitar.
Em seguida, o precipitado foi filtrado, lavado e calcinado (reação II), gerando uma amostra sólida de 3,05 g.
Reação I: Mg2+ (aq) + C2 O4 2- (aq) → MgC2 O4 (s)
Reação II: MgC2 O4 (s) → MgO (s) + CO (g) + CO2 (g)
A concentração, em g L-1, de magnésio na amostra é
Dado massas molares: Mg = 24 g mol-1 , O = 16 g mol-1 , C = 12 g mol-1
A amostra reagiu com uma solução de íons oxalato em excesso, acarretando a precipitação de MgC2 O4 , conforme apresentado na reação I. Considere que o magnésio foi o único componente da amostra a precipitar.
Em seguida, o precipitado foi filtrado, lavado e calcinado (reação II), gerando uma amostra sólida de 3,05 g.
Reação I: Mg2+ (aq) + C2 O4 2- (aq) → MgC2 O4 (s)
Reação II: MgC2 O4 (s) → MgO (s) + CO (g) + CO2 (g)
A concentração, em g L-1, de magnésio na amostra é
Dado massas molares: Mg = 24 g mol-1 , O = 16 g mol-1 , C = 12 g mol-1
Provas
Questão presente nas seguintes provas
A reação química entre clorometano e a solução aquosa
de NaOH a 60°C corresponde a uma reação de substituição.
A ordem global dessa reação e o principal produto orgânico formado são
A ordem global dessa reação e o principal produto orgânico formado são
Provas
Questão presente nas seguintes provas
Em uma célula eletrolítica, é realizada a eletrólise de uma
solução aquosa de iodeto de potássio.
Nessa eletrólise, a substância simples formada no catodo é
Nessa eletrólise, a substância simples formada no catodo é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container