Foram encontradas 600 questões.
Observação: Caso necessário, utilize a Tabela Periódica.
O teste de chama é um experimento clássico de laboratório utilizado para exemplificar a identificação de alguns elementos químicos por meio da emissão de uma luz característica. Portanto, o teste de chama é um exemplo de técnica espectroscópica baseada nas transições de estados energéticos do tipo:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
Em laboratórios de química existe o risco de acidente em função das características inerentes às diversas substâncias químicas que podem ser tóxicas, inflamáveis e explosivas. Por isso, é necessário estar atento às normas e procedimentos de segurança para o trabalho em laboratório. Dentre os procedimentos descritos a seguir, aquele que tem potencial de resultar em um acidente é
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
Durante o preparo de uma solução aquosa de ácido sulfúrico, o técnico de laboratório se descuidou e ocorreu um derramamento do ácido na bancada. A maneira recomendada de neutralizar o ácido sulfúrico derramado e evitar a contaminação da rede hidrossanitária é neutralizar com
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
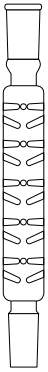
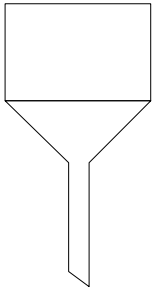
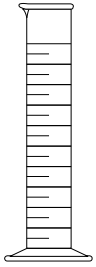
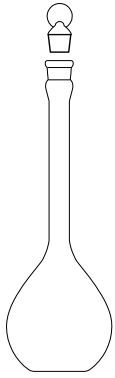
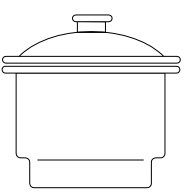
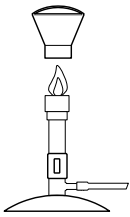
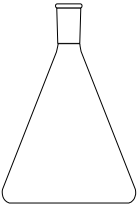
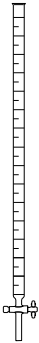
As imagens a seguir representam alguns itens usados em atividades laboratoriais de química.
|
I |
II |
III |
IV |
V |
Com base nessas imagens, verifica-se que o item apresentado em
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
As imagens a seguir representam alguns itens usados em atividades laboratoriais de química.
|
I |
II |
III |
IV |
V |
Na ordem em que são apresentadas, estas imagens representam os seguintes materiais e vidrarias:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
O permanganato de potássio é um sólido de coloração roxa e um poderoso agente oxidante. Em contato com líquidos combustíveis pode resultar em ignição espontânea. Em contato com ácido sulfúrico concentrado pode causar fogo ou explosão. O Globally Harmonized System of Classification and Labelling of Chemicals (GHS) é usado em comunicações de perigos dos produtos químicos. A seguir são apresentados alguns pictogramas que fazem parte desse sistema.
|
I |
II |
III |
IV |
V |
Qual dos pictogramas apresentados indica a característica de agente oxidante do permanganato de potássio?
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
Em um experimento clássico de análise química por gravimetria de precipitação química, o ânion sulfato pode ser determinado na forma de sulfato de bário. Se uma solução aquosa de cloreto de bário for misturada a outra solução aquosa de ácido sulfúrico, a reação química que ocorrerá será representada pela seguinte equação química balanceada:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
De acordo com o princípio de Thompsen e Berthelot, uma reação química será progressivamente mais espontânea à medida que se tornar mais exotérmica. No entanto, esse não é o único critério que deve ser avaliado para prever a espontaneidade de uma reação. Em 1854, Clausius introduziu o conceito de entropia, que apresenta a ideia de que toda reação que ocorre de forma espontânea tende para um aumento de desordem no sistema.
Com base nas ideias de variação de entalpia e entropia, em qual dos seguintes casos a reação poderá ser espontânea, para qualquer valor de temperatura?
Provas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaHidrocarbonetos
Observação: Caso necessário, utilize a Tabela Periódica.
A adrenalina é uma substância secretada em nosso organismo em momentos de tensão, medo e pânico, e tem a capacidade de aumentar a pressão sanguínea, a contração cardíaca e a pulsação. A figura a seguir mostra uma representação da estrutura molecular da adrenalina.
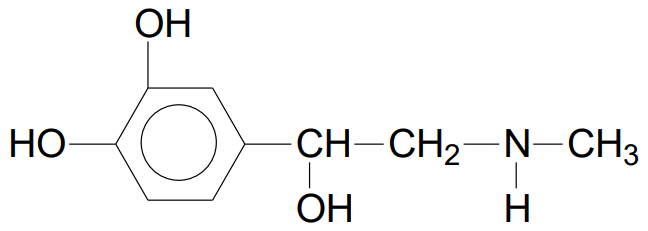
Com base nessa figura, verifica-se que as funções orgânicas presentes na molécula de adrenalina são:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
O etanol é um composto que apresenta uma gama de aplicações, dentre as quais se destacam o uso como fonte renovável de combustível e como matéria-prima de tintas, solventes, aerossóis, fabricação de detergentes e produtos têxteis. Grande parte do etanol produzido no Brasil é proveniente da cana de açúcar, a partir de um processo dividido em várias etapas, tais como a moagem da cana de açúcar, produção do melaço, fermentação do melaço, e destilação do mosto fermentado. Outra forma de produção do etanol ocorre por meio de uma reação entre o carbono grafite, o hidrogênio e o oxigênio, conforme mostra a equação química a seguir:
!$ 2C_{(graf)}+3H_{2(g)}+1⁄2\ O_{2(g)}→C_2H_6O_{(l)} !$
Considere as seguintes equações que representam os processos de combustão:
Eq. 1: combustão completa do carbono grafite !$ (C_{graf}) !$
!$ C_{(graf)}+O_{2(g)}→CO_{2(g)\ }\quad\quad !$ !$ ΔH=-394kJmol^{-1}; !$
Eq. 2: combustão do hidrogênio gasoso
!$ H_{2(g)}+1⁄2\ O_{2(g)}→H_2O_{(l)}\ \quad\quadΔH=-286kJmol^{-1}; !$
Eq. 3: combustão completa do etanol
!$ C_2H_6O_{(l)}+3O_{2\left(g\right)}→2CO_{2(g)}+3H_2O_{(l)}\ \quad\quadΔH=-1368kJmol^{-1}; !$
Empregando a Lei de Hess e as equações representativas de combustão, verifica-se que a entalpia de formação do etanol, a partir do grafite, é igual a
Provas
Caderno Container