Foram encontradas 670 questões.
Dadas as seguintes afirmativas sobre equilíbrio iônico em solução aquosa,
I. Quanto maior a constante de ionização de um ácido, mais forte será esse ácido.
II. Em um ácido poliprótico, a remoção do 2º hidrogênio é bem mais fácil que o 1º hidrogênio.
III. Quanto menor o valor da constante de ionização maior a tendência de liberar !$ H^+ !$.
IV. Para poliácidos o valor da primeira constante de ionização é maior que o da segunda constante.
verifica-se que estão corretas
Provas
Questão presente nas seguintes provas
Dada a tabela abaixo,
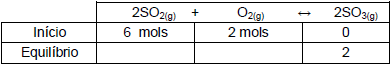
após determinação das lacunas em branco na tabela, o valor da constante de equilíbrio é
Provas
Questão presente nas seguintes provas
Quando representamos graficamente V contra T(ºC), de acordo com a lei de Charles, encontramos uma reta
Provas
Questão presente nas seguintes provas
A capacidade de uma reação espontânea, a T e P constantes, para produzir trabalho útil é a energia livre de Gibbs !$ (ΔG) !$. Dependendo do sinal da variação de energia livre, podemos verificar sua espontaneidade. Dadas as seguintes afirmativas,
I. Se !$ ΔG !$ for negativo a reação a T e P constantes é espontânea.
II. Se !$ ΔG !$ for positivo a reação a T e P constantes é não espontânea.
III. Se !$ ΔG !$ for igual a zero o sistema está em equilíbrio.
IV. Se !$ ΔG !$ for positivo a reação a T e P constantes não se deslocará em nenhuma direção.
verifica-se que estão corretas
Provas
Questão presente nas seguintes provas
O engenheiro francês Sadi Carnot, baseado numa transformação cíclica de um sistema, estudou os princípios que governam a transformação de energia térmica em energia mecânica, trabalho. Com isso ele criou o Ciclo de Carnot, um ciclo reversível que é constituído de
Provas
Questão presente nas seguintes provas
Dada a figura abaixo, a quantidade de matéria do gás no estado A é aproximadamente
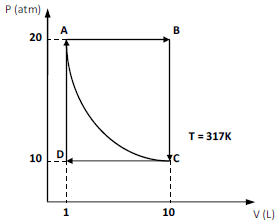
Provas
Questão presente nas seguintes provas
Os sais são substâncias que podem ter comportamento anfótero em soluções aquosas. Considerando os seguintes sais,
I. Cloreto de potássio.
II. Carbonato de sódio.
III. Cloreto de amônio.
IV. Acetato de sódio.
V. Fluoreto de lítio.
quais as soluções aquosas dos sais referidos que vão apresentar um pH acima de 7?
Provas
Questão presente nas seguintes provas
Para que a queima de um combustível ocorra dentro do padrões técnicos e produza a energia e o trabalho desejado, é necessário que a massa do combustível injetada no motor seja misturada a uma quantidade de ar. Forma-se, assim, a mistura combustível-ar, cuja dosagem é feita pela injeção eletrônica ou pelo carburador. A combustão do etanol, dada pela equação, !$ C_2H_5OH + 3O_2 → 2CO_2 + 3 H_2O !$, requer proporções que estabelecem a quantidade mínima de ar necessária para fornecer a quantidade de oxigênio requerida pela queima completa do combustível. De acordo com a equação, a quantidade em mol de oxigênio necessária para queimar 1,80 mol de etanol é
Provas
Questão presente nas seguintes provas
O Cloreto de cálcio é um composto químico extremamente solúvel em água e é deliquescente. É um sal que se apresenta no estado sólido à temperatura ambiente e tem muitas aplicações comuns como em salmoura para máquinas de refrigeração, controle de pó e gelo nas estradas, e no cimento. Por causa de sua forte higroscopia, pode ser usado para secar o ar, assim como outros gases e líquidos orgânicos. A quantidade em mol de cálcio necessária para reagir com 2,5 mol de !$ Cl ^– !$, para produzir o cloreto de cálcio, é
Provas
Questão presente nas seguintes provas
Misturas homogêneas são aquelas que se apresentam como um todo uniforme, mesmo quando observadas através de microscópio. Com base nessa definição e observando os sistemas a seguir,
I. Mistura de mercúrio e ouro, da extração do minério aurífero.
II. Álcool (l) + Acetona (l).
III. Água (l) + Açúcar (s).
IV. Fração gasosa do petróleo (Metano + Etano + Propano + Butano).
constituem sempre sistemas homogêneos, qualquer que seja a proporção:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container