Foram encontradas 240 questões.
Considere a célula (pilha) representada na figura a seguir:
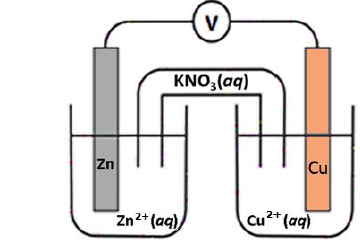
As semirreações são:
\( Zn^{2+}(aq) + 2e^– → Zn(s) Eº = –0,76 V \\ Cu^{2+}(aq) + 2e– → Cu(s) Eº = +0,34 V \)
Assinale a alternativa que corresponde à reação espontânea da célula (pilha):
Provas
Considere a situação na qual um estudante acidentalmente preparou uma solução de 250,0 mL de NaC\( \ell \) com uma concentração de 0,150 mol L–1, em vez de 0,250 mol L–1. O volume de água necessário para evaporar a solução para obter a concentração desejada de 0,250 mol L–1 é:
Provas
O ácido fosfórico, H3PO4, estabelece o seguinte equilíbrio em solução aquosa:
H3PO4(aq)+H2O(l)⇌H3O+(aq)+H2PO4−(aq) K1
H2PO4−(aq)+H2O(l)⇌H3O+(aq)+HPO\( ^{2-}_4 \)(aq) K2
HPO\( ^{2-}_4 \)(aq)+H2O(l)⇌H3O+(aq)+PO\( ^{3-}_4 \)(aq) K3
A relação entre os valores da constante de equilíbrio, K, é:
Provas
A maioria das reações químicas não é elementar, ou seja, ocorre em mais de uma etapa. O conjunto de etapas por meio do qual ocorre uma reação é denominado mecanismo de reação. Para ilustrar um mecanismo de reação, considere a reação química que ocorre em duas etapas:
Etapa 1: 2NO + H2 → N2 + H2O2 Lenta Etapa 2: H2O2 + H2 → 2H2 Rápida
A partir dessas informações, podemos afirmar que a ordem de reação é:
Provas
A Lei de Hess estabelece que, para uma dada reação, a variação da entalpia é sempre a mesma, esteja essa reação ocorrendo em uma ou em várias etapas. Para exemplificar, no quadro a seguir são dadas algumas reações químicas e suas respectivas variações de entalpia de reação:
| Reação | Δ /(kJ mol–1) |
|---|---|
| S(s) + O2(g) → SO2(g) | –296,8 |
| H2(g) + ½O2(g) → H2O(\( \ell \)) | –285,8 |
| H2(g) + S(s) → H2S(g) | –20,6 |
Considere a seguinte reação:
2H2S(g) + 3O2(g) → 2H2O(\( \ell \)) + 2SO2(g)
A partir dessas informações, podemos afirmar que a variação de entalpia dessa reação é:
Provas
Num experimento realizado no Laboratório de Química, são utilizados dois frascos 1 e 2, com exatamente 2,0 L de volume. Considere os dados a seguir:
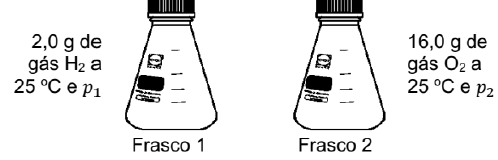
Sendo a energia cinética média e a pressão, podemos afirmar que:
Provas
A eletroquímica estuda a transferência de elétrons durante o processo de conversão de energia química em energia elétrica ou vice-versa. Nesse contexto, assinale a alternativa que NÃO caracteriza um agente oxidante:
Provas
A coleta seletiva de resíduos sólidos tem o objetivo de reduzir o impacto ambiental gerado pela produção de resíduos em uma cidade, destinando corretamente os materiais para reaproveitamento ou descarte adequado. Nesse caso, são usados coletores de cores diferentes para diferentes tipos de lixos ou resíduos. Para exemplificar, relacione o tipo de coletor com o tipo de lixo a ser coletado:
| Coletor de Plástico (Código de cor) | Tipo de lixo ou resíduo |
|---|---|
| 1.Amarelo | ( ) Copos, garrafas Pet, plásticos em geral. |
| 2.Azul | ( ) Garrafas e cacos de vidro. |
| 3.Marrom | ( ) Jornais, revistas e embalagens de leite. |
| 4.Verde | ( ) Latas e ferragens. |
| 5.Vermelho | ( ) Resíduos orgânicos, de origem animal ou vegetal. |
Assinale a alternativa que preenche, CORRETAMENTE, a coluna da direita de cima para baixo:
Provas
Um dos fatores que alteram a velocidade das reações é o uso de um catalisador, pois ele acelera uma reação porque:
Provas
Em um experimento para provar a lei da conservação da massa, no laboratório, um aluno usou um fio fino de ferro de 15,5 g e colocou imerso em uma solução contendo 21,0 g de sulfato de cobre (II), e o cobre metálico começou a se formar. Depois de certo tempo, a reação parou porque todo o sulfato de cobre (II) reagiu. A massa do fio de ferro restante foi de 8,5 g e a massa de cobre formado foi de 8,6 g. A partir dessas informações, podemos afirmar que a massa de sulfato de ferro (II) formada na reação é:
Provas
Caderno Container