Foram encontradas 50 questões.
A química analítica pode ser dividida em qualitativa e em quantitativa e tem aplicações nas mais diversas
áreas da ciência. Os métodos clássicos de análise envolvem as análises gravimétricas e titulométricas. Sobre
esses métodos, assinale a alternativa CORRETA:
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Titulou-se uma solução aquosa de ácido hipocloroso com solução aquosa de hidróxido de sódio 0,20 mol L-1 para a determinação da sua concentração. Para a titulação 10,0 mL do ácido, foram necessários 22,0 mL da
base. A concentração molar do ácido hipocloroso e o pH da solução ao final da titulação são, respectivamente:
Provas
Questão presente nas seguintes provas
Considere uma solução aquosa de ácido acético (CH3COOH), com concentração 0,10 mol/L, e uma solução
aquosa de hidróxido de sódio (NaOH), também com concentração 0,10 mol/L. A constante de dissociação
ácida do ácido acético (Ka) é 1,8 × 10-5.
Considerando esses dados, analise as proposições a seguir:
I - O pH da solução de ácido acético será menor que o pH da solução de NaOH.
II - A adição de NaOH à solução de ácido acético irá formar acetato de sódio (CH3COONa) e água.
III - O pH de uma solução tampão formada pela adição de CH3COOH e CH3COONa pode ser calculado pela equação de Henderson-Hasselbalch.
IV - O pH da solução tampão depende da concentração relativa de CH3COOH e CH3COONa, e não da concentração total.
É CORRETO concluir o que se afirma em:
Considerando esses dados, analise as proposições a seguir:
I - O pH da solução de ácido acético será menor que o pH da solução de NaOH.
II - A adição de NaOH à solução de ácido acético irá formar acetato de sódio (CH3COONa) e água.
III - O pH de uma solução tampão formada pela adição de CH3COOH e CH3COONa pode ser calculado pela equação de Henderson-Hasselbalch.
IV - O pH da solução tampão depende da concentração relativa de CH3COOH e CH3COONa, e não da concentração total.
É CORRETO concluir o que se afirma em:
Provas
Questão presente nas seguintes provas
A reação reversível e exotérmica de formação do amoníaco a partir de nitrogênio e hidrogênio é representada
pela equação:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Considerando essas informações, avalie as proposições sobre o comportamento do sistema em equilíbrio a seguir:
I - A diminuição da pressão total favorece a formação de amoníaco (NH3).
II - A elevação da temperatura desloca o equilíbrio no sentido da decomposição do amoníaco.
III - O aumento da concentração de hidrogênio desloca o equilíbrio no sentido da formação de mais amoníaco.
IV - A adição de um catalisador aumenta a constante de equilíbrio da reação.
V - A redução da concentração de amoníaco faz com que o sistema se desloque no sentido de produzir mais amoníaco.
Com base princípio de Le Chatelier, é CORRETO concluir o que se afirma em:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Considerando essas informações, avalie as proposições sobre o comportamento do sistema em equilíbrio a seguir:
I - A diminuição da pressão total favorece a formação de amoníaco (NH3).
II - A elevação da temperatura desloca o equilíbrio no sentido da decomposição do amoníaco.
III - O aumento da concentração de hidrogênio desloca o equilíbrio no sentido da formação de mais amoníaco.
IV - A adição de um catalisador aumenta a constante de equilíbrio da reação.
V - A redução da concentração de amoníaco faz com que o sistema se desloque no sentido de produzir mais amoníaco.
Com base princípio de Le Chatelier, é CORRETO concluir o que se afirma em:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Para preparar 500 mL de uma solução de ácido clorídrico com uma concentração molar de 0,2 mol/L (M),
você tem disponível ácido clorídrico concentração 3 M. Para preparar a solução desejada, qual volume da
solução concentrada deve ser diluído e qual será o volume final da solução após a diluição?
Provas
Questão presente nas seguintes provas
O ácido nítrico é amplamente utilizado na indústria química, tais como: a Indústria Têxtil, de Espumas, de
Tintas e de Embalagens. Um dos processos industriais para a produção de ácido nítrico envolve as seguintes
etapas:
1. Oxidação da amônia para formar óxido nítrico.
2. Oxidação do óxido nítrico para formar dióxido de nitrogênio.
3. Dissolução do dióxido de nitrogênio em água para formar ácido nítrico.
Considerando essas reações, um rendimento global de 85% em todo o processo, e massas molares dos elementos H: 1,01 g/mol, N: 14,01 g/mol e O: 16,00 g/mol; a massa de amônia necessária para produzir 1 kg de ácido nítrico é de aproximadamente:
1. Oxidação da amônia para formar óxido nítrico.
2. Oxidação do óxido nítrico para formar dióxido de nitrogênio.
3. Dissolução do dióxido de nitrogênio em água para formar ácido nítrico.
Considerando essas reações, um rendimento global de 85% em todo o processo, e massas molares dos elementos H: 1,01 g/mol, N: 14,01 g/mol e O: 16,00 g/mol; a massa de amônia necessária para produzir 1 kg de ácido nítrico é de aproximadamente:
Provas
Questão presente nas seguintes provas
Sobre os compostos inorgânicos, analise as alternativas acerca de suas características:
I - Em geral, ácidos são substâncias moleculares que reagem com a água para produzir íons, um dos quais é o íon hidrônio, H3O+.
II - As bases compreendem duas espécies de compostos: os compostos iônicos, que contêm OH− ou O2−, e os compostos moleculares, que reagem com a água produzindo íons hidróxido.
III - Os sais inorgânicos podem ser eletrólitos fortes, pois são compostos iônicos solúveis e conduzem corrente elétrica quando dissolvidos em água.
IV - Óxidos de não-metais produzem soluções aquosas ácidas.
É CORRETO o que se afirma em:
I - Em geral, ácidos são substâncias moleculares que reagem com a água para produzir íons, um dos quais é o íon hidrônio, H3O+.
II - As bases compreendem duas espécies de compostos: os compostos iônicos, que contêm OH− ou O2−, e os compostos moleculares, que reagem com a água produzindo íons hidróxido.
III - Os sais inorgânicos podem ser eletrólitos fortes, pois são compostos iônicos solúveis e conduzem corrente elétrica quando dissolvidos em água.
IV - Óxidos de não-metais produzem soluções aquosas ácidas.
É CORRETO o que se afirma em:
Provas
Questão presente nas seguintes provas
Com base nas regras sobre nomenclatura de compostos inorgânicos, as representações das fórmulas
moleculares cujas nomenclaturas são: ácido perclórico, hidróxido ferroso, carbonato de zinco e dióxido de
titânio, são respectivamente:
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Sobre a geometria molecular e suas características, avalie as proposições a seguir:
I - A molécula de água possui uma geometria angular devido à repulsão dos pares de elétrons dos domínios não ligantes.
II - A molécula de metano possui uma geometria tetraédrica, com 2 domínios ligantes e 2 não ligantes.
III - A molécula de trifluoreto de cloro apresenta uma geometria gangorra, devido a presença de 3 domínios ligantes e 1 não ligante.
É CORRETO o que se afirma em:
I - A molécula de água possui uma geometria angular devido à repulsão dos pares de elétrons dos domínios não ligantes.
II - A molécula de metano possui uma geometria tetraédrica, com 2 domínios ligantes e 2 não ligantes.
III - A molécula de trifluoreto de cloro apresenta uma geometria gangorra, devido a presença de 3 domínios ligantes e 1 não ligante.
É CORRETO o que se afirma em:
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A estrutura de Lewis fornece a conectividade atômica, nos mostrando o número e os tipos de ligação entre os
átomos. Analise as estruturas a seguir no que se refere às ligações entre átomos diferentes nas seguintes
moléculas:
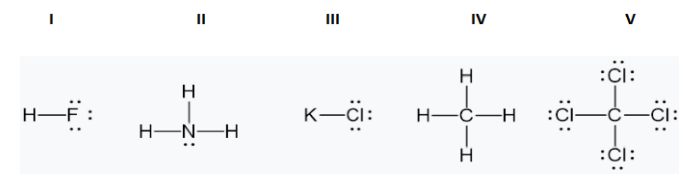
A partir da análise é correto afirmar que ordem de polaridade decrescente para as ligações entre átomos diferentes é:

A partir da análise é correto afirmar que ordem de polaridade decrescente para as ligações entre átomos diferentes é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container