Foram encontradas 364 questões.
- Gases
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
Provas
A reação de 1 mol de grafita, C(s), com 1 mol de oxigênio gasoso produz 1 mol de dióxido de carbono gasoso. O diagrama abaixo mostra a variação de entalpia para essa reação.

Analise as afirmativas abaixo sobre essa reação.
I. A energia liberada pode ser chamada de entalpia de formação de CO2(g).
II. A energia liberada pode ser chamada de entalpia de combustão de grafita.
III. É uma reação endotérmica.
IV. Para queimar 1 mol de C(s), é necessário fornecer 393,5 kJ para o sistema.
Está(ão) CORRETA(S):
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaVelocidade de Reação, Energia de Ativação e Catalisadores
Na reação de zinco metálico (Zn(s)) com ácido clorídrico (HCl(aq)), há formação de cloreto de zinco (ZnCl2(aq)) e gás hidrogênio (H2(g)), conforme a seguinte equação:
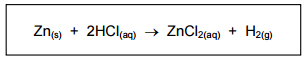
Nessa reação, o HCl é consumido e a tabela a seguir mostra a sua concentração em função do tempo.
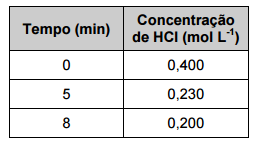
A alternativa que apresenta o valor correto da velocidade média da reação (mol L-1 min-1 ) no intervalo de 5 a 8 minutos é
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias Inorgânicas
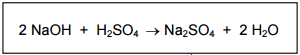
O volume, em litros (L), de uma solução de H2SO4 1,0 mol L-1 que reage com 0,5 mol de NaOH é:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
Analise as reações abaixo.
I. SO2 + H2O2 -› H2SO4
II. SO2 + H2O -› H2SO3
III. SO2 + NH4OH -› NH4HSO3
Das reações, ocorre o fenômeno de oxirredução em
Provas
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
Caderno Container