Foram encontradas 364 questões.
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma amostra de 6,000 g de hematita, um mineral de ferro, foi dissolvida completamente em
ácido, e o ferro presente foi totalmente reduzido a Fe2+. A seguir, a amostra dissolvida foi transferida para
um balão volumétrico de 250,0 mL, o qual foi completado com água destilada até a marca de aferição. Uma
alíquota de 10,00 mL dessa solução contendo o Fe2+ foi titulada com exatamente 25,00 mL de uma solução
padrão 0,020 mol L-1
de dicromato, em meio ácido, segundo a equação abaixo.
Cr2O72-(aq) + 6Fe2+(aq) + 14H+(aq) -› 2Cr3+(aq) + 6Fe3+(aq) + 7H2O(l)
Considerando a estequiometria dessa reação, a porcentagem em massa de Fe na amostra analisada é, aproximadamente, igual a
Cr2O72-(aq) + 6Fe2+(aq) + 14H+(aq) -› 2Cr3+(aq) + 6Fe3+(aq) + 7H2O(l)
Considerando a estequiometria dessa reação, a porcentagem em massa de Fe na amostra analisada é, aproximadamente, igual a
Provas
Questão presente nas seguintes provas
O fenômeno de corrosão metálica causa grandes prejuízos às indústrias, pois nesse
processo ocorre a dissolução lenta da superfície de equipamentos, quando os mesmos são expostos ao ar,
em contato com o solo ou água do mar. Com o objetivo de minimizar a corrosão do ferro em equipamentos,
são utilizados os chamados “eletrodos de sacrifício”, os quais são formados por barras de outros metais,
convenientemente escolhidos que, quando colocados em contato com a superfície do equipamento, sofrem
corrosão no lugar do ferro.

Com base nos dados tabelados, são considerados “eletrodos de sacrifício” adequados as barras de

Com base nos dados tabelados, são considerados “eletrodos de sacrifício” adequados as barras de
Provas
Questão presente nas seguintes provas
A célula eletroquímica representada pelo esquema da figura que segue, onde V é um
voltímetro e S é uma ponte salina que contém uma solução saturada de nitrato de potássio (KNO3), possui
um eletrodo de zinco imerso em uma solução de nitrato de zinco, Zn(NO3)2, e outro eletrodo de prata imerso
em uma solução de nitrato de prata, AgNO3, nas concentrações indicadas a 25ºC.
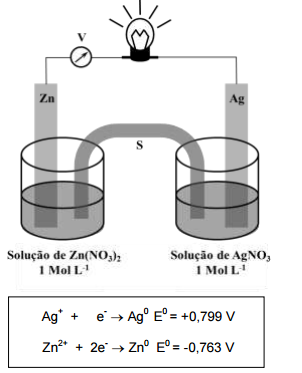
Considerando a célula eletroquímica e os potenciais-padrão de redução acima representados, é CORRETO afirmar:

Considerando a célula eletroquímica e os potenciais-padrão de redução acima representados, é CORRETO afirmar:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
A tabela abaixo mostra os valores de constantes de dissociação, Kb, a 25 °C, para
diversas bases. 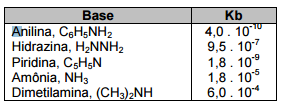
Analisando esses valores, é CORRETO afirmar:

Analisando esses valores, é CORRETO afirmar:
Provas
Questão presente nas seguintes provas
A quantidade de carbono em um composto orgânico foi determinada através da queima de
0,2121 g do composto em um fluxo de oxigênio. O CO2 produzido na reação foi coletado em uma solução
de hidróxido de bário. Se 0,6000 g de BaCO3 foi formado, a porcentagem de carbono na amostra é
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O Cr de uma superfície cromada de dimensões 3,00 x 5,00 cm foi dissolvido em ácido
clorídrico. O pH da solução foi ajustado e, posteriormente, foram adicionados 15,00 mL de solução padrão
de EDTA 0,200 mol L-1
. O reagente em excesso foi retrotitulado com um volume de 4,00 mL de solução
padrão de Cu2+ 0,100 mol L-1
. A massa aproximada, em mg, de Cr em cada centímetro quadrado da
superfície foi
Provas
Questão presente nas seguintes provas
A técnica de cromatografia é utilizada para separação, identificação e quantificação de
componentes químicos em misturas complexas. Essa técnica se baseia na distribuição de substâncias entre
duas fases químicas ou físicas, sendo uma fase estacionária e a outra fase móvel ao longo do sistema.
Com relação aos diferentes tipos de técnicas cromatográficas, é INCORRETO afirmar:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Transformações Químicas e EnergiaEletroquímica
Os métodos potenciométricos de análise se baseiam em medidas do potencial de células
eletroquímicas na ausência de correntes apreciáveis. O potencial medido está relacionado com a
composição química dos eletrodos e das soluções nas quais estão submersos. Considerando as
características desses métodos, analise as afirmativas que se seguem.
I. O eletrodo adequado para medidas de pH mede o potencial que se desenvolve através de uma fina membrana de vidro que separa duas soluções com diferentes concentrações do íon hidrogênio. II. A potenciometria é uma técnica eletroanalítica em que se obtêm medidas de potencial geradas por espécies químicas em um meio, sem a necessidade da utilização de um eletrodo de referência. III. A medida do potencial de um eletrodo indicador pode ser utilizada para determinar o ponto de equivalência de uma titulação.
É CORRETO
I. O eletrodo adequado para medidas de pH mede o potencial que se desenvolve através de uma fina membrana de vidro que separa duas soluções com diferentes concentrações do íon hidrogênio. II. A potenciometria é uma técnica eletroanalítica em que se obtêm medidas de potencial geradas por espécies químicas em um meio, sem a necessidade da utilização de um eletrodo de referência. III. A medida do potencial de um eletrodo indicador pode ser utilizada para determinar o ponto de equivalência de uma titulação.
É CORRETO
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A técnica de condutometria direta pode avaliar o comportamento de soluções aquosas
quanto à condução de corrente elétrica, por meio de medidas de condutância. Essa condutância é um
resultado da soma da contribuição individual de cada íon presente na solução. A tabela a seguir mostra
diferentes tipos de soluções aquosas e suas concentrações.

Considerando as medidas de condutância que poderiam ser obtidas para essas soluções, é CORRETO afirmar:

Considerando as medidas de condutância que poderiam ser obtidas para essas soluções, é CORRETO afirmar:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em uma titulação condutométrica, uma amostra de 5 mL de HCl foi titulada com NaOH
0,10 mol L-1
padrão. A partir do gráfico de condutância vs. volume de solução de NaOH adicionado na
titulação, é CORRETO afirmar que a concentração, em mol por litro, da solução de HCl titulada é 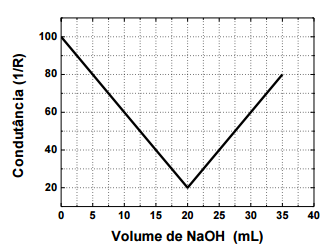

Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container