Foram encontradas 50 questões.
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um estudante preparou 100 mL de uma solução 1,0 M de NaCl, solução A. Em seguida, retirou uma alíquota de
2 mL dessa solução e transferiu para um frasco contendo 98 mL de água destilada, gerando a solução B. Por
fim, da solução B retirou 50 mL e transferiu para um balão volumétrico de 100 mL e aferiu o volume final com
água destilada, solução C. As concentrações molares das soluções B e C são, respectivamente:
Provas
Questão presente nas seguintes provas
Os ácidos e bases são identificados empiricamente como duros ou moles pela ordem oposta das forças com as
quais elas formam complexos com as bases íons haletos. Os ácidos duros tendem a se ligar com bases duras, e
bases moles tendem a se ligar com ácidos moles. Assinale a alternativa que contém somente ácidos duros.
Provas
Questão presente nas seguintes provas
A análise elementar é uma técnica de química analítica que determina a composição de uma amostra. Uma
amostra de produto de limpeza foi analisada e apresentou as seguintes percentagens: 22,9% de Na; 21,5% de B
e 55,7% de O. A sua fórmula empírica é
Provas
Questão presente nas seguintes provas
A medida de amostras em uma análise química está sujeita a erros. Entre as alternativas abaixo, assinale a que
contém dois tipos de erros sistemáticos mais comuns em uma análise de dados.
Provas
Questão presente nas seguintes provas
Um extrato vegetal de uma planta medicinal da Amazônia foi analisado por CLAE (HPLC) e compostos
aromáticos apolares foram separados usando fase estacionária C18 e como fase móvel uma mistura de
H2O/MeOH 4:6 em modo isocrático. Assinale a alternativa que indica como seriam afetados os tempos de
retenção se a fase móvel fosse alterada para H2O/MeOH 2:8 em modo isocrático.
Provas
Questão presente nas seguintes provas
Um técnico em química calculou, através do método de Mohr, a percentagem de cloreto em uma amostra de sal.
Para isso, ele pesou 0,6510 g do sal seco em estufa e posteriormente dissolveu em água. A solução salina
resultante foi, então, transferida para um frasco de Erlenmeyer e titulada com solução de AgNO3 0,1000 mol/L,
sendo gastos 45,35 mL de AgNO3 na titulação. A porcentagem de cloreto encontrada pelo técnico na amostra de
sal foi de
Dado: MM Cl= 35,45 g/mo
Dado: MM Cl= 35,45 g/mo
Provas
Questão presente nas seguintes provas
Considere as seguintes medidas: 1,32; 120; 0,005 e 0,023. Indique quantos números significativos há em cada
medida, respectivamente.
Provas
Questão presente nas seguintes provas
O professor de laboratório pediu para os alunos realizarem a reação de condensação da benzoína. Foram
utilizados 5 mL de benzaldeído para a reação apresentada a seguir.
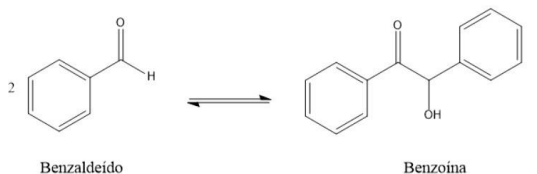
Ao final da reação foram obtidos 2 g de benzoína. Considerando a densidade do benzaldeído igual a 1 g/cm3 e as seguintes massas molares (C= 12 g/mol, H= 1 g/mol e O= 16 g/mol), é correto afirmar que o rendimento da reação correspondeu a

Ao final da reação foram obtidos 2 g de benzoína. Considerando a densidade do benzaldeído igual a 1 g/cm3 e as seguintes massas molares (C= 12 g/mol, H= 1 g/mol e O= 16 g/mol), é correto afirmar que o rendimento da reação correspondeu a
Provas
Questão presente nas seguintes provas
Um estudante deixou na bancada do laboratório um frasco de 1,0 L contendo um líquido sem identificação. O
técnico do laboratório descobriu que 37,9 mL do líquido pesam 29,9 g, o que possibilitou a rotulagem do frasco
pelo técnico de laboratório. Esse líquido é o
Provas
Questão presente nas seguintes provas
Um técnico de laboratório ficou responsável de analisar a percentagem de ferro em 0,250 g de uma amostra de
minério. Para essa análise, ele resolveu usar a dicromatometria. Então, após tratamento adequado do mineral,
todo o ferro foi reduzido a Fe2+. Na análise titulométrica, ele gastou 25 mL de uma solução 0,02 M de K2Cr2O7.
Assinale a alternativa que apresenta a percentagem de ferro encontrada na amostra.
Dados: MM Fe = 56 g/mol
Cr2O72- + 6Fe2+ + 14H+ → 2Cr3+ + 6Fe3+ + 7H2O
Assinale a alternativa que apresenta a percentagem de ferro encontrada na amostra.
Dados: MM Fe = 56 g/mol
Cr2O72- + 6Fe2+ + 14H+ → 2Cr3+ + 6Fe3+ + 7H2O
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container