Foram encontradas 60 questões.
TEXTO 1
Por que razão é tão difícil manter o peso ideal, se todos almejam ficar esguios e sabem que a obesidade aumenta o risco de hipertensão, diabetes, osteo-artrite, ataques cardíacos e derrames cerebrais?
No cérebro, existe um centro neural responsável pelo controle da fome e da saciedade. Milhões de anos de seleção natural forjaram a fisiologia desse centro, para assegurar a ingestão de um número de calorias compatível com as necessidades energéticas do organismo.
Nessa área cerebral são integradas as informações transmitidas pelos neurônios, que conduzem sinais recolhidos no meio externo, nas vísceras, na circulação e no ambiente bioquímico que servem de substrato para os fenômenos psicológicos. Estímulos auditivos, visuais e olfatórios são permanentemente registrados pelo centro da saciedade, e explicam a fome que subitamente sentimos diante do cheiro e da visão de certos alimentos. Faz frio, os neurônios responsáveis pela condução dos estímulos térmicos enviam informações para o centro e a fome aumenta, em resposta às maiores necessidades energéticas dos animais para manter constante a temperatura corporal, no inverno.
Quando as paredes do estômago são distendidas, a taxa de glicose na circulação aumenta, certos neurotransmissores são liberados no aparelho digestivo; ou quando determinadas enzimas digestivas atingem os limites de sua produção, o centro da saciedade bloqueia a fome e interrompe a refeição. Fenômenos psicológicos também interferem permanentemente com o mecanismo da fome e da saciedade, porque os centros cerebrais são especialmente sensíveis aos neurotransmissores envolvidos nas sensações de prazer. Por isso, comemos mais quando estamos entre amigos e menos em ambientes hostis ou sob stress psicológico.
(Drauzio Varella. Folha de S. Paulo, 27 de julho de 2002. Fragmento.).
O Texto 1 se inicia com uma pergunta: “Por que razão é tão difícil manter o peso ideal...”. Na verdade, com essa pergunta o autor do texto pretende:
Provas
Questão presente nas seguintes provas
No ambiente laboratorial, muitos são os riscos aos quais estudantes, pesquisadores e técnicos podem estar submetidos. Estes riscos podem ser categorizados em diferentes grupos. Faça a associação correta entre os riscos abaixo relacionados e os grupos aos quais eles pertencem.
1) Radiação ionizante ( ) Risco biológico
2) Vapores tóxicos ( ) Risco químico
3) Mofo ( ) Risco físico
4) Ferramentas inadequadas ( ) Risco ergonômico
5) Esforço físico intenso ( ) Risco de acidente
A sequência correta, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
TEXTO 1
Por que razão é tão difícil manter o peso ideal, se todos almejam ficar esguios e sabem que a obesidade aumenta o risco de hipertensão, diabetes, osteo-artrite, ataques cardíacos e derrames cerebrais?
No cérebro, existe um centro neural responsável pelo controle da fome e da saciedade. Milhões de anos de seleção natural forjaram a fisiologia desse centro, para assegurar a ingestão de um número de calorias compatível com as necessidades energéticas do organismo.
Nessa área cerebral são integradas as informações transmitidas pelos neurônios, que conduzem sinais recolhidos no meio externo, nas vísceras, na circulação e no ambiente bioquímico que servem de substrato para os fenômenos psicológicos. Estímulos auditivos, visuais e olfatórios são permanentemente registrados pelo centro da saciedade, e explicam a fome que subitamente sentimos diante do cheiro e da visão de certos alimentos. Faz frio, os neurônios responsáveis pela condução dos estímulos térmicos enviam informações para o centro e a fome aumenta, em resposta às maiores necessidades energéticas dos animais para manter constante a temperatura corporal, no inverno.
Quando as paredes do estômago são distendidas, a taxa de glicose na circulação aumenta, certos neurotransmissores são liberados no aparelho digestivo; ou quando determinadas enzimas digestivas atingem os limites de sua produção, o centro da saciedade bloqueia a fome e interrompe a refeição. Fenômenos psicológicos também interferem permanentemente com o mecanismo da fome e da saciedade, porque os centros cerebrais são especialmente sensíveis aos neurotransmissores envolvidos nas sensações de prazer. Por isso, comemos mais quando estamos entre amigos e menos em ambientes hostis ou sob stress psicológico.
(Drauzio Varella. Folha de S. Paulo, 27 de julho de 2002. Fragmento.).
No trecho: “Milhões de anos de seleção natural forjaram a fisiologia desse centro, para assegurar a ingestão de um número de calorias compatível com as necessidades energéticas do organismo”, quanto ao sentido, indica:
Provas
Questão presente nas seguintes provas
O gás acetileno, !$ C_2H_2 !$, é muito utilizado como combustível de maçaricos utilizados em processos de soldagem. Uma das maneiras de se preparar este hidrocarboneto, é através do carbeto de cálcio, !$ CaC_2 !$, que reage com água para formar hidróxido de cálcio e acetileno, de acordo com a reação abaixo:
!$ { \large {CaC_2 (s) + 2H_2 O(l) \longrightarrow Ca (OH)_2 (aq) + C_2 H_2 (g)}} !$
Calcule o volume de gás acetileno a 1 atm e !$ 27^\circ C !$ , que é produzido a partir de 3,20 g de carbeto de cálcio e água em excesso, considerando o rendimento da reação igual a 100%. Dado: !$ CaC_2 = 64,0\,g/mol; R = 0,082\,atmLmol^{-1}K^{-1} !$
Provas
Questão presente nas seguintes provas
Um técnico decidiu analisar o teor de manganês de uma amostra por espectroscopia de absorção atômica. Para determinar a curva de calibração, ele preparou cinco soluções diferentes de !$ Mn^{2+} !$ (100 mL cada solução) com as seguintes concentrações: 5 ppm, 10 ppm, 15 ppm, 20 ppm e 25 ppm. Para preparar essas soluções, foi utilizada uma solução padrão com concentração de íons !$ Mn^{2+} !$ igual 0,1000 g/L. Calcule o volume total de solução padrão que foi utilizado para preparar as cinco soluções, considerando que a densidade das soluções é 1,0 g/mL.
Provas
Questão presente nas seguintes provas
A água utilizada na preparação de soluções padrão deve seguir um rigoroso processo de purificação. Muitas vezes, é necessário que a água passe por uma coluna contendo uma resina de troca iônica. No caso das resinas de troca catiônica, ocorre a troca de íons hidrogênio !$ (H^+) !$ por contaminantes catiônicos, como !$ Ca^{2+} !$, !$ Mg{2+} !$, !$ Na^+ !$ etc. As resinas aniônicas trocam seus íons hidroxila !$ (OH)^- !$ pelos contaminantes aniônicos, como !$ Cl; CIO_3^{-}, NO_3^{-}, F^- !$ etc. Como resultado, a água que passa por este processo é denominada:
Provas
Questão presente nas seguintes provas
O gráfico a seguir ilustra o resultado de uma pesquisa sobre o nível de colesterol, em mg/dl, de um grupo de 300 pessoas. Na horizontal, estão marcados os níveis de colesterol, e, na vertical correspondente, o número de pessoas com aquele nível de colesterol. Os dados também figuram na tabela a seguir.
| Nível de colesterol (em mg/dl) | Nº de pessoas |
| 205 | 40 |
| 210 | 80 |
| 215 | 60 |
| 220 | 120 |
Admitindo as informações acima, assinale a alternativa incorreta.
Provas
Questão presente nas seguintes provas
A espectrofotometria é um método analítico muito utilizado em investigações biológicas e físico-químicas. Sobre a espectrofotometria na região visível, foram feitas as seguintes afirmações:
1) Se o analito for incolor, é possível adicionar reagentes que o convertam numa espécie colorida.
2) A espectrofotometria na região do visível não deve ser utilizada em análises quantitativas.
3) Neste tipo de análise, devem-se utilizar fontes que emitam radiação na faixa de 1000 a 2000 nm.
2) A espectrofotometria na região do visível não deve ser utilizada em análises quantitativas.
3) Neste tipo de análise, devem-se utilizar fontes que emitam radiação na faixa de 1000 a 2000 nm.
Está(ão) correta(s):
Provas
Questão presente nas seguintes provas
Um estudante preparou uma solução conforme mostra o esquema abaixo:
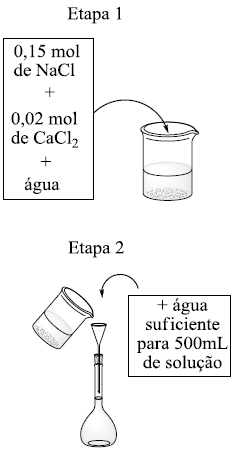
Considerando a total solubilização dos sais utilizados, a concentração de íons cloreto na solução preparada é:
Provas
Questão presente nas seguintes provas
Dentro de um frasco sem rótulo, a !$ 25^\circ C !$ , há um sólido branco desconhecido. Este sólido é muito solúvel em água, e sua solução aquosa tem pH maior que 7. Não conduz a corrente elétrica no estado sólido; entretanto, sua solução aquosa conduz. Este sólido pode ser:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container