Foram encontradas 280 questões.
Um frasco contém uma mistura em equilíbrio de X2(g) e X atômico, segundo a reação:
X2(g) ⇌ 2 X(g)
A pressão de equilíbrio encontrada foi de 2,4 atm em certa condição de temperatura e volume. Se X2 gasoso a uma pressão parcial de 3 atm for adicionado à mistura em equilíbrio acima, a volume e temperatura constantes, a nova pressão de equilíbrio será de 5,66 atm, sendo que, no processo, a pressão do X (g) atômico aumenta 65% em relação ao valor da condição inicial. Nestas condições, assinale a opção que mostra O VALOR MAIS PRÓXIMO DE Kp para a decomposição de X2(g), na mesma temperatura:
Provas
Questão presente nas seguintes provas
Em uma aula de laboratório, o professor entrega uma solução e informa que ela contém 6,56% em massa de
glicose (C6H12O6), que a densidade da solução é 1,03 g/mL e solicita que seja determinada a concentração molar
da solução. De posse dessas informações, assinale a opção que mostra o valor CORRETO da concentração
molar da solução:
Dados eventualmente necessários: massas molares (g/mol): C = 12; O = 16; H = 1.
Provas
Questão presente nas seguintes provas
Sabendo que, em certa temperatura, em uma reação química de primeira ordem: R → P, a concentração de
reagente que não reagiu após 2h e 5h desde o início da reação foi 3,00 x 10-3 mol/L e 1,50 x 10-3 mol/L,
respectivamente, assinale a opção que mostra A CONCENTRAÇÃO DE REAGENTE que permanece sem reagir
após 10h do início da reação:
Dados eventualmente necessários: ln(2) = 0,693; ln(0,315) = -1,155; ln(0,630) = -0,462; ln(0,0993) = -2,31.
Provas
Questão presente nas seguintes provas
Um processo eletrolítico envolvendo o hidrogenossulfato de amônio produz persulfato de amônio, de acordo com
as reações: 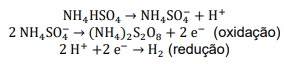
A hidrólise do persulfato de amônio forma H2O2:
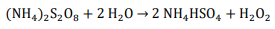
Se a eficiência do processo eletrolítico é de 60% assinale a opção que mostra a INTENSIDADE DE CORRENTE necessária para produzir 97 g de H2O2 por hora: Dados eventualmente necessários: constante de Faraday = 96500 C/mol; massas molares (g/mol): N = 14; O = 16; H = 1; S = 32.
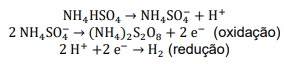
A hidrólise do persulfato de amônio forma H2O2:
Se a eficiência do processo eletrolítico é de 60% assinale a opção que mostra a INTENSIDADE DE CORRENTE necessária para produzir 97 g de H2O2 por hora: Dados eventualmente necessários: constante de Faraday = 96500 C/mol; massas molares (g/mol): N = 14; O = 16; H = 1; S = 32.
Provas
Questão presente nas seguintes provas
A Ficha de Informações de Segurança de Produtos Químicos (FISPQ) fornece informações sobre vários
aspectos de produtos químicos (substâncias ou misturas) quanto à proteção, à segurança, à saúde e ao meio
ambiente. Analisando as afirmações abaixo, assinale a opção CORRETA:
Provas
Questão presente nas seguintes provas
No trabalho diário de um técnico de laboratório de Química, faz-se necessário o conhecimento de materiais e
equipamentos básicos de laboratório, haja vista que é rotineiro o uso de vidrarias e outros instrumentos de uso
geral. Com base neste conhecimento, analise as informações abaixo:
I. Suporta elevadas temperaturas, tem formato arredondado e permite aquecimento uniforme. Essa vidraria é utilizada em processos de destilação, sistemas de evaporação a vácuo e refluxo;
II. É utilizada para medição de volumes, em que não é requerida precisão, e a presença de um bico facilita a transferência de líquidos. Essa vidraria é de uso geral e é útil para realizar misturas e dissolver substâncias em experimentos;
III. É utilizada para medir e transferir líquidos, podendo ser possível controlar o escoamento do material, rápido ou por gotejamento, pois a torneira na extremidade da vidraria permite fazer esse controle. Essa vidraria é amplamente utilizada em titulações, para comportar a substância titulante;
IV. É utilizada para preparar soluções, armazená-las e realizar experimentos que necessitem de aquecimento. Em processos de titulação, essa vidraria geralmente é utilizada para comportar a substância que vai ser titulada.
Com base na análise dos itens I a IV, assinale a opção CORRETA:
I. Suporta elevadas temperaturas, tem formato arredondado e permite aquecimento uniforme. Essa vidraria é utilizada em processos de destilação, sistemas de evaporação a vácuo e refluxo;
II. É utilizada para medição de volumes, em que não é requerida precisão, e a presença de um bico facilita a transferência de líquidos. Essa vidraria é de uso geral e é útil para realizar misturas e dissolver substâncias em experimentos;
III. É utilizada para medir e transferir líquidos, podendo ser possível controlar o escoamento do material, rápido ou por gotejamento, pois a torneira na extremidade da vidraria permite fazer esse controle. Essa vidraria é amplamente utilizada em titulações, para comportar a substância titulante;
IV. É utilizada para preparar soluções, armazená-las e realizar experimentos que necessitem de aquecimento. Em processos de titulação, essa vidraria geralmente é utilizada para comportar a substância que vai ser titulada.
Com base na análise dos itens I a IV, assinale a opção CORRETA:
Provas
Questão presente nas seguintes provas
A legislação brasileira que dispõe sobre as condições e padrões de lançamento de efluentes, Resolução n°
430/2011, do Conselho Nacional do Meio Ambiente - CONAMA, por meio de decretos e resoluções, estabelece
uma série de orientações acerca do tema. Analisando os itens a seguir:
I. Os efluentes não poderão conferir ao corpo receptor características de qualidade em desacordo com as metas obrigatórias progressivas, intermediárias e final do seu enquadramento;
II. O estudo de capacidade de suporte deve considerar, no mínimo, a diferença entre os padrões estabelecidos pela classe e as concentrações existentes no trecho desde a montante, estimando a concentração após a zona de mistura;
III. É vedado, nos efluentes, o lançamento dos Poluentes Orgânicos Persistentes - POPs, observada a legislação em vigor;
IV. O lançamento de efluentes em corpos de água, com exceção daqueles enquadrados na classe especial, não poderá exceder as condições e padrões de qualidade de água estabelecidos para as respectivas classes.
Assinale a opção CORRETA:
I. Os efluentes não poderão conferir ao corpo receptor características de qualidade em desacordo com as metas obrigatórias progressivas, intermediárias e final do seu enquadramento;
II. O estudo de capacidade de suporte deve considerar, no mínimo, a diferença entre os padrões estabelecidos pela classe e as concentrações existentes no trecho desde a montante, estimando a concentração após a zona de mistura;
III. É vedado, nos efluentes, o lançamento dos Poluentes Orgânicos Persistentes - POPs, observada a legislação em vigor;
IV. O lançamento de efluentes em corpos de água, com exceção daqueles enquadrados na classe especial, não poderá exceder as condições e padrões de qualidade de água estabelecidos para as respectivas classes.
Assinale a opção CORRETA:
Provas
Questão presente nas seguintes provas
Um técnico de laboratório encontrou um frasco contendo um sólido com a seguinte informação, “indicador ácido
(Ka = 5,0 x 10-5
)”. Consultando um manual de soluções disponível, o técnico informou-se de que o indicador em
questão apresenta duas colorações distintas em meio aquoso, dependendo se ele está na sua forma “protonada”
ou “desprotonada”, sendo elas AMARELA e AZUL, respectivamente. Diante das informações, assinale a opção
que mostra o VALOR DE pH, no qual uma solução do indicador se apresentará com coloração VERDE:
Dado eventualmente necessário: log(5) = 0,70.
Provas
Questão presente nas seguintes provas
As ligas metálicas de zinco e cobre, conhecidas como latões, têm amplo interesse comercial, sendo utilizadas na
indústria automotiva (em peças, engrenagens, rolamentos, molas e componentes do sistema de freio), indústria
da construção (na fabricação de tubos, conexões, ferragens e telhas), entre muitas outras aplicações. Tal
versatilidade está relacionada com a sua resistência à corrosão, durabilidade e facilidade de usinagem.
Na análise de um pedaço de latão, uma amostra da liga de 2,616 g foi colocada em um erlenmeyer de 250 mL e
dissolvida (em uma capela) com 5,00 mL de uma mistura de ácido nítrico e ácido clorídrico, ambos
concentrados. Após a completa dissolução, a solução resultante foi transferida quantitativamente para um balão
volumétrico de 250 mL, ajustando-se o menisco com água deionizada. Uma alíquota de 25,00 mL da solução de
amostra foi ajustada para pH 5,5 e titulada com solução de EDTA 0,100 mol/L usando um indicador apropriado.
O volume de EDTA gasto foi de 32,00 mL e, nestas condições, sabe-se que ambos os metais foram titulados na
forma de Zn2+ e Cu2+. Outra alíquota de 25,00 mL da solução foi ajustada para pH neutro, observando-se a
precipitação de todo o zinco na forma de hidróxido. A esta mistura adicionou-se, a seguir, iodeto de potássio em
excesso, para a formação de iodo segundo a reação: 2 Cu2+ (aq) + 4 I- (aq) ➝ 2 CuI(s) + I2.
Na sequência o iodo foi titulado com tiossulfato de sódio a 0,100 mol/L até o ponto final, com o gasto de 30,00 mL de titulante. Esta última reação foi: I2 + 2 S2O2-3(aq) ➝ 2 I-(aq) + S4O2-6(aq).
Diante das informações, assinale a opção que mostra A PORCENTAGEM EM MASSA DE ZINCO NA AMOSTRA de latão: Dados: massas molares (g/mol): Cu = 63,5; Zn = 65,4.
Na sequência o iodo foi titulado com tiossulfato de sódio a 0,100 mol/L até o ponto final, com o gasto de 30,00 mL de titulante. Esta última reação foi: I2 + 2 S2O2-3(aq) ➝ 2 I-(aq) + S4O2-6(aq).
Diante das informações, assinale a opção que mostra A PORCENTAGEM EM MASSA DE ZINCO NA AMOSTRA de latão: Dados: massas molares (g/mol): Cu = 63,5; Zn = 65,4.
Provas
Questão presente nas seguintes provas
Dadas as afirmações abaixo, julgue-as como Verdadeira (V) ou Falsa (F).
I. A uma temperatura fixa, uma solução aquosa saturada de um determinado soluto sempre contém uma quantidade fixa desse soluto;
II. Todos os líquidos fervem a uma temperatura superior ao seu ponto de ebulição normal quando contêm impurezas não voláteis;
III. Toda solução comporta-se como uma solução ideal.
Com base na análise dos itens I, II e III, assinale a opção CORRETA:
I. A uma temperatura fixa, uma solução aquosa saturada de um determinado soluto sempre contém uma quantidade fixa desse soluto;
II. Todos os líquidos fervem a uma temperatura superior ao seu ponto de ebulição normal quando contêm impurezas não voláteis;
III. Toda solução comporta-se como uma solução ideal.
Com base na análise dos itens I, II e III, assinale a opção CORRETA:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container