Foram encontradas 280 questões.
A calcita é um mineral composto principalmente por carbonato de cálcio (CaCO3). Ela tem diversas aplicações
em diferentes áreas, desde a construção civil até a fabricação de produtos farmacêuticos e cosméticos. Na
indústria da construção civil, a calcita é utilizada como material de construção, especialmente como agregado em
concreto. Ela também pode ser usada como revestimento de pisos e paredes, além de ser utilizada como
matéria-prima na produção de cal. A solubilidade da calcita em água depende do pH do meio, e pode ser
calculada com o auxílio do gráfico na Figura abaixo, que apresenta as curvas dos valores das frações em mols, à
temperatura de 25 °C, para as espécies H2CO3 , HCO-3 e CO2-3
Figura: Curvas dos valores de frações em mol para: ácido carbônico - linha pontilhada; bicarbonato - linha tracejada; carbonato - linha sólida.
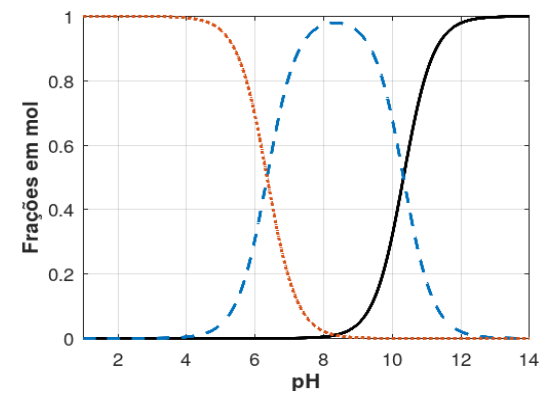
A partir das informações acima e sabendo que o Kps (constante produto de solubilidade) do CaCO3(s) (Calcita) é 4,5 x 10-9 , a 25°C , assinale a opção que mostra o valor aproximado da SOLUBILIDADE MOLAR deste carbonato, em pH 10: Dados eventualmente necessários:√4,5 = 2,12; √6,25 = 2,5; √3 = 1,73; √5 = 2,24; √10 = 3,16; √20 = 4,47.
Figura: Curvas dos valores de frações em mol para: ácido carbônico - linha pontilhada; bicarbonato - linha tracejada; carbonato - linha sólida.

A partir das informações acima e sabendo que o Kps (constante produto de solubilidade) do CaCO3(s) (Calcita) é 4,5 x 10-9 , a 25°C , assinale a opção que mostra o valor aproximado da SOLUBILIDADE MOLAR deste carbonato, em pH 10: Dados eventualmente necessários:√4,5 = 2,12; √6,25 = 2,5; √3 = 1,73; √5 = 2,24; √10 = 3,16; √20 = 4,47.
Provas
Questão presente nas seguintes provas
Um professor queria fazer uma prática de laboratório e necessitava de 10 mL de éster. Como não tinha o éster
no laboratório, ele pediu ao técnico que preparasse uma mistura de álcool, ácido e água. O técnico misturou
1,0 mol de metanol (C2H5OH), 1,0 mol de ácido etanóico (CH3COOH) e 1,0 mol de água. Depois de 30 horas a
25 °C, ao analisar a mistura, observou-se que, ao atingir o equilíbrio, 50% do ácido estava esterificado. Na
análise, o técnico descobriu que A CONSTANTE DE EQUILÍBRIO da reação é:
Provas
Questão presente nas seguintes provas
A extração sólido-líquido com aparelhagem Soxhlet é uma técnica de extração usada para separar um composto
solúvel, em um solvente, de um sólido insolúvel. O processo é usado principalmente em química orgânica para
extrair compostos de materiais sólidos, como plantas, alimentos e tecidos. O equipamento Soxhlet consiste em
três partes principais: um balão de fundo redondo, um extrator de Soxhlet e um condensador (Figura abaixo). A
amostra sólida a ser extraída é colocada num cartucho que por sua vez é inserido no extrator de Soxhlet. O
solvente é colocado no balão de fundo redondo, que é aquecido por uma fonte de calor, geralmente um banho
de água.

A respeito da aparelhagem mostrada e da técnica de extração com Soxhlet, assinale a opção CORRETA:

A respeito da aparelhagem mostrada e da técnica de extração com Soxhlet, assinale a opção CORRETA:
Provas
Questão presente nas seguintes provas
As estruturas de cristais de sólidos iônicos binários podem ser racionalizadas como um empacotamento de
átomos de um dos elementos, estando os átomos do segundo elemento preenchendo os buracos (interstícios)
formados pelo primeiro. Considere uma célula unitária cúbica de face centrada de um composto iônico com
fórmula XY (Figura abaixo). Na estrutura mostrada, as esferas mais claras representam o elemento Y e os sítios
marcados com esferas pretas representam os interstícios tetraédricos (como pode ser visto pelo tetraedro
desenhado dentro da célula unitária).
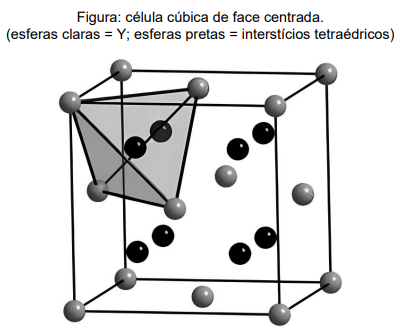
Sabe-se que, na célula apresentada, 1/8 (um oitavo) dos elementos nos vértices contribuem efetivamente para o retículo, enquanto os elementos nas faces contribuem com 1/2 (um meio). Diante das informações citadas, assinale a opção que mostra o número de INTERSTÍCIOS TETRAÉDRICOS, na célula cúbica mostrada, OCUPADOS PELO ELEMENTO X:

Sabe-se que, na célula apresentada, 1/8 (um oitavo) dos elementos nos vértices contribuem efetivamente para o retículo, enquanto os elementos nas faces contribuem com 1/2 (um meio). Diante das informações citadas, assinale a opção que mostra o número de INTERSTÍCIOS TETRAÉDRICOS, na célula cúbica mostrada, OCUPADOS PELO ELEMENTO X:
Provas
Questão presente nas seguintes provas
Uma antiga versão de um bafômetro é baseada na reação de oxidação do etanol formando ácido acético pela
ação do dicromato, conforme a reação mostrada abaixo:
Através da corrente elétrica gerada no dispositivo é calculada a massa de álcool exalada pela pessoa. A seguir, para obter o teor de álcool no sangue do indivíduo é utilizada a correlação:
Concentração de álcool no sangue, em g/mL = 2000 x (Concentração de álcool no sopro, em g/mL). Se em um teste é realizado um sopro de 50 mL, registrando-se uma corrente de 0,2 A (ampéres) durante 30 segundos, qual o teor de álcool no sangue dessa pessoa?
Assinale a opção CORRETA: Dados eventualmente necessários: Massa molar do etanol = 46 g/mol; 1 A = 1 Coulomb/s; Constante de Faraday, F = 96500 C/(mol de e- ).
Através da corrente elétrica gerada no dispositivo é calculada a massa de álcool exalada pela pessoa. A seguir, para obter o teor de álcool no sangue do indivíduo é utilizada a correlação:
Concentração de álcool no sangue, em g/mL = 2000 x (Concentração de álcool no sopro, em g/mL). Se em um teste é realizado um sopro de 50 mL, registrando-se uma corrente de 0,2 A (ampéres) durante 30 segundos, qual o teor de álcool no sangue dessa pessoa?
Assinale a opção CORRETA: Dados eventualmente necessários: Massa molar do etanol = 46 g/mol; 1 A = 1 Coulomb/s; Constante de Faraday, F = 96500 C/(mol de e- ).
Provas
Questão presente nas seguintes provas
A reação de decomposição de um composto gasoso de fórmula molecular A2B ocorre segundo a equação
química: 2 A2B(g) → 2 A2(g) + B2(g). Os dados mostrados na Tabela abaixo foram coletados num estudo da
cinética dessa reação, através do método da velocidade inicial. Neste estudo, concluiu-se que: 1) o mecanismo
reacional (em termos das etapas elementares) é o mesmo entre as temperaturas de 500 e 700 K; e 2) a
magnitude da constante de velocidade, entre as mesmas temperaturas, é diretamente proporcional à
temperatura absoluta.
Tabela: Dados obtidos na investigação cinética (método da velocidade inicial) para a reação: 2 A2B(g) → 2 A2(g) + B2(g).
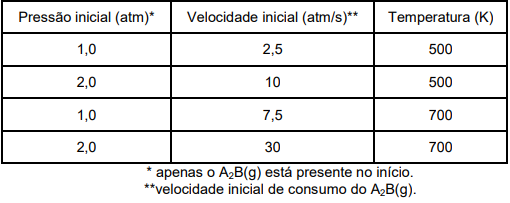
Diante das informações acima, assinale a opção que mostra A VELOCIDADE DA REAÇÃO (em termos de consumo do A2B(g)), em atm/s, quando a pressão de A2B(g) é igual a 1,5 atm à temperatura de 600 K:
Tabela: Dados obtidos na investigação cinética (método da velocidade inicial) para a reação: 2 A2B(g) → 2 A2(g) + B2(g).

Diante das informações acima, assinale a opção que mostra A VELOCIDADE DA REAÇÃO (em termos de consumo do A2B(g)), em atm/s, quando a pressão de A2B(g) é igual a 1,5 atm à temperatura de 600 K:
Provas
Questão presente nas seguintes provas
Em uma cidade, com temperaturas bem amenas, uma dona de casa esqueceu uma amostra de leite fora da
geladeira e observou que o leite azedou em 64 horas, à temperatura de 20 °C. Logo depois, esta mesma dona
de casa observou que ao deixar na geladeira, a 3 °C, o leite pode ser armazenado por um período de tempo três
vezes maior que a 20 °C, antes de azedar. Com base nessas informações, podemos dizer que a ENERGIA DE
ATIVAÇÃO do processo envolvido é:
Dados eventualmente necessários: constante universal dos gases ideais, R = 8,314 J/mol.K = 2 cal/mol.K; ln(3) = 1,1; (276)-1 = 0,0036; (293)-1 = 0,0034; (313)-1 = 0,0032.
Dados eventualmente necessários: constante universal dos gases ideais, R = 8,314 J/mol.K = 2 cal/mol.K; ln(3) = 1,1; (276)-1 = 0,0036; (293)-1 = 0,0034; (313)-1 = 0,0032.
Provas
Questão presente nas seguintes provas
A autoionização da água é um processo muito importante, pois dependendo da sua posição de equilíbrio
químico, define-se a acidez (ou alcalinidade) das soluções aquosas. Através de experimentos de condutividade
elétrica da água pura e da sua condutância específica, é possível determinar o grau de ionização da água e,
posteriormente, a constante de equilíbrio, Kw, da reação de autoionização. A 25 °C, o valor de Kw é 1,00 x 10-14
.
Por outro lado, para a água pura, a 37 °C, o grau de ionização é 73% maior, tendo em vista que a autoionização
da água é endotérmica. Vale ressaltar que nesta variação de temperatura a concentração molar da água é
praticamente invariável.
Diante das informações e a partir dos seus conhecimentos, assinale a opção que mostra aproximadamente O VALOR DO pOH de uma solução de pH 8,50, a 37 °C:
Dados: densidade da água = 1000 g/L; massa molar da água = 18 g/mol; log(1,73) = 0,24; log(3) = 0,48.
Diante das informações e a partir dos seus conhecimentos, assinale a opção que mostra aproximadamente O VALOR DO pOH de uma solução de pH 8,50, a 37 °C:
Dados: densidade da água = 1000 g/L; massa molar da água = 18 g/mol; log(1,73) = 0,24; log(3) = 0,48.
Provas
Questão presente nas seguintes provas
Num laboratório de Química, para preparar uma solução de ácido sulfúrico é importante seguir algumas
precauções de segurança. Num desses preparos, um técnico dispunha de um banho de gelo e outros materiais,
mostrados na Figura abaixo. O rótulo do produto (ácido sulfúrico concentrado) também é reproduzido
parcialmente, com algumas informações importantes.
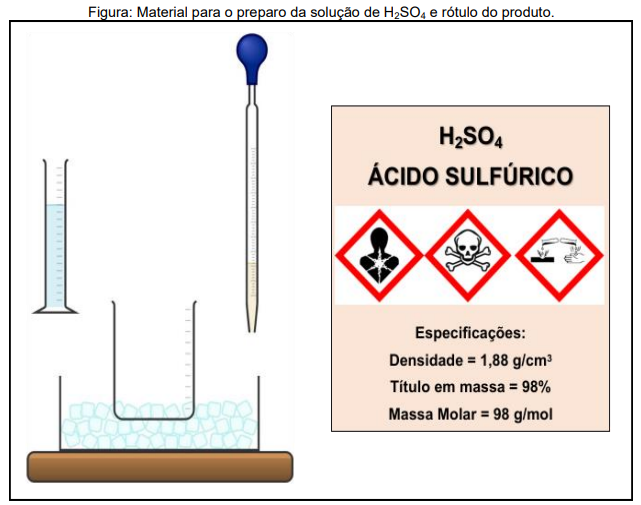
A respeito da preparação da solução de ácido sulfúrico e dos elementos na Figura acima, assinale a opção INCORRETA: Dado: considere a densidade da água = 1 g/mL.

A respeito da preparação da solução de ácido sulfúrico e dos elementos na Figura acima, assinale a opção INCORRETA: Dado: considere a densidade da água = 1 g/mL.
Provas
Questão presente nas seguintes provas
Um certo ácido orgânico, Y, encontra-se parcialmente na forma de dímeros (reação: 2Y(g) ⇌ Y2(g) ), quando em
fase de vapor. Na temperatura de 298 K e sob pressão total de 0,200 atm, este ácido tem um grau de
dimerização de 90%.
Diante dessas informações, assinale a opção que mostra O VALOR DA CONSTANTE DE EQUILÍBRIO, Kp, para a reação de dimerização e a afirmação CORRETA que expressa a influência da pressão (FAVORECE OU DESFAVORECE) na dimerização:
Diante dessas informações, assinale a opção que mostra O VALOR DA CONSTANTE DE EQUILÍBRIO, Kp, para a reação de dimerização e a afirmação CORRETA que expressa a influência da pressão (FAVORECE OU DESFAVORECE) na dimerização:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container