Foram encontradas 40 questões.
- Química Orgânica
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
A síntese de p-nitroanilina é um experimento clássico em disciplinas de Química Orgânica Experimental, pois essa rota permite a
abordagem de inúmeros tópicos dos Programas de Química Orgânica adotados por várias instituições de ensino superior. A figura a
seguir apresenta, esquematicamente e de forma resumida, uma rota sintética para a obtenção de para-nitroanilina a partir da anilina.
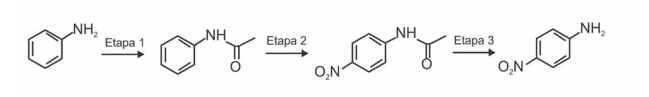
Dados do procedimento experimental da literatura: 10,00 g de p-nitroacetanilida; 50,00 mL de solução aquosa de ácido sulfúrico 50% (V/V); solução aquosa de hidróxido de sódio 20% (m/V).
Outras informações: ácido sulfúrico concentrado: densidade = 1,84 g/cm3; massas atômicas aproximadas (g/mol): C = 12,00; H = 1,00; N = 14,00; O = 16,00; Na = 23,00; S = 32,06.
Considerando que a pureza do hidróxido de sódio seja de 90% (m/m), a quantidade de NaOH(s), em gramas, necessária para atender a demanda dessa aula experimental é de:
Provas
Questão presente nas seguintes provas
A síntese de p-nitroanilina é um experimento clássico em disciplinas de Química Orgânica Experimental, pois essa rota permite a
abordagem de inúmeros tópicos dos Programas de Química Orgânica adotados por várias instituições de ensino superior. A figura a
seguir apresenta, esquematicamente e de forma resumida, uma rota sintética para a obtenção de para-nitroanilina a partir da anilina.

Provas
Questão presente nas seguintes provas
A síntese de p-nitroanilina é um experimento clássico em disciplinas de Química Orgânica Experimental, pois essa rota permite a
abordagem de inúmeros tópicos dos Programas de Química Orgânica adotados por várias instituições de ensino superior. A figura a
seguir apresenta, esquematicamente e de forma resumida, uma rota sintética para a obtenção de para-nitroanilina a partir da anilina.

1. A acetanilida pode ser obtida por reação de anilina com cloreto de acetila.
2. A reação da Etapa 2 é uma reação de substituição nucleofílica.
3. A p-nitroanilina pode ser transformada em p-nitrofenol.
4. A acetanilida possui um anel aromático desativado para SEAr.
Assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- Química OrgânicaIsomeria Plana e Espacial
O estereoisômero (S)-2-bromobutano apresenta rotação específica de +23,1º. Uma mistura dos dois enantiômeros
apresentou rotação específica de +4,6º. A respeito dessa mistura, considere as seguintes afirmativas:
1. A pureza óptica da mistura citada é de 20%.
2. Os dois isômeros apresentam o mesmo valor de ponto de ebulição.
3. A mistura analisada é uma mistura racêmica.
4. Os dois componentes da mistura apresentada não podem ser separados.
Assinale a alternativa correta.
1. A pureza óptica da mistura citada é de 20%.
2. Os dois isômeros apresentam o mesmo valor de ponto de ebulição.
3. A mistura analisada é uma mistura racêmica.
4. Os dois componentes da mistura apresentada não podem ser separados.
Assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
Um artigo científico que tratava de compostos com atividades flavorizantes mostrava diversos espectros de
ressonância magnética nuclear de hidrogênio para a comprovação da estrutura química da série de ésteres estudados
pelo autor. O revisor do artigo solicitou que, em lugar da figura dos espectros, fosse apresentada apenas a descrição
textual contendo o assinalamento dos picos, a multiplicidade e as demais informações pertinentes a cada composto.
Um dos espectros apresentados no artigo pode ser transcrito como:
RMN de 1H (400 MHz, CDCl3, TMS), δ (ppm): 4,12 (q, J = 7,1 Hz, 2H); 2,04 (s, 3H); 1,26 (t, J = 7,1 Hz, 3H).
O espectro de RMN de 1H descrito corresponde ao composto:
RMN de 1H (400 MHz, CDCl3, TMS), δ (ppm): 4,12 (q, J = 7,1 Hz, 2H); 2,04 (s, 3H); 1,26 (t, J = 7,1 Hz, 3H).
O espectro de RMN de 1H descrito corresponde ao composto:
Provas
Questão presente nas seguintes provas
A funcionalização de polímeros pré-formados é uma técnica utilizada para a reutilização de artefatos plásticos
pós-consumo (reciclagem química) que pode alterar as propriedades do material inicial, permitindo uma nova
aplicação, o aumento da vida útil e a consequente proteção do meio ambiente, pela redução do lixo plástico. Artefatos
de poliestireno (PS) pós-uso podem sofrer reações de substituição eletrofílica aromática, como a sulfonação, gerando
copolímeros que, dependendo do teor de grupos sulfônicos introduzidos na cadeia polimérica, podem ser utilizados
como catalisadores ou trocadores de íons em processos de purificação de água, entre outras aplicações. Um
experimento de sulfonação parcial de PS gerou um copolímero de poliestireno e poliestireno sulfonado (PS-SPS),
conforme figura a seguir, cujo teor de grupos sulfônicos foi determinado por volumetria de neutralização, utilizando-se
solução de hidróxido de potássio 0,01 mol/L recém padronizada.
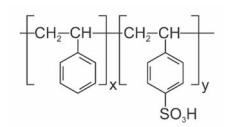
Considerando que a titulação de amostras de 150,00 mg de PS-SPS consumiu, em média, 20,00 mL da solução titulante, assinale o valor que mais se aproxima do grau de sulfonação do PS-SPS, expresso em mol%.

Considerando que a titulação de amostras de 150,00 mg de PS-SPS consumiu, em média, 20,00 mL da solução titulante, assinale o valor que mais se aproxima do grau de sulfonação do PS-SPS, expresso em mol%.
Provas
Questão presente nas seguintes provas
A Síntese Orgânica utiliza frequentemente a cromatografia em camada delgada (CCD) para acompanhar a progressão
de uma reação química e a identificação dos produtos formados. A partir da acetofenona (acetil-benzeno), dois
experimentos de redução foram conduzidos, em paralelo: uma redução com hidreto de boro e sódio [1) NaBH4/CH3OH;
2) H3O+] que gerou 1-feniletanol; e um experimento de redução usando amálgama de zinco em meio ácido [Zn-Hg/HCl],
que produziu etilbenzeno. As duas reações foram monitoradas por CCD utilizando-se uma cromatoplaca de sílica gel,
como fase estacionária, sobre a qual foram aplicadas uma amostra de cada composto orgânico citado. O experimento
de CCD foi corretamente conduzido, e os valores do Índice de Retenção (Rf) foram determinados utilizando-se uma
mistura de hexano:acetato de etila 4:1 (V/V) como eluente.
Na cromatoplaca, em ordem decrescente do Rf, observam-se os seguintes compostos, em sequência:
Na cromatoplaca, em ordem decrescente do Rf, observam-se os seguintes compostos, em sequência:
Provas
Questão presente nas seguintes provas
Soluções-tampão são misturas que contêm um ácido fraco e sua base conjugada, ou uma base fraca e seu ácido
conjugado. Essas soluções são resistentes à mudança de pH por diluição ou adição de pequenas quantidades de
ácidos ou bases. Pode-se calcular o pH de uma solução-tampão utilizando-se a equação de Henderson-Hasselbalch,
como para o tampão ácido acético (HOAc) / acetato de sódio (NaOAc):
pH = pKa + log([OAc–] / [HOAC])
Com relação a esse exemplo, assinale a alternativa correta.
pH = pKa + log([OAc–] / [HOAC])
Com relação a esse exemplo, assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
A contaminação de mercúrio (Hg0) no ar pode ser determinada pela passagem de uma corrente de ar por uma solução
ácida de permanganato de potássio (KMnO4). O excesso de permanganato é eliminado com hidroxilamina, e o mercúrio
(Hg+2) absorvido pela solução é precipitado, na forma de Hg0, finamente dividido, pela adição de cloreto estanoso
(SnCl2). O mercúrio metálico é então analisado por absorção atômica. As equações a seguir ilustram o processo:
5 Hg0 + 2 MnO4 – +16 H+ → 5 Hg+2 + 2 Mn+2 + 8 H2O
6 MnO4 – + 5 NH2OH + 13 H+ → 6 Mn+2 + 5 NO3 – + 14 H2O
Hg+2 + SnCl2 + 2 Cl – → Hg0 + SnCl4
Com relação ao procedimento descrito, é correto afirmar:
5 Hg0 + 2 MnO4 – +16 H+ → 5 Hg+2 + 2 Mn+2 + 8 H2O
6 MnO4 – + 5 NH2OH + 13 H+ → 6 Mn+2 + 5 NO3 – + 14 H2O
Hg+2 + SnCl2 + 2 Cl – → Hg0 + SnCl4
Com relação ao procedimento descrito, é correto afirmar:
Provas
Questão presente nas seguintes provas
A bomba calorimétrica é um equipamento utilizado para a determinação do poder calorífico de amostras sólidas ou
líquidas por meio da combustão das amostras em atmosfera com excesso de oxigênio. Nesse aparato, pode-se medir
o calor de combustão de substâncias puras, como o naftaleno (C10H8), cuja reação de combustão completa não
balanceada é:
C10H8 + O2 → CO2 + H2O
Considerando que uma massa m de naftaleno foi queimada em uma bomba calorimétrica (V constante) de capacidade calorífica Cc, (J/°C), indicando uma variação de temperatura Δt (°C), e que os gases são ideais e o volume dos sólidos e líquidos é desprezível, assinale a alternativa que apresenta corretamente a expressão da variação de entalpia de combustão (ΔH) do naftaleno.
Dados: MM (naftaleno) = 128 g/mol; P = pressão (kPa); V = volume (L); R = constante universal dos gases perfeitos (J/mol.K); T = temperatura absoluta (K); e ΔH = ΔU + (PV), em que ΔU é a variação da energia interna do sistema (J).
C10H8 + O2 → CO2 + H2O
Considerando que uma massa m de naftaleno foi queimada em uma bomba calorimétrica (V constante) de capacidade calorífica Cc, (J/°C), indicando uma variação de temperatura Δt (°C), e que os gases são ideais e o volume dos sólidos e líquidos é desprezível, assinale a alternativa que apresenta corretamente a expressão da variação de entalpia de combustão (ΔH) do naftaleno.
Dados: MM (naftaleno) = 128 g/mol; P = pressão (kPa); V = volume (L); R = constante universal dos gases perfeitos (J/mol.K); T = temperatura absoluta (K); e ΔH = ΔU + (PV), em que ΔU é a variação da energia interna do sistema (J).
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container