Foram encontradas 50 questões.
O composto puro que pode formar ligação hidrogênio é o da alternativa
Provas
Alguns compostos naturais contêm mais de um grupo funcional.
Analise o composto a seguir.
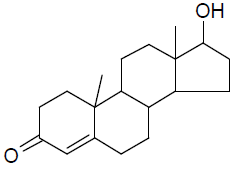
Os grupos no composto acima são identificados por
Provas
Considere o composto a seguir.
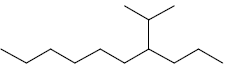
A nomenclatura correspondente a esse composto é
Provas
Um composto orgânico X apresenta os quatro átomos de hidrogênio do metano substituídos pelos radicais isopropil, benzil, hidroxi e metil.
A fórmula molecular de X é
Provas
Os ésteres são, algumas vezes, obtidos pela reação de um ácido carboxílico e um álcool. São encontrados abundantemente na natureza e quando apresentam pequeno número de átomos de carbono, podem ser classificados como essências, exemplificadas na tabela a seguir.
| Essência |
Éster |
| abacaxi |
butanoato de etila |
| laranja |
acetato de n-octila |
| banana |
acetato de isoamila |
Os álcoois produzidos pela hidrólise ácida das essências de abacaxi, laranja e banana são, respectivamente,
Provas
As ligações químicas nos compostos orgânicos podem ser do tipo \( σ \) ou \( \pi \). A ligação \( σ \) é formada pela interação de dois orbitais atômicos, segundo o eixo que une os dois átomos, ao passo que, na ligação \( \pi \), a interação dos orbitais atômicos se faz segundo o plano que contém o eixo da ligação.
Analise a estrutura a seguir.
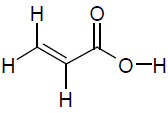
Na estrutura representada acima, tem-se
Provas
Os fenóis são compostos orgânicos oxigenados. Muitos são utilizados como desinfetantes para uso doméstico.
Indica-se, a seguir, as estruturas de alguns fenóis.
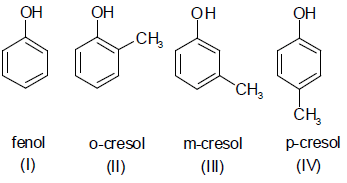
Considere a reação a seguir.
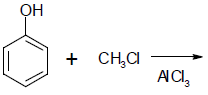
Nessa reação, os produtos principais são os que apresentam suas estruturas indicadas por
Provas
Sabe-se que um composto orgânico pode ser obtido a partir da reação de ozonólise do but-2-eno. O composto a que se faz referência é o
Provas
Na célula eletroquímica Al0/Al3+//Fe2+/Fe0, é CORRETO afirmar que
Provas
Considere os dados a seguir.
\( \Delta \)Hform do CH4 (g) = –17 kcal mol–1
\( \Delta \)Hform do O2 (g) = zero
\( \Delta \)Hform do CO2 (g) = – 94 kcal mol–1
\( \Delta \)Hform do H2O (
O \( \Delta \)H do processo CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (
Provas
Caderno Container