Foram encontradas 225 questões.
Dadas as vidrarias listadas na primeira coluna, correlacione-as com sua utilidade descrita na segunda coluna:
I. Funil de decantação ( ) Destilação simples
II. Funil analítico ( ) Filtração a vácuo
III. Erlenmeyer ( ) Titulação
IV. Kitassato ( ) Extração por solvente
V. Condensador ( ) Filtração simples
Assinale a alternativa que apresenta CORRETAMENTE a sequência da segunda coluna, de cima para baixo:
Provas
Em solução aquosa na presença de íons iodeto, ocorre um equilíbrio químico entre o ácido arsênico e o ácido arsenioso, representado pela seguinte reação:
H3AsO4(aq) + 3 I-(aq) + 2 H+(aq) ⇌ H3AsO3(aq) + I3-(aq) + H2O(l)
Considerando o sistema em equilíbrio, o Princípio de Le Chatelier e o fato de uma solução contendo o íon triiodeto apresentar a cor azul na presença de amido, um estudante fez as seguintes afirmações:
I. A adição de solução aquosa de hidróxido de sódio e solução de amido torna a solução azul.
II. A adição de solução aquosa de ácido clorídrico favorece a formação de ácido arsenioso.
III. A adição de solução aquosa de iodeto de potássio e solução de amido não produz alteração na coloração da solução.
IV. Com o aumento do pH do meio reacional, ocorrerá o deslocamento do equilíbrio no sentido de formação do ácido arsênico.
Está CORRETO o que se afirma apenas em:
Provas
A substância Vincristina é um alcaloide obtido da planta Catharanthus roseus, utilizado como quimioterápico no tratamento de leucemia. A figura abaixo apresenta a estrutura química deste alcaloide.
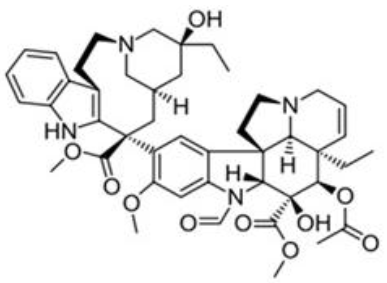
Vincristina
Analisando a estrutura química acima, considere as afirmativas a seguir:
I. A Vincristina possui função cetona em sua estrutura.
II. A Vincristina não é um aromático.
III. Existem duas ligações duplas entre átomos de carbono fora do anel aromático.
IV. A função álcool está presente na molécula três vezes.
V. Existe pelo menos uma amina terciária na estrutura da Vincristina.
VI. Existem ao menos 2 ésteres na estrutura química da Vincristina.
Está CORRETO o que se afirma apenas em:
Provas
Considere as seguintes substâncias químicas:
I. H3PO4
II. NaHCO3
III. SO3
IV. HClO4
V. Ca(OH)2
Com base nas estruturas químicas das substâncias apresentadas acima, assinale a afirmativa INCORRETA:
Provas
Uma indústria farmacêutica produz água oxigenada 10 volumes e necessita de realizar o controle de qualidade periódica de cada lote produzido. A análise realizada para o controle de qualidade envolve a reação entre a água oxigenada ou peróxido de hidrogênio e uma solução de permanganato, conforme a reação dada:
KMnO4(aq) + H2O2(aq) + H2SO4(aq) → MnSO4(aq) + K2SO4(aq) + O2(g) + H2O(l).
A partir desta reação, afirma-se que:
I. a reação ocorre em meio ácido.
II. a soma dos coeficientes dos reagentes é igual a 10.
III. a soma dos coeficientes dos produtos é igual a 15.
IV. o KMnO4 é o agente redutor.
V. o número total de elétrons transferidos no processo é igual a 10.
Está CORRETO o que se afirma apenas em:
Provas
O etanol (C2H5OH) é um composto orgânico da classe ou função álcool e é produzido no Brasil principalmente a partir da destilação do caldo de cana fermentado. Ele é utilizado em várias atividades econômicas, incluindo o uso como combustível alternativo aos derivados de petróleo. As reações envolvendo a combustão do etanol são apresentadas a seguir:
1. H2O(l) ⇌ H2O(g), ΔH1 = + 44,0 kJ
2. C2H5OH(l) ⇌ C2H5OH(g), ΔH2 = + 42,6 kJ
3. C2H5OH(l) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(l), ΔH3 = - 1366,8 kJ
4. C2H5OH(l) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(g), ΔH4 = ?
5. C2H5OH(g) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(l), ΔH5 = ?
6. C2H5OH(g) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(g), ΔH6 = ?
Com base no exposto acima, considere as afirmativas a seguir, atribuindo V para a(s) verdadeira(s) e F para a(s) falsa(s):
( ) A reação 1 é exotérmica.
( ) O valor calculado para ΔH6 é de -1277,4 kJ.
( ) O valor de ΔH5 é menor que o valor de ΔH4.
( ) A reação 5 é a que libera mais energia dentre todas as reações apresentadas.
A sequência CORRETA é:
Provas
Considerando os seguintes compostos e seus nomes, faça a correlação do nome do composto com sua fórmula química:
A. Butanal I. CH3CH2OCH2CH2CH3
B. Etoxipropano II. CH3CH2COCH3
C. Metanoato de butila III. CH3NHCH2CH3
D. Butanona IV. CH3CH2CH2COH
E. Metiletilamina V. CH3CH2CH2CH2OCHO
Assinale a alternativa que apresenta a associação CORRETA:
Provas
A Tabela Periódica dos elementos químicos foi elaborada originalmente por Mendeleev e aprimorada por diversos outros cientistas. Nela, os elementos estão dispostos em ordem crescente de seus números atômicos, e por meio dela podemos avaliar a tendência de algumas propriedades químicas dos elementos, tais como Energia de Ionização (EI), Afinidade Eletrônica (AE), Raio Atômico (RA), além da Eletronegatividade (EM).
Ao avaliarmos a Energia de Ionização dos elementos químicos, observamos que, quanto maior a energia de ionização de um elemento químico, mais difícil é para ele:
Provas
As substâncias Fe2O3, AlCl3, BaI2 e K2S possuem como características em comum:
Provas
O elemento Fe, extraído da natureza na forma de Fe2O3, e utilizado na produção de aço, é classificado como um metal de transição, possuindo 26 prótons e 30 nêutrons. Quando recebe energia suficiente, se transforma no íon Fe3+. Assinale a alternativa que apresenta CORRETAMENTE a distribuição eletrônica do íon Fe3+:
Provas
Caderno Container