Foram encontradas 35 questões.
A tabela abaixo apresenta alguns elementos químicos muito utilizados na indústria, em vários processos:
|
Semirreação de redução |
Eº (V) |
|
Al3+ + 3 e- ⇌ Alº |
-1,66 |
|
Mn2+ + 2 e- ⇌ Mnº |
-1,18 |
|
Zn2+ + 2 e- ⇌ Znº |
-0,76 |
|
Cr3+ + 3 e- ⇌ Crº |
-0,74 |
|
Fe2+ + 2 e- ⇌ Feº |
-0,44 |
|
Ni2+ + 2 e- ⇌ Niº |
-0,25 |
|
Sn2+ + 2 e- ⇌ Snº |
-0,14 |
|
Pb2+ + 2 e- ⇌ Pbº |
-0,13 |
|
Cu2+ + 2 e- ⇌ Cuº |
+0,34 |
|
Fe3+ + e- ⇌ Fe2+ |
+0,77 |
|
Ag+ + e- ⇌ Agº |
+0,80 |
|
Au3+ + 3 e- ⇌ Auº |
+1,50 |
De acordo com as reações de redução e seus respectivos potenciais de redução padrão informadas na tabela acima, podemos observar que existem diferenças na reatividade dos elementos citados. Pilhas ou sistemas eletroquímicos podem ser construídos para gerar energia elétrica a partir dessas diferenças de reatividade. Considere as afirmativas abaixo sobre pilhas, onde as soluções apresentam concentrações iônicas iguais:
I. Feº|Fe2+∥Cu2+|Cuº produz uma ddp = + 0,78V.
II. Em uma pilha utilizando Ouro e Zinco, o Ouro será o anodo.
III. Znº|Zn2+∥Cu2+|Cuº produz uma ddp menor do que a do sistema Mnº|Mn2+∥ Cu2+|Cuº.
IV. Alº|Al3+∥Fe3+|Feº produz uma ddp maior do que a do sistema Crº|Cr3+∥ Fe3+|Feº.
Está CORRETO o que se afirma apenas em:
Provas
Colocou-se aleatoriamente em três béqueres A, B e C massas iguais dos seguintes líquidos incolores: água, éter etílico e tetracloreto de carbono.
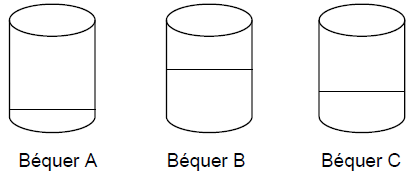
Como os béqueres não foram previamente identificados, o técnico responsável pelo laboratório verificou a densidade de cada substância para, em seguida, realizar a identificação dos líquidos. Considerando que a densidade da água seja 1,00 g.cm-3, a do éter etílico 0,79 g.cm-3 e a do tetracloreto de carbono 1,59 g.cm-3, a alternativa que apresenta CORRETAMENTE a identificação dos béqueres é:
Provas
O ácido nítrico é um importante insumo utilizado na indústria química, com destaque para a fabricação de fertilizantes e explosivos. As reações relacionadas ao processo de oxidação da amônia para se obter o ácido nítrico estão representadas por meio das três equações termoquímicas descritas a seguir:
4 NH3(g) + 5 O2(g) → 4NO(g) + 6 H2O(l) ΔH = - 1170 kJ
2 NO2(g) → 2 NO(g) + O2(g) ΔH = +114 kJ
3 NO2(g) + H2O(|) → 2 HNO3(aq) + NO(g) ΔH = - 138 kJ
Com base nas equações termoquímicas apresentadas, conclui-se que o ΔH referente à reação completa de produção de um mol do ácido nítrico aquoso e um mol de água líquida a partir da amônia e do oxigênio gasosos equivale a:
Provas
Considere as afirmativas abaixo, atribuindo V para a(s) verdadeira(s) e F para a(s) falsa(s):
( ) Reagentes como biftalato de potássio e tetraborato de sódio são padrões primários adequados para a padronização de bases e ácidos, respectivamente.
( ) Um potenciômetro, desde que conectado a um eletrodo de vidro adequado, pode ser utilizado para determinação de pH de soluções.
( ) Para medidas de absorbância de soluções coloridas, podemos usar cubetas de quartzo, vidro ou acrílico.
( ) Vidrarias como balão volumétrico, pipeta graduada, pipeta volumétrica e bureta, antes de serem utilizadas, devem ser bem lavadas com solução de detergente, enxaguadas com água destilada e secas em estufa, para evitar contaminações de reagentes e erros nas aferições de volume.
( ) Água destilada e água deionizada são exemplos de água purificada para o preparo de soluções que podem existir no laboratório. Destas, a de maior pureza é a água destilada.
( ) O preparo de soluções ácidas diluídas deve ser realizado em capela, mediante adição de volume apropriado de solução do ácido sobre volume apropriado de água.
( ) Os incêndios em laboratório, caso não haja extintor apropriado nas proximidades, devem ser controlados jogando-se água.
Assinale a sequência CORRETA:
Provas
Dadas as vidrarias listadas na primeira coluna, correlacione-as com sua utilidade descrita na segunda coluna:
I. Funil de decantação ( ) Destilação simples
II. Funil analítico ( ) Filtração a vácuo
III. Erlenmeyer ( ) Titulação
IV. Kitassato ( ) Extração por solvente
V. Condensador ( ) Filtração simples
Assinale a alternativa que apresenta CORRETAMENTE a sequência da segunda coluna, de cima para baixo:
Provas
Em solução aquosa na presença de íons iodeto, ocorre um equilíbrio químico entre o ácido arsênico e o ácido arsenioso, representado pela seguinte reação:
H3AsO4(aq) + 3 I-(aq) + 2 H+(aq) ⇌ H3AsO3(aq) + I3-(aq) + H2O(l)
Considerando o sistema em equilíbrio, o Princípio de Le Chatelier e o fato de uma solução contendo o íon triiodeto apresentar a cor azul na presença de amido, um estudante fez as seguintes afirmações:
I. A adição de solução aquosa de hidróxido de sódio e solução de amido torna a solução azul.
II. A adição de solução aquosa de ácido clorídrico favorece a formação de ácido arsenioso.
III. A adição de solução aquosa de iodeto de potássio e solução de amido não produz alteração na coloração da solução.
IV. Com o aumento do pH do meio reacional, ocorrerá o deslocamento do equilíbrio no sentido de formação do ácido arsênico.
Está CORRETO o que se afirma apenas em:
Provas
A substância Vincristina é um alcaloide obtido da planta Catharanthus roseus, utilizado como quimioterápico no tratamento de leucemia. A figura abaixo apresenta a estrutura química deste alcaloide.
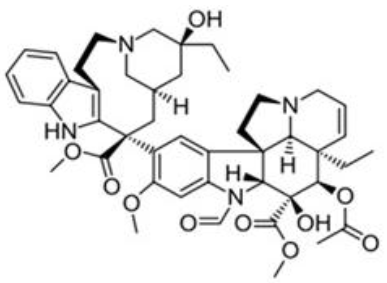
Vincristina
Analisando a estrutura química acima, considere as afirmativas a seguir:
I. A Vincristina possui função cetona em sua estrutura.
II. A Vincristina não é um aromático.
III. Existem duas ligações duplas entre átomos de carbono fora do anel aromático.
IV. A função álcool está presente na molécula três vezes.
V. Existe pelo menos uma amina terciária na estrutura da Vincristina.
VI. Existem ao menos 2 ésteres na estrutura química da Vincristina.
Está CORRETO o que se afirma apenas em:
Provas
Considere as seguintes substâncias químicas:
I. H3PO4
II. NaHCO3
III. SO3
IV. HClO4
V. Ca(OH)2
Com base nas estruturas químicas das substâncias apresentadas acima, assinale a afirmativa INCORRETA:
Provas
Uma indústria farmacêutica produz água oxigenada 10 volumes e necessita de realizar o controle de qualidade periódica de cada lote produzido. A análise realizada para o controle de qualidade envolve a reação entre a água oxigenada ou peróxido de hidrogênio e uma solução de permanganato, conforme a reação dada:
KMnO4(aq) + H2O2(aq) + H2SO4(aq) → MnSO4(aq) + K2SO4(aq) + O2(g) + H2O(l).
A partir desta reação, afirma-se que:
I. a reação ocorre em meio ácido.
II. a soma dos coeficientes dos reagentes é igual a 10.
III. a soma dos coeficientes dos produtos é igual a 15.
IV. o KMnO4 é o agente redutor.
V. o número total de elétrons transferidos no processo é igual a 10.
Está CORRETO o que se afirma apenas em:
Provas
O etanol (C2H5OH) é um composto orgânico da classe ou função álcool e é produzido no Brasil principalmente a partir da destilação do caldo de cana fermentado. Ele é utilizado em várias atividades econômicas, incluindo o uso como combustível alternativo aos derivados de petróleo. As reações envolvendo a combustão do etanol são apresentadas a seguir:
1. H2O(l) ⇌ H2O(g), ΔH1 = + 44,0 kJ
2. C2H5OH(l) ⇌ C2H5OH(g), ΔH2 = + 42,6 kJ
3. C2H5OH(l) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(l), ΔH3 = - 1366,8 kJ
4. C2H5OH(l) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(g), ΔH4 = ?
5. C2H5OH(g) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(l), ΔH5 = ?
6. C2H5OH(g) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(g), ΔH6 = ?
Com base no exposto acima, considere as afirmativas a seguir, atribuindo V para a(s) verdadeira(s) e F para a(s) falsa(s):
( ) A reação 1 é exotérmica.
( ) O valor calculado para ΔH6 é de -1277,4 kJ.
( ) O valor de ΔH5 é menor que o valor de ΔH4.
( ) A reação 5 é a que libera mais energia dentre todas as reações apresentadas.
A sequência CORRETA é:
Provas
Caderno Container