Foram encontradas 350 questões.
| substância | !$ \Delta H_f^0 (kj/mol) !$ |
| CO2 (g) | -394 |
| H2O (l) | -286 |
Considerando os valores de entalpias padrão de formação ( !$ \Delta H_f^0 !$ ), a 25 ºC, apresentados na tabela e sabendo que a f 0 entalpia padrão de combustão da glicose a 25 ºC é -2.800 kJ/mol, assinale a opção que apresenta o valor, em kJ/mol, da entalpia padrão de formação da glicose, a 25 ºC.
Provas
As sensações causadas pelos equipamentos radicais dos parques de diversão são pura química. Tudo começa quando as glândulas suprarrenais liberam glicocorticoides que estimulam a conversão de glicogênio ((C6H10O5)n) em glicose (C6H12O6), cujo metabolismo produz energia imediata para o corpo. Do núcleo das suprarrenais é secretada adrenalina, um hormônio que vai para a corrente sanguínea e aumenta a frequência cardíaca e a respiratória, além de dilatar as artérias que nutrem os músculos. A sensação de perigo iminente promove a liberação de dopamina e noradrenalina, que alertam as várias regiões cerebrais. Enfim, é a ação sinérgica dessas substâncias que, em algumas pessoas, causa o grande prazer de ir a um parque de diversões.
Internet: <www.parquedediversoes.net> (com adaptações).
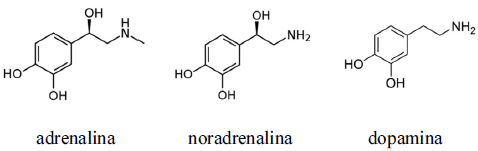
A seguir, são apresentadas as equações químicas simplificadas da conversão de glicogênio em glicose (reação I) e da oxidação da glicose (reação II) e as fórmulas estruturais dos neurotransmissores adrenalina, noradrenalina e dopamina.
reação I: (C6H10O5)n(s) + nH2O(l) → nC6H12O6 (s)
reação II: C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2 O(l)
A partir das informações acima, julgue os itens de 90 a 94 e faça o que se pede no item 95, que é do tipo C.
Sabendo-se que, no corpo humano, a dopamina pode ser convertida em noradrenalina por ação de enzimas, é correto inferir, com base na estrutura química desses neurotransmissores, que a referida conversão pode ser realizada alternativamente, em laboratório, por reação de hidratação da dopamina em meio ácido.
Provas
As sensações causadas pelos equipamentos radicais dos parques de diversão são pura química. Tudo começa quando as glândulas suprarrenais liberam glicocorticoides que estimulam a conversão de glicogênio ((C6H10O5)n) em glicose (C6H12O6), cujo metabolismo produz energia imediata para o corpo. Do núcleo das suprarrenais é secretada adrenalina, um hormônio que vai para a corrente sanguínea e aumenta a frequência cardíaca e a respiratória, além de dilatar as artérias que nutrem os músculos. A sensação de perigo iminente promove a liberação de dopamina e noradrenalina, que alertam as várias regiões cerebrais. Enfim, é a ação sinérgica dessas substâncias que, em algumas pessoas, causa o grande prazer de ir a um parque de diversões.
Internet: <www.parquedediversoes.net> (com adaptações).
A seguir, são apresentadas as equações químicas simplificadas da conversão de glicogênio em glicose (reação I) e da oxidação da glicose (reação II) e as fórmulas estruturais dos neurotransmissores adrenalina, noradrenalina e dopamina.
reação I: (C6H10O5)n(s) + nH2O(l) → nC6H12O6 (s)
reação II: C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2 O(l)

A partir das informações acima, julgue os itens de 90 a 94 e faça o que se pede no item 95, que é do tipo C.
Segundo a reação I, o glicogênio é um polímero de adição formado por monômeros de glicose.
Provas
As sensações causadas pelos equipamentos radicais dos parques de diversão são pura química. Tudo começa quando as glândulas suprarrenais liberam glicocorticoides que estimulam a conversão de glicogênio ((C6H10O5)n) em glicose (C6H12O6), cujo metabolismo produz energia imediata para o corpo. Do núcleo das suprarrenais é secretada adrenalina, um hormônio que vai para a corrente sanguínea e aumenta a frequência cardíaca e a respiratória, além de dilatar as artérias que nutrem os músculos. A sensação de perigo iminente promove a liberação de dopamina e noradrenalina, que alertam as várias regiões cerebrais. Enfim, é a ação sinérgica dessas substâncias que, em algumas pessoas, causa o grande prazer de ir a um parque de diversões.
Internet: <www.parquedediversoes.net> (com adaptações).
A seguir, são apresentadas as equações químicas simplificadas da conversão de glicogênio em glicose (reação I) e da oxidação da glicose (reação II) e as fórmulas estruturais dos neurotransmissores adrenalina, noradrenalina e dopamina.
reação I: (C6H10O5)n(s) + nH2O(l) → nC6H12O6 (s)
reação II: C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2 O(l)

A partir das informações acima, julgue os itens de 90 a 94 e faça o que se pede no item 95, que é do tipo C.
Com base nos princípios da teoria ácido-base de Lewis, a basicidade do átomo de nitrogênio dos neurotransmissores mostrados ocorre na seguinte ordem crescente: adrenalina < noradrenalina < dopamina.
Provas
As sensações causadas pelos equipamentos radicais dos parques de diversão são pura química. Tudo começa quando as glândulas suprarrenais liberam glicocorticoides que estimulam a conversão de glicogênio ((C6H10O5)n) em glicose (C6H12O6), cujo metabolismo produz energia imediata para o corpo. Do núcleo das suprarrenais é secretada adrenalina, um hormônio que vai para a corrente sanguínea e aumenta a frequência cardíaca e a respiratória, além de dilatar as artérias que nutrem os músculos. A sensação de perigo iminente promove a liberação de dopamina e noradrenalina, que alertam as várias regiões cerebrais. Enfim, é a ação sinérgica dessas substâncias que, em algumas pessoas, causa o grande prazer de ir a um parque de diversões.
Internet: <www.parquedediversoes.net> (com adaptações).
A seguir, são apresentadas as equações químicas simplificadas da conversão de glicogênio em glicose (reação I) e da oxidação da glicose (reação II) e as fórmulas estruturais dos neurotransmissores adrenalina, noradrenalina e dopamina.
reação I: (C6H10O5)n(s) + nH2O(l) → nC6H12O6 (s)
reação II: C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2 O(l)

A partir das informações acima, julgue os itens de 90 a 94 e faça o que se pede no item 95, que é do tipo C.
Na molécula de adrenalina, o carbono da cadeia alifática ligado ao grupo hidroxila possui hibridização do tipo sp3.
Provas
As sensações causadas pelos equipamentos radicais dos parques de diversão são pura química. Tudo começa quando as glândulas suprarrenais liberam glicocorticoides que estimulam a conversão de glicogênio ((C6H10O5)n) em glicose (C6H12O6), cujo metabolismo produz energia imediata para o corpo. Do núcleo das suprarrenais é secretada adrenalina, um hormônio que vai para a corrente sanguínea e aumenta a frequência cardíaca e a respiratória, além de dilatar as artérias que nutrem os músculos. A sensação de perigo iminente promove a liberação de dopamina e noradrenalina, que alertam as várias regiões cerebrais. Enfim, é a ação sinérgica dessas substâncias que, em algumas pessoas, causa o grande prazer de ir a um parque de diversões.
Internet: <www.parquedediversoes.net> (com adaptações).
A seguir, são apresentadas as equações químicas simplificadas da conversão de glicogênio em glicose (reação I) e da oxidação da glicose (reação II) e as fórmulas estruturais dos neurotransmissores adrenalina, noradrenalina e dopamina.
reação I: (C6H10O5)n(s) + nH2O(l) → nC6H12O6 (s)
reação II: C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2 O(l)

A partir das informações acima, julgue os itens de 90 a 94 e faça o que se pede no item 95, que é do tipo C.
A variação de entalpia da reação II é ilustrada corretamente no esquema abaixo.

Provas
Considere que, nas condições em que a reconstituição da água foi realizada no gasômetro de Lavoisier, tenha ocorrido uma reação cinética elementar e trimolecular. Considerando a lei de velocidade do processo, assinale a opção que apresenta o gráfico que melhor representa a dependência da velocidade (v) da reação em função da pressão parcial ( pH2 ) de gás hidrogênio no interior do gasômetro.
Provas

Internet: <www.arts-et-metiers.net>.
Em 1772, o cientista Lavoisier, em seus primeiros trabalhos sobre a combustão, mostrou que determinadas substâncias, como o fósforo, não perdem — mas ganham — massa durante o processo. Onze anos mais tarde, Lavoisier, para decompor a água, elaborou o equipamento ilustrado na figura acima e, utilizando-o, descobriu que a água é uma substância formada por dois elementos: hidrogênio e oxigênio. Em seu experimento, ele colocou em um recipiente (A) uma massa conhecida de água destilada e a fez passar sobre ferro incandescente (B), promovendo a decomposição da água e a obtenção de gás H2, que foi coletado em um recipiente indeformável (C). A seguinte equação química não balanceada retrata essa reação.
Fe(s) + H2O(l) → Fe3O4(s) + H2(g)
Em outro experimento, o gás hidrogênio produzido foi misturado ao gás oxigênio em um balão de vidro — o gasômetro de Lavoisier — e a mistura de gases foi inflamada por uma fagulha elétrica. Pronto: a água líquida tinha sido reconstituída!
Internet: <www.chc.cienciahoje.uol.com.br> (com adaptações).
Considerando o texto acima e os diversos aspectos a ele relacionados, julgue os itens de 83 a 88 e faça o que se pede no item 89, que é do tipo C.
No experimento para decomposição da água, a pressão p exercida por uma massa m de gás hidrogênio coletado no recipiente C, sob temperatura termodinâmica T, pode ser expressa, de acordo com a lei dos gases ideais, por p = K × m × T, em que K é uma constante de proporcionalidade.
Provas

Internet: <www.arts-et-metiers.net>.
Em 1772, o cientista Lavoisier, em seus primeiros trabalhos sobre a combustão, mostrou que determinadas substâncias, como o fósforo, não perdem — mas ganham — massa durante o processo. Onze anos mais tarde, Lavoisier, para decompor a água, elaborou o equipamento ilustrado na figura acima e, utilizando-o, descobriu que a água é uma substância formada por dois elementos: hidrogênio e oxigênio. Em seu experimento, ele colocou em um recipiente (A) uma massa conhecida de água destilada e a fez passar sobre ferro incandescente (B), promovendo a decomposição da água e a obtenção de gás H2, que foi coletado em um recipiente indeformável (C). A seguinte equação química não balanceada retrata essa reação.
Fe(s) + H2O(l) → Fe3O4(s) + H2(g)
Em outro experimento, o gás hidrogênio produzido foi misturado ao gás oxigênio em um balão de vidro — o gasômetro de Lavoisier — e a mistura de gases foi inflamada por uma fagulha elétrica. Pronto: a água líquida tinha sido reconstituída!
Internet: <www.chc.cienciahoje.uol.com.br> (com adaptações).
Considerando o texto acima e os diversos aspectos a ele relacionados, julgue os itens de 83 a 88 e faça o que se pede no item 89, que é do tipo C.
No processo de reconstituição da água realizado no gasômetro de Lavoisier, a fagulha elétrica atuou como catalisador, permitindo a reação entre o hidrogênio e o oxigênio.
Provas

Internet: <www.arts-et-metiers.net>.
Em 1772, o cientista Lavoisier, em seus primeiros trabalhos sobre a combustão, mostrou que determinadas substâncias, como o fósforo, não perdem — mas ganham — massa durante o processo. Onze anos mais tarde, Lavoisier, para decompor a água, elaborou o equipamento ilustrado na figura acima e, utilizando-o, descobriu que a água é uma substância formada por dois elementos: hidrogênio e oxigênio. Em seu experimento, ele colocou em um recipiente (A) uma massa conhecida de água destilada e a fez passar sobre ferro incandescente (B), promovendo a decomposição da água e a obtenção de gás H2, que foi coletado em um recipiente indeformável (C). A seguinte equação química não balanceada retrata essa reação.
Fe(s) + H2O(l) → Fe3O4(s) + H2(g)
Em outro experimento, o gás hidrogênio produzido foi misturado ao gás oxigênio em um balão de vidro — o gasômetro de Lavoisier — e a mistura de gases foi inflamada por uma fagulha elétrica. Pronto: a água líquida tinha sido reconstituída!
Internet: <www.chc.cienciahoje.uol.com.br> (com adaptações).
Considerando o texto acima e os diversos aspectos a ele relacionados, julgue os itens de 83 a 88 e faça o que se pede no item 89, que é do tipo C.
A decomposição da água ocorrida no experimento de Lavoisier é um processo de oxirredução, no qual o ferro incandescente atua como agente oxidante.
Provas
Caderno Container