Foram encontradas 348 questões.
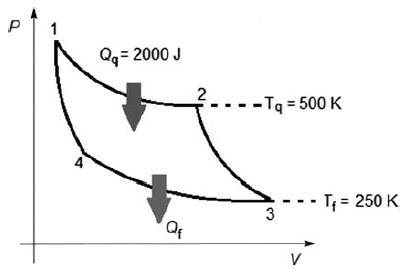
A figura é um diagrama pressão (P) versus volume (V) de um ciclo de Carnot típico a ser obedecido por uma máquina reversível para que ela tenha o melhor rendimento possível. Um exemplo hipotético desse tipo de máquina é o motor do automóvel do personagem Batmam, o chamado batmóvel. Com relação ao diagrama e considerando que o combustível do batmóvel se comporte como um gás ideal, julgue os itens de 145 a 149 e faça o que se pede no item 150, que é do tipo D.
Infere-se do diagrama que a relação entre as pressões e os volumes da isoterma do trecho 1-2 é P1V1 = P2V2.
Provas

A figura é um diagrama pressão (P) versus volume (V) de um ciclo de Carnot típico a ser obedecido por uma máquina reversível para que ela tenha o melhor rendimento possível. Um exemplo hipotético desse tipo de máquina é o motor do automóvel do personagem Batmam, o chamado batmóvel. Com relação ao diagrama e considerando que o combustível do batmóvel se comporte como um gás ideal, julgue os itens de 145 a 149 e faça o que se pede no item 150, que é do tipo D.
O calor Qf cedido à fonte fria é inferior a 750 J.
Provas

A figura é um diagrama pressão (P) versus volume (V) de um ciclo de Carnot típico a ser obedecido por uma máquina reversível para que ela tenha o melhor rendimento possível. Um exemplo hipotético desse tipo de máquina é o motor do automóvel do personagem Batmam, o chamado batmóvel. Com relação ao diagrama e considerando que o combustível do batmóvel se comporte como um gás ideal, julgue os itens de 145 a 149 e faça o que se pede no item 150, que é do tipo D.
Se V2, V3 e P2, P3 são, respectivamente, os volumes e as pressões nos pontos 2 e 3 do diagrama, então a expressão seguinte apresenta uma relação correta entre os calores específicos a pressão (cP) e volume (cV) constantes do processo adiabático no trecho 2-3 do ciclo de Carnot.
cp=cv log!$ \left ( \dfrac{V_3}{V_2} \right ) !$ x log!$ \left ( \dfrac{P_3}{P_2} \right ) !$
Provas

A figura é um diagrama pressão (P) versus volume (V) de um ciclo de Carnot típico a ser obedecido por uma máquina reversível para que ela tenha o melhor rendimento possível. Um exemplo hipotético desse tipo de máquina é o motor do automóvel do personagem Batmam, o chamado batmóvel. Com relação ao diagrama e considerando que o combustível do batmóvel se comporte como um gás ideal, julgue os itens de 145 a 149 e faça o que se pede no item 150, que é do tipo D.
O motor do batmóvel deve alcançar um rendimento de 100%, dada a hipótese de que ele seja uma máquina que obedece ao ciclo de Carnot.
Provas

A figura é um diagrama pressão (P) versus volume (V) de um ciclo de Carnot típico a ser obedecido por uma máquina reversível para que ela tenha o melhor rendimento possível. Um exemplo hipotético desse tipo de máquina é o motor do automóvel do personagem Batmam, o chamado batmóvel. Com relação ao diagrama e considerando que o combustível do batmóvel se comporte como um gás ideal, julgue os itens de 145 a 149 e faça o que se pede no item 150, que é do tipo D.
Um processo é considerado reversível quando o sistema passa de um estado inicial de equilíbrio para um estado final de equilíbrio mediante uma sucessão de estados de equilíbrio termodinâmico.
Provas
O morador de uma cidade invadida por zumbis leu que eles poderiam ser eliminados se transpassados por uma estaca de prata. Como não havia estaca de prata disponível, o morador utilizou uma estaca de aço, sobre a qual depositou prata por meio da eletrólise de uma solução aquosa de AgNO3.
Em relação à situação apresentada e aos múltiplos aspectos a ela relacionados, julgue os itens de 114 a 119, considerando que a constante de Faraday seja igual a 96.500 C/mol e que, no anodo da célula, ocorra oxidação da água.
O pH da solução submetida ao processo de eletrólise irá aumentar à medida que a prata for depositada.
Provas
O morador de uma cidade invadida por zumbis leu que eles poderiam ser eliminados se transpassados por uma estaca de prata. Como não havia estaca de prata disponível, o morador utilizou uma estaca de aço, sobre a qual depositou prata por meio da eletrólise de uma solução aquosa de AgNO3.
Em relação à situação apresentada e aos múltiplos aspectos a ela relacionados, julgue os itens de 114 a 119, considerando que a constante de Faraday seja igual a 96.500 C/mol e que, no anodo da célula, ocorra oxidação da água.
Se o indivíduo da situação hipotética desejasse recobrir a estaca com 21,58 g de prata, empregando uma corrente constante de 10,0 A, ele deveria conduzir o processo de deposição por período de tempo superior a 30 min.
Provas
O morador de uma cidade invadida por zumbis leu que eles poderiam ser eliminados se transpassados por uma estaca de prata. Como não havia estaca de prata disponível, o morador utilizou uma estaca de aço, sobre a qual depositou prata por meio da eletrólise de uma solução aquosa de AgNO3.
Em relação à situação apresentada e aos múltiplos aspectos a ela relacionados, julgue os itens de 114 a 119, considerando que a constante de Faraday seja igual a 96.500 C/mol e que, no anodo da célula, ocorra oxidação da água.
A equação apresentada a seguir é a equação balanceada para a reação de oxirredução verificada durante a eletrólise da solução de AgNO3.
Ag+ (aq) + 2H2O (l) 6 Ag (s) + O2 (g) + 4H+ (aq)
Provas
O morador de uma cidade invadida por zumbis leu que eles poderiam ser eliminados se transpassados por uma estaca de prata. Como não havia estaca de prata disponível, o morador utilizou uma estaca de aço, sobre a qual depositou prata por meio da eletrólise de uma solução aquosa de AgNO3.
Em relação à situação apresentada e aos múltiplos aspectos a ela relacionados, julgue os itens de 114 a 119, considerando que a constante de Faraday seja igual a 96.500 C/mol e que, no anodo da célula, ocorra oxidação da água.
A solução aquosa de AgNO3 apresenta pH básico.
Provas
O morador de uma cidade invadida por zumbis leu que eles poderiam ser eliminados se transpassados por uma estaca de prata. Como não havia estaca de prata disponível, o morador utilizou uma estaca de aço, sobre a qual depositou prata por meio da eletrólise de uma solução aquosa de AgNO3.
Em relação à situação apresentada e aos múltiplos aspectos a ela relacionados, julgue os itens de 114 a 119, considerando que a constante de Faraday seja igual a 96.500 C/mol e que, no anodo da célula, ocorra oxidação da água.
Considerando-se que a massa atômica da prata seja de 107,9 u e que apenas os isótopos 107Ag e 109Ag contribuam de forma significativa para a ocorrência natural desse elemento, é correto concluir que, na prata, o isótopo 109Ag tem maior abundância isotópica que o isótopo 107Ag.
Provas
Caderno Container